Clear Sky Science · ru
Диета с высоким содержанием жиров перестраивает сети регуляции генов в преоптической области
Почему ваш мозг имеет значение при диабете
Большинство людей воспринимают диабет прежде всего как проблему поджелудочной железы и уровня глюкозы в крови, но мозг тоже играет в этом важную роль. В этом исследовании рассматривается, как диета с высоким содержанием жиров и мощное экспериментальное лечение изменяют активность генов в небольшой, но значимой области мозга — преоптической области. Картируя, какие клетки мозга «сбросились» при наступлении ремиссии диабета, исследователи надеются указать путь к новым терапиям, которые используют собственные способности мозга помогать контролировать уровень сахара в крови.
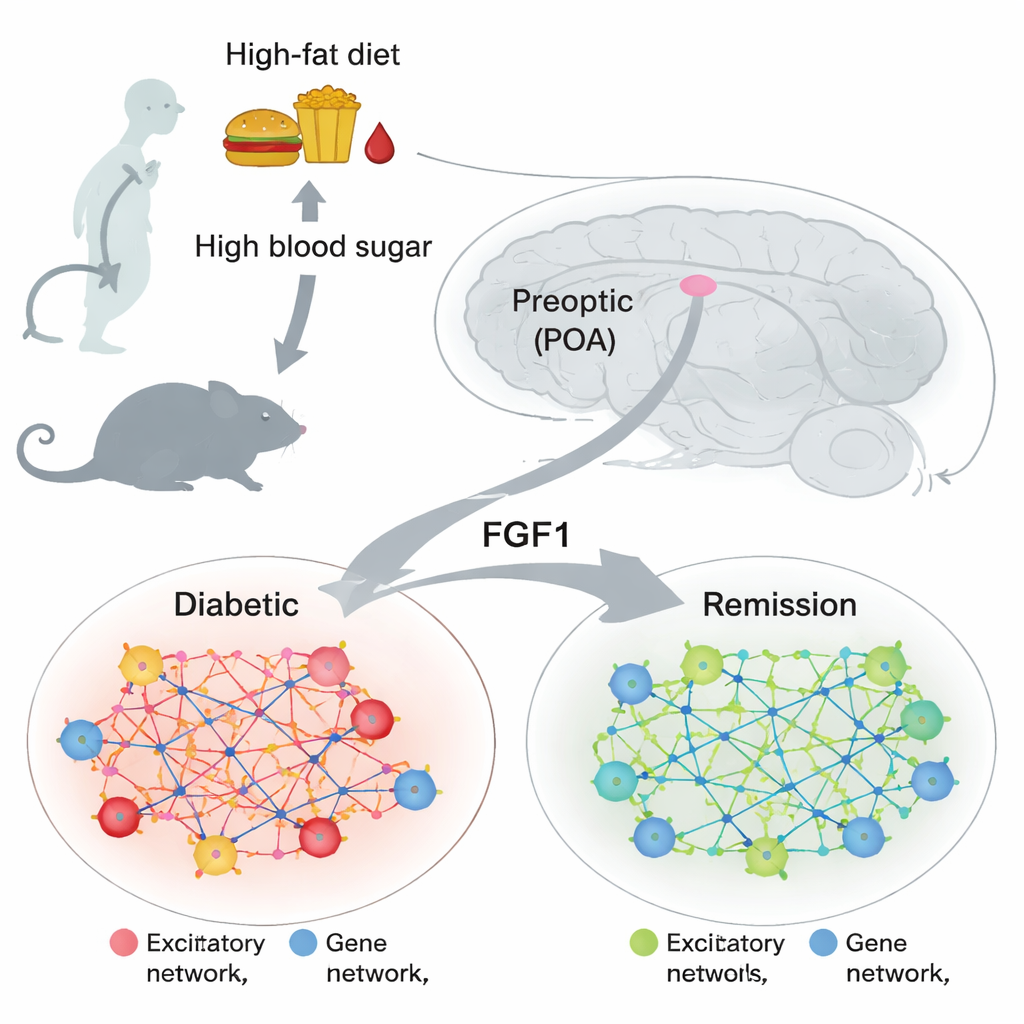
Небольшой мозговой узел с большим метаболическим влиянием
Преоптическая область расположена в передней части гипоталамуса — участка мозга, который участвует в регуляции температуры тела, сна, питания и гормональных сигналов. Ранние исследования показали, что клетки в этой области могут влиять на то, как организм обрабатывает глюкозу и реагирует на тепло, но их роль в диабете была мало изучена. В то же время другие работы продемонстрировали, что однократное введение белка фибробластного фактора роста 1 (FGF1) в мозг может привести к длительной ремиссии у ожиревших диабетических мышей. Это подняло важный вопрос: какие клетки мозга и какие генетические программы меняются при нормализации уровня сахара, и появляются ли похожие изменения в преоптической области?
Чтение активности генов по одной клетке
Чтобы ответить на этот вопрос, команда применила одноклеточный РНК-секвенирование — метод, который измеряет, какие гены включены в тысячах отдельных клеток одновременно. Они повторно проанализировали существующий набор данных от мышей, у которых наступила ремиссия после лечения FGF1, сосредоточившись на нервных клетках гипоталамуса. С помощью статистических методов они выделили группы генов, которые повышались или понижались вместе по мере перехода животных из состояния диабета в ремиссию. Эти «модули ремиссии» действуют как отпечатки восстановления: вместо отслеживания одного гена за раз они фиксируют согласованные сдвиги в большом числе генов внутри определённых типов нейронов.
Диета с высоким содержанием жиров, клетки мозга и снижение расхода энергии
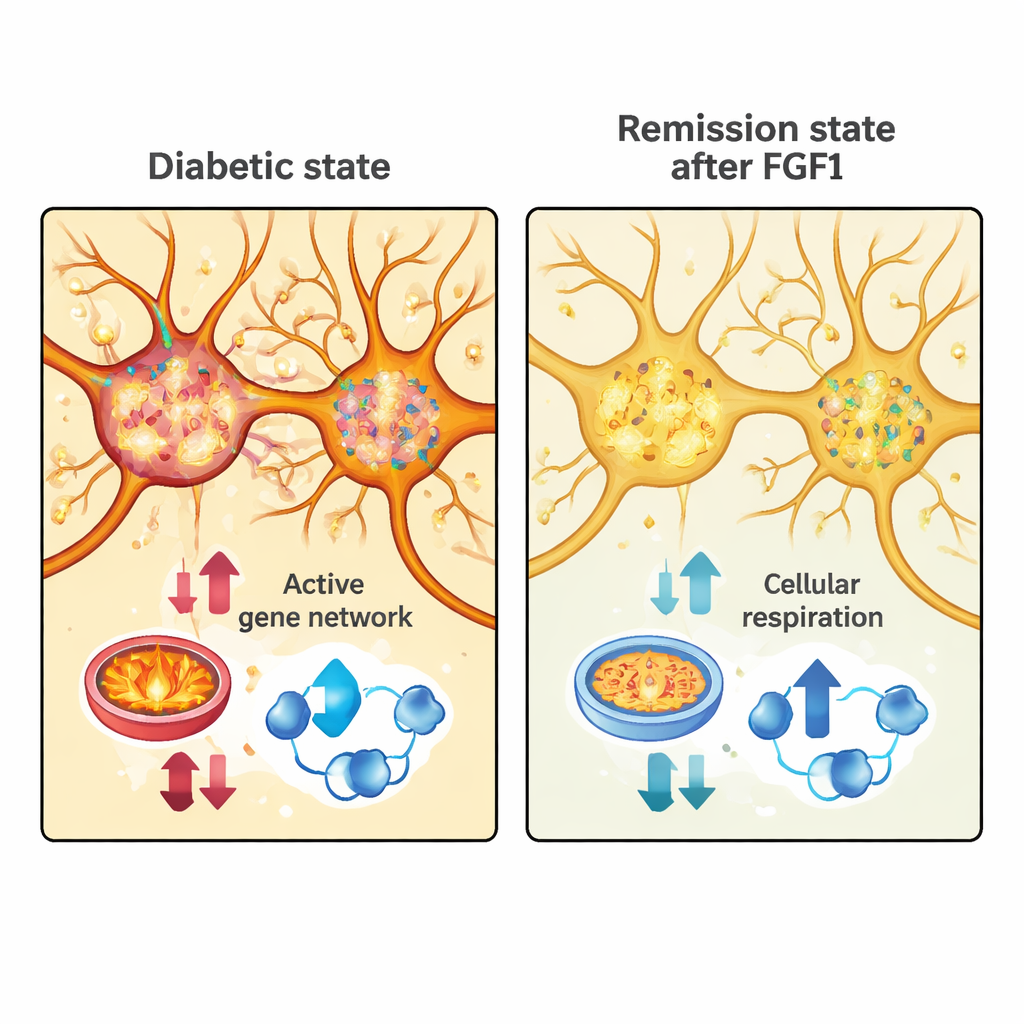
Затем исследователи сравнили эти модули ремиссии с активностью генов в другом наборе данных, в котором были отобраны клетки из преоптической области нормальных мышей. Сначала они разделили нейроны на два широких класса: возбуждающие клетки, которые обычно увеличивают активность в своих цепях, и тормозные клетки, которые её подавляют. У диабетических мышей, получивших FGF1, оба типа нейронов показывали широкое снижение экспрессии генов, связанных с производством энергии — особенно тех, что участвуют в окислительном фосфорилировании, клеточном дыхании и митохондриальном аппарате, питающем активные клетки. В возбуждающих нейронах большой «бирюзовый» генный модуль, связанный с использованием энергии и синаптической активностью, был значительно подавлен в ремиссии, что указывает на то, что эти клетки становятся менее метаболически требовательными при нормализации уровня сахара в крови.
Прослеживание подписей ремиссии до конкретных групп нейронов
Далее команда поинтересовалась, совпадают ли эти связанные с ремиссией генетические паттерны с конкретными популяциями клеток в преоптической области. Путём вычислительного объединения двух наборов данных они обнаружили, что некоторые кластеры нейронов преоптической области экспрессировали многие из тех же генов, которые менялись при ремиссии, индуцированной FGF1. Они выделили несколько генов — таких как Trpc4, Dgkg и Ryr3 — которые оказались в перекрёстке этих анализов. С помощью высокочувствительного метода микроскопии RNAscope они показали, что эти гены действительно экспрессируются в отдельных зонах преоптической области мыши, преимущественно в дорсальных субрегионах. Это подтверждает их как реальные маркеры конкретных групп нейронов, которые могут участвовать в реакции мозга на метаболическое заболевание.
Что это значит для будущих методов лечения диабета
Для неспециалистов основная идея в том, что диабет — это не только проблема уровня сахара в крови, но и проблема сетей в мозге. Исследование показывает, что при наступлении ремиссии у мышей определённые нейроны преоптической области переходят в состояние пониженного расхода энергии и координируют изменения в активности генов. Определяя эти модули ремиссии и связывая их с конкретными типами клеток и маркерными генами, работа предоставляет дорожную карту для будущих экспериментов: исследователи теперь могут целенаправленно воздействовать на эти нейроны, чтобы проверить, как они влияют на контроль глюкозы, ожирение и сопутствующие осложнения. В долгосрочной перспективе лучшее понимание этих мозговых контуров может помочь вдохновить терапии, дополняющие или даже обходящие отказывающие органы, используя встроенный контроль обмена веществ со стороны мозга.
Цитирование: Lazaro, O., Beimfohr, C., App, B. et al. High fat diet remodels the gene regulatory networks in the preoptic area. Sci Rep 16, 7042 (2026). https://doi.org/10.1038/s41598-026-37692-8
Ключевые слова: мозг и сахарный диабет, преоптическая область, диета с высоким содержанием жиров, генные сети, ремиссия после FGF1