Clear Sky Science · ru
Метод обнаружения структурных вариантов с использованием матрицы контактов Hi-C и нейронных сетей
Почему важно, как ДНК сгибается в 3D
Наша ДНК обычно изображается как простая строка букв, но внутри каждой клетки она складывается в сложную трёхмерную форму. Когда большие фрагменты этой строки удаляются, переворачиваются или перемещаются — изменения, называемые структурными вариантами — они могут нарушать работу генов и способствовать развитию рака. В этой работе представлен VarHiCNet, новая система искусственного интеллекта, которая «читает» карты 3D-складывания ДНК и обнаруживает такие рискованные крупномасштабные изменения точнее, чем существующие инструменты, предлагая новый подход к изучению раковых геномов и других заболеваний.
Видеть изменения генома через 3D-карты контактов
Традиционные тесты генома считывают ДНК как прямую последовательность, что затрудняет обнаружение сложных перестроек, особенно в повторяющихся областях или когда фрагменты перемещаются без изменения числа копий. Методика Hi-C решает задачу иначе: она измеряет, как часто удалённые участки ДНК физически соприкасаются в ядре, а затем записывает эти контакты в виде сетки — матрицы контактов, где более яркие точки означают сильное взаимодействие. Структурные варианты оставляют характерные отпечатки в этих матрицах — например, отсутствующие «полосы», когда регион удалён, зеркальные паттерны при инверсиях или внедиагональные горячие точки при слиянии двух хромосом. VarHiCNet разработан для автоматического распознавания этих визуальных шаблонов.
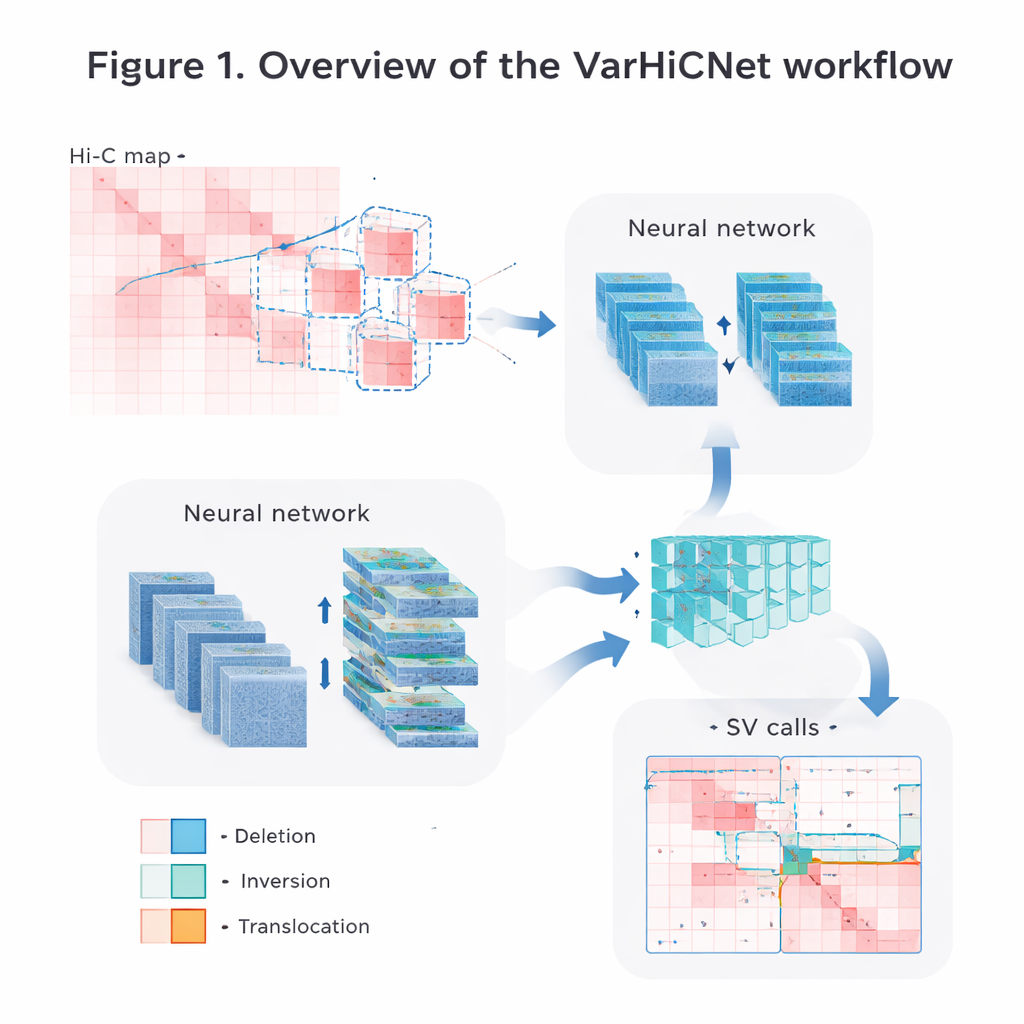
Преобразование карт генома в изображения для ИИ
Авторы преобразуют сырые данные Hi-C в изображения, которые легко обрабатывают системы компьютерного зрения. Сначала матрицы аккуратно нормализуют, чтобы скорректировать естественное падение частоты контактов с увеличением расстояния между сегментами ДНК, при этом сохраняя сигналы как ближайших, так и дальних взаимодействий. Затем они сканируют каждую хромосому перекрывающимися квадратными окнами и вырезают множество меньших подматриц. Каждая подматрица масштабируется до стандартизированного цветного изображения размером 800 на 800 пикселей, где разные силы контактов кодируются оттенками красного в трёх цветовых каналах. Такое представление в виде изображения позволяет модели применять мощные приёмы, изначально разработанные для распознавания объектов на фотографиях.
Заимствование приёмов из детекции объектов
VarHiCNet рассматривает каждый потенциальный структурный вариант как «объект» на изображении. Он основан на современной архитектуре детекции объектов RT-DETR, которая сочетает свёрточные нейронные сети и трансформеры для выделения важных областей. РесНет-бэкбон сначала извлекает многоуровневые признаки: мелкие слои сохраняют тонкие детали, необходимые для точного определения точек разрыва, в то время как глубокие слои улавливают более широкие паттерны, сигнализирующие о крупных событиях. Модуль слияния признаков затем объединяет информацию из нескольких слоёв, чтобы сохранить и локальные, и глобальные подсказки. Ещё один пользовательский блок, вдохновлённый пространственным пирамидальным пуллингом, регулирует объём окружающей области, «видимой» модели за один раз, делая её чувствительной к вариантам, охватывающим диапазон от относительно небольших до очень больших участков ДНК.
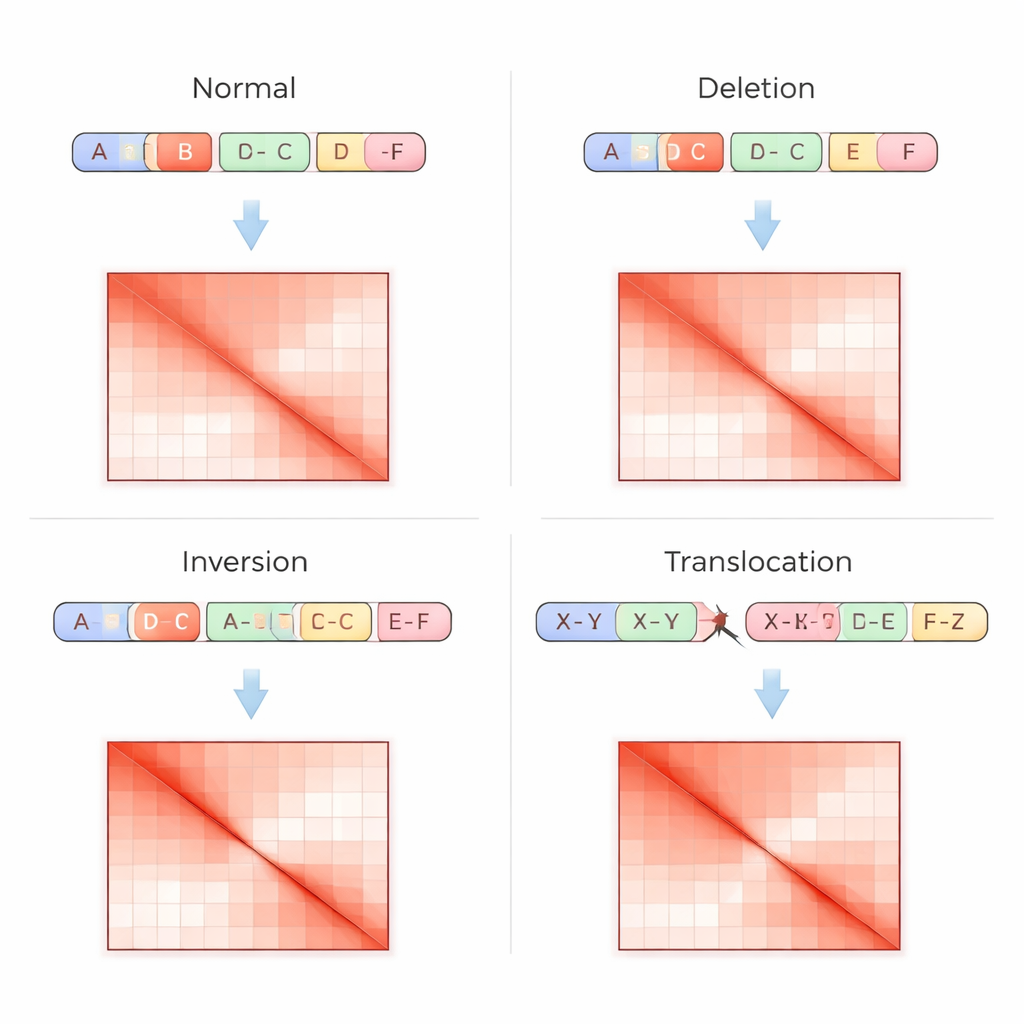
От кандидатных регионов к точным типам вариантов
Когда VarHiCNet предлагает кандидатные регионы на изображении Hi-C, его задача — уточнить их до точных точек разрыва и конкретных типов вариантов, таких как делеции, инверсии, дупликации или транслокации. Для этого система увеличивает район вокруг каждой предсказанной точки разрыва и уменьшает его размерность с помощью метода главных компонент (PCA), который выделяет места, где паттерн контактов меняется наиболее резко. Эти компактные представления затем подаются в классификатор на основе трансформера, который обучается различать тонкие отличия локальных паттернов для каждой категории варианта. В результате получается детализированная запись для каждого события: где оно происходит в геноме и какой тип структурного изменения ему соответствует.
Работа на разных линиях раковых клеток
Исследователи протестировали VarHiCNet на данных Hi-C из шести различных человеческих раковых клеточных линий, охватывающих опухоли крови, молочной железы, мозга, почки, лёгкого и предстательной железы. Используя каталог высоконадежных известных структурных вариантов в качестве эталона, они сравнили свой метод с несколькими ведущими инструментами анализа Hi-C. По событиям как внутри одной хромосомы, так и между хромосомами VarHiCNet в целом достигал более высоких или сопоставимых F1-оценок, что означает лучшее сочетание чувствительности и точности по сравнению с другими подходами. Особенно хорошо он справлялся с обнаружением сбалансированных транслокаций и инверсий — перестроек, которые часто мало проявляются в стандартном секвенировании, но дают чёткие 3D-подписи. Авторы также показали, что их архитектурные решения, такие как разрешение изображения и модули слияния признаков, последовательно улучшали результаты в контролируемых тестах.
Что это значит для понимания болезней
Проще говоря, VarHiCNet даёт учёным более интеллектуальный способ «видеть», как геном складывается в 3D, и обнаруживать крупные, связные с болезнью перестройки, которые могут быть пропущены при обычном секвенировании. Преобразуя сложные карты контактов в изображения и применяя современные нейросети в стиле компьютерного зрения, метод способен надёжно обнаруживать и классифицировать многие типы структурных вариантов в разных типах раковых клеток. Хотя он всё ещё испытывает трудности с очень малыми или сильно запутанными изменениями и зависит от насыщенных обучающих данных, VarHiCNet указывает на будущее, в котором трёхмерная архитектура генома станет рутинной частью того, как мы читаем, интерпретируем и в конечном итоге нацеливаем генетические изменения, лежащие в основе рака и других заболеваний.
Цитирование: Shen, J., Wang, H., Zhai, H. et al. A method for structural variant detection using Hi-C contact matrix and neural networks. Sci Rep 16, 7324 (2026). https://doi.org/10.1038/s41598-026-37678-6
Ключевые слова: структурные варианты, Hi-C, глубокое обучение, геномика рака, 3D-геном