Clear Sky Science · ru
Идентификация вредоносных вариантов в кандидатных генах, связанных с коровьим паратуберкулезом, по всему транскриптому
Скрытые гены за дорогостоящим заболеванием крупного рогатого скота
Коровий паратуберкулез, также известный как болезнь Джонса, тихо подрывает здоровье и продуктивность молочных стад по всему миру, обходясь фермерам в сотни миллионов долларов ежегодно и вызывая опасения в связи с возможной связью с кишечными заболеваниями у людей. В этом исследовании заглянули «под капот» генома голштинских коров, задав простой, но важный вопрос: какие различия в их генах могут помочь одним животным противостоять инфекции, в то время как другие ей подвержены? Читая РНК — рабочие копии генов — в крови и кишечных тканях, исследователи проследили, как тонкие изменения в ДНК ключевых иммунных генов могут направлять развитие болезни.
Почему это заболевание коров имеет значение
Паратуберкулез вызывается бактерией Mycobacterium avium подвид paratuberculosis (MAP). Коровы обычно заражаются рано в жизни, но признаки часто проявляются спустя годы. На бессимптомных и доклинических стадиях животные выглядят здоровыми, но могут выделять низкие уровни бактерий и давать меньше молока. На клинической стадии развиваются хроническая диарея, сильная потеря веса и значительное снижение удоев. Уровни заражения на уровне стада могут превышать 50% во многих регионах, включая части Европы и Северной Америки, создавая экономическую и зоозащитную проблему. Поскольку бактерия может выступать в роли триггера для человеческих воспалительных заболеваний, таких как болезнь Крона, усиливается давление по улучшению стратегий контроля в скотоводстве.
Чтение рабочего генома
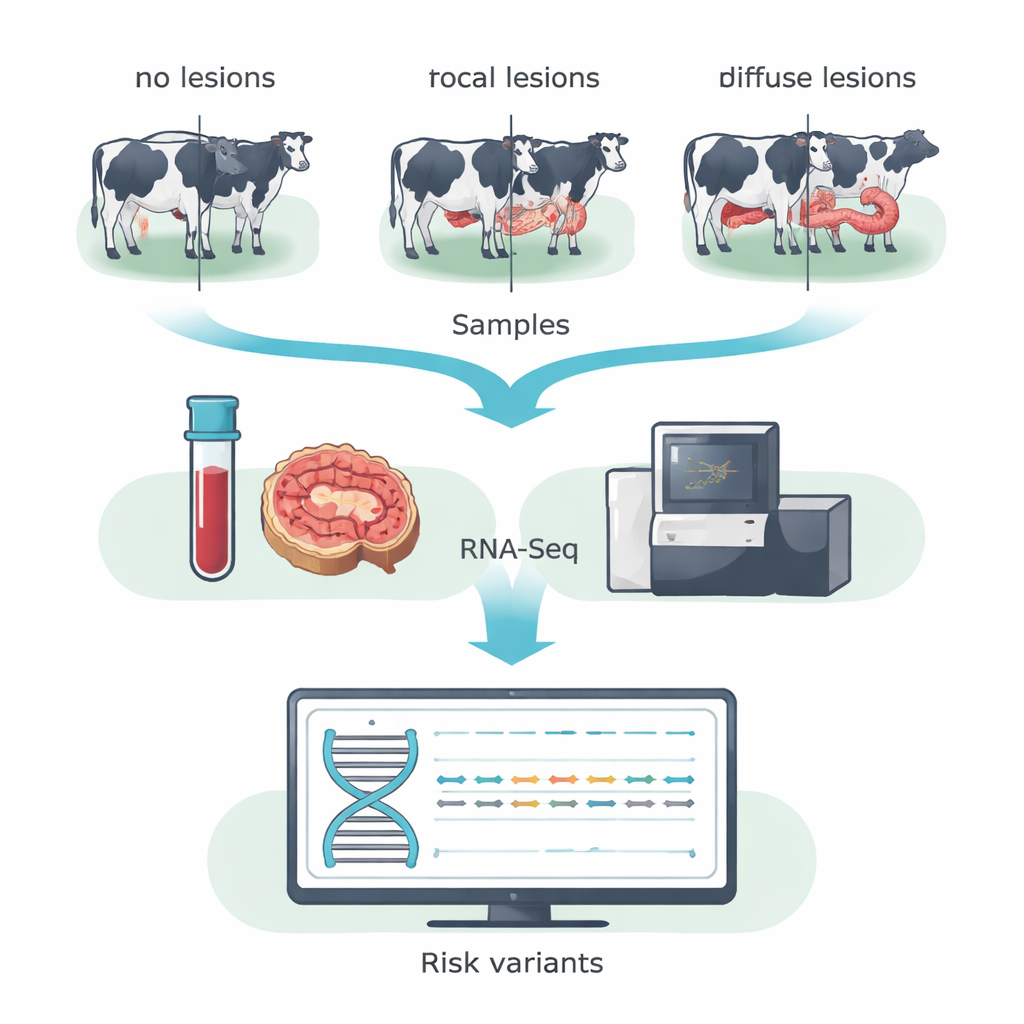
Вместо сканирования всей последовательности ДНК команда использовала РНК‑секвенирование (RNA‑Seq), чтобы сфокусироваться на генах, которые действительно активны в животном. Они собрали кровь и образцы из илеоцекального клапана — участка кишечника, сильно поражаемого MAP — от 14 голштинских коров на испанской молочной ферме. На основании микроскопического исследования кишечных тканей коров разделили на три категории: животные без обнаруживаемых поражений, животные с небольшими локализованными (фокальными) поражениями, типичными для длительной доклинической инфекции, и животные с тяжелыми, широко распространенными (диффузными) поражениями, связанными с клинической формой болезни. Объединив данные крови и кишечника внутри каждой группы, исследователи повысили способность обнаруживать однонуклеотидные варианты в кодирующих последовательностях экспрессируемых генов.
Поиск вредоносных изменений в ключевых иммунных генах
Из сотен тысяч вариантов команда сосредоточилась на тех, которые меняют последовательность белка и, по прогнозам, нарушают его функцию — так называемых вредоносных вариантов. Они применили строгие фильтры для обеспечения высокой достоверности, а затем использовали устоявшиеся инструменты предсказания, чтобы пометить рискованные изменения. В результате отбора выявили 31 такой вариант, уникальный для коров без поражений, 15 уникальных для коров с фокальными поражениями и 31 уникальный для коров с диффузными поражениями. Многие из них локализовались в генах, управляющих распознаванием и устранением инфекций иммунными клетками, регуляцией клеточной гибели и метаболизмом. Особое внимание привлекла семья генов BOLA — бычья версия главного комплекса гистосовместимости класса II, помогающая иммунным клеткам представлять фрагменты бактерий Т‑клеткам. Различные потенциально вредоносные варианты в BOLA были обнаружены во всех трех группах, что указывает на то, что конкретные версии BOLA могут склонять животных к устойчивости, контролируемой инфекции или вредному воспалению.
От вариантов ДНК к путям болезни
Чтобы понять практическое значение этих изменений, исследователи проанализировали, какие биологические пути обогащены в каждой группе. У коров без поражений были обнаружены измененные варианты в генах, связанных с обработкой антигенов, везикулярным транспортом и кишечным иммунным балансом, включая BOLA, AP3B1 и CHGA. Эти изменения могут способствовать эффективному перевариванию бактерий в иммунных клетках и созданию стабильной среды в кишечнике, ограничивающей повреждения. У коров с фокальными поражениями вредоносные варианты сосредоточились в генах (ORMDL3 и KANK2), которые подавляют программируемую клеточную гибель и настраивают клеточный метаболизм, что потенциально помогает хозяину удерживать низкую численность бактерий в течение длительной доклинической фазы. У коров с диффузными поражениями затронутые гены указывали на чрезмерную активность иммунных путей, таких как дифференцировка Th1/Th2 и презентация антигенов, а также на пути транспорта желчных кислот и ответа на лекарства. Здесь измененные гены семейства BOLA могут вызывать сильную, иногда самоповреждающую воспалительную реакцию, перекликающуюся с паттернами, наблюдаемыми при многих аутоиммунных и воспалительных заболеваниях у людей.
Подсказки для разведения более устойчивых стад
Помимо прояснения того, как разные генетические варианты формируют иммунный ответ на MAP, исследование также связало эти рискованные изменения с известными регионами бычьего генома, ассоциированными со здоровьем, включая восприимчивость к паратуберкулезу и другим инфекциям. Хотя эти результаты требуют проверки на больших стадах и пока не могут служить автономными диагностическими маркерами, они предлагают перспективный каталог кандидатных вариантов и генов. Проще говоря, работа показывает, что некоторые коровы несут версии генов, помогающие им тихо контролировать инфекцию, в то время как другие несут версии, склоняющие к неконтролируемому воспалению и тяжелому течению болезни. В будущем такая информация может поддержать селекцию и генетическое тестирование, направленные на повышение естественной устойчивости стад, что снизит экономические потери и потребность в интенсивных мерах контроля заболеваний.
Цитирование: Badia-Bringué, G., Lam, S., Cánovas, Á. et al. Whole-transcriptome identification of deleterious variants in candidate genes linked to bovine paratuberculosis. Sci Rep 16, 6243 (2026). https://doi.org/10.1038/s41598-026-37675-9
Ключевые слова: коровий паратуберкулез, генетика болезни Джонса, иммунитет молочного скота, РНК‑секвенирование, селекция на устойчивость к болезням