Clear Sky Science · ru
Wnt-3a усугубляет продукцию TNF-α в микроglии, стимулированной LPS, независимо от канонического пути β-катенин
Почему воспаление мозга важно
Многие заболевания мозга, включая болезнь Паркинсона, сегодня рассматриваются как связанные с хроническим воспалением. В этом процессе резидентные иммунные клетки мозга — микроглия — могут переключаться из защитного состояния в чрезмерно активные атакующие клетки, наносящие вред соседним нейронам. В данном исследовании поставлен своевременный вопрос: может ли сигнальная молекула Wnt‑3a, долгое время считавшаяся успокаивающей и защитной, на самом деле усиливать воспаление при определённых условиях? Ответ оказался сложнее, чем ожидали, и подчёркивает, почему одна и та же молекула может быть полезной в одном контексте и вредной в другом.
Посланник с двумя лицами
Белки Wnt — это семейство химических посредников, которые направляют развитие мозга, поддерживают клетки мозга во взрослом состоянии и формируют реакцию клеток на повреждение. Один из наиболее изученных членов, Wnt‑3a, обычно ассоциируется с «каноническим» сигнальным путём, стабилизирующим в клетках белок β‑катенин. Во многих системах активация этого пути, как правило, подавляет воспаление и поддерживает выживание нейронов, поэтому некоторые исследователи предполагали, что усиление Wnt‑3a может защитить уязвимые дофаминергические нейроны при болезни Паркинсона. Однако белки Wnt также могут сигнализировать через альтернативные, «неканонические» пути, которые, наоборот, могут стимулировать воспаление, и доминирующий путь зависит от типа клетки и её состояния.
Когда спокойные клетки остаются спокойными
Чтобы изучить эти возможности, учёные исследовали первичные микроглиальные культуры, полученные из мозга мышей. Сначала они посмотрели на микроглию в состоянии покоя и обработали её только Wnt‑3a. При этих спокойных условиях Wnt‑3a не увеличивал выброс ключевых провоспалительных молекул, таких как TNF‑α или IL‑1β. Хотя внутри клеток активировалась некоторая сигнализация, микроглия не переходила в ярко выраженный воспалительный режим. Это указывает на то, что в здоровом, невоспалённом мозге введение Wnt‑3a само по себе вряд ли сильно повлияет на воспалительную активность микроглии.
Когда воспалённые клетки дополнительно подталкивают
Картина резко изменилась, когда микроглию предварительно активировали липополисахаридом (LPS), стандартным лабораторным средством для моделирования инфекции. Как и ожидалось, LPS сам вызывал сильное повышение продукции TNF‑α. Но при одновременном воздействии Wnt‑3a и LPS микроглия выделяла значительно больше TNF‑α, чем при воздействии только LPS, тогда как IL‑1β дополнительно не увеличивалась. Точные измерения показали, что это усиление TNF‑α не объясняется большей активацией обычного NFκB‑маршрута воспаления или дополнительной активацией канонического пути β‑катенин. Блокирование пути β‑катенин белком DKK1 не уничтожало прирост TNF‑α, вызванный Wnt‑3a, что указывает на то, что ожидаемый «антивоспалительный» путь не был ответственен.
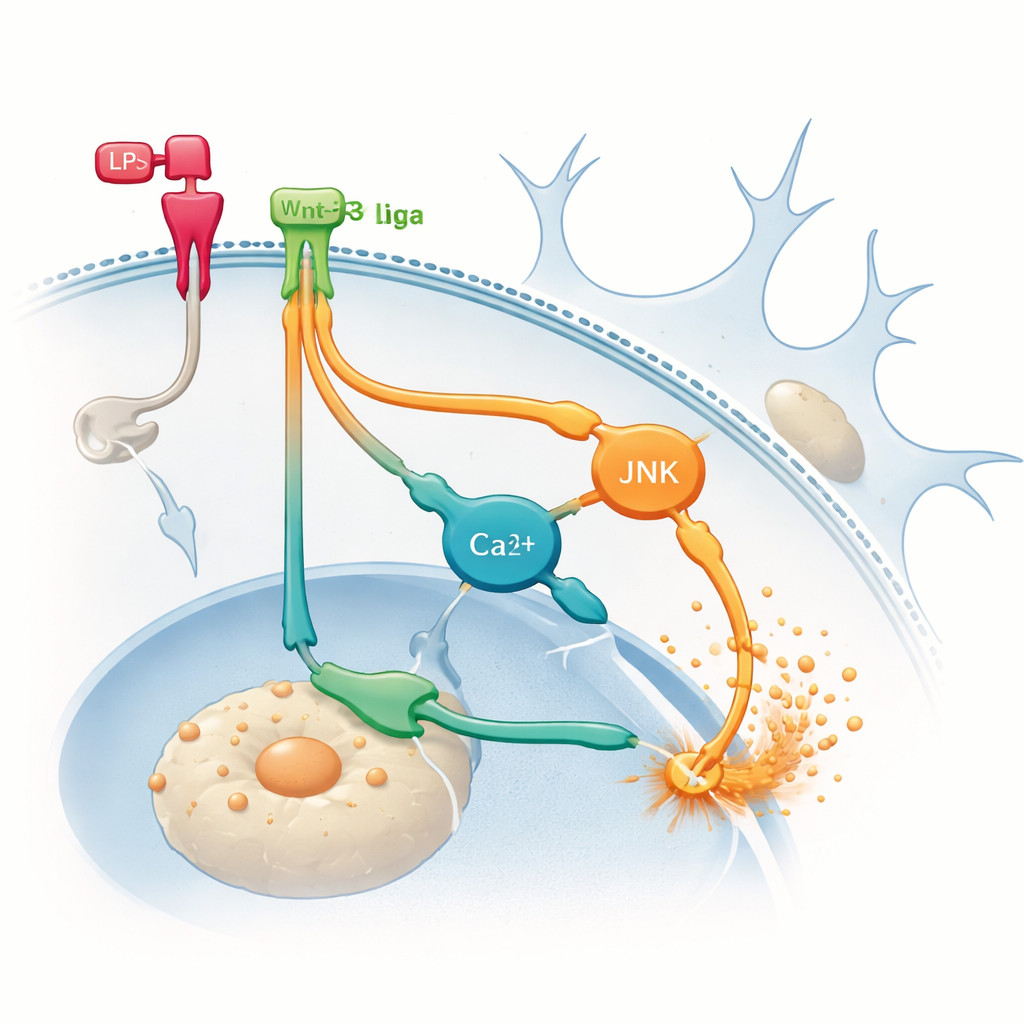
Скрытые маршруты, подбрасывающие дрова
Чтобы выяснить источник дополнительного воспаления, исследователи обратились к альтернативным неконаноническим путям, которые могут использовать белки Wnt. Они фармакологически блокировали две сигнальные ветви в микроглии: одну, связанную с белком JNK, и другую, зависящую от изменений уровня кальция внутри клетки. Ингибирование любой из этих ветвей снижало продукцию TNF‑α, индуцированную LPS, и, что важно, препятствовало дальнейшему усилению TNF‑α под действием Wnt‑3a. Эти результаты позволяют предположить, что, когда микроглия уже воспалена, Wnt‑3a может переключаться на преимущественное использование неканонических путей, которые усиливают воспалительные сигналы, а не успокаивают их. Другими словами, один и тот же посланник может выбрать другой внутренний путь в зависимости от исходного состояния клетки, с крайне разными последствиями.
Испытание в модели болезни Паркинсона
Далее учёные поинтересовались, перенесётся ли поведение Wnt‑3a в микроглии на более масштабные эффекты для нейронов в живом мозге. Они инфузировали Wnt‑3a непосредственно в желудочки мозга мышей, получавших токсин MPTP — широко используемую модель паркинсонического повреждения дофаминергических нейронов и активации микроглии. Как и ожидалось, MPTP уменьшал число дофаминергических нейронов и увеличивал количество микроглии в средней части мозга, важной для контроля движения. Однако дополнительный Wnt‑3a не усугублял дальше потерю нейронов и существенно не изменял число микроглии по сравнению с животными, получавшими растворитель. В этой сложной in vivo-ситуации Wnt‑3a в изученный временной промежуток ни спасал, ни явно не усугублял повреждающее действие токсина.
Что это значит для будущих терапий
В целом исследование показывает, что Wnt‑3a не является простым выключателем воспаления мозга. В спокойной микроглии он оказывает мало влияния, но в уже воспалённых клетках может селективно увеличивать выброс TNF‑α через неканонические сигнальные пути, независимо от классического пути β‑катенин. Одновременно введение Wnt‑3a в модели болезни Паркинсона у мышей в коротком временном отрезке не продемонстрировало явной защиты или дополнительного вреда дофаминергическим нейронам. Для тех, кто разрабатывает будущие терапии, ключевой вывод таков: вмешательство в Wnt‑сигналы потребует тщательной оценки клеточного контекста. Терапии на основе Wnt‑3a или родственных молекул могут помочь в одних ситуациях, но в других — непреднамеренно усилить вредное воспаление.
Цитирование: Federici, G., Stayte, S., Rentsch, P. et al. Wnt-3a exacerbates production of TNF-α in LPS stimulated microglia independent of the β-catenin canonical pathway. Sci Rep 16, 8222 (2026). https://doi.org/10.1038/s41598-026-37653-1
Ключевые слова: воспаление мозга, микроглия, Wnt-сигнальные пути, болезнь Паркинсона, TNF-альфа