Clear Sky Science · ru
Пулы APOL1 в плазматической мембране сопротивляются быстрому разрушению белка
Почему «исчезновение» белка почки важно
Значительная доля тяжелых заболеваний почек у людей с недавним африканским происхождением связана с двумя вариантами одного гена — APOL1. Тем не менее учёным всё ещё трудно объяснить, как этот ген повреждает клетки почки, не причиняя вреда большинству носителей. В этом исследовании рассматривается на вид простой, но важный вопрос: как долго белок APOL1 сохраняется после синтеза внутри клетки и в каких локализациях он наиболее стабилен? Ответы выявляют неожиданную двойственность — APOL1 быстро уничтожается внутри клетки, но остаётся упрямо стабильным, когда встроен в наружную поверхность клетки, что даёт ключ к возможным терапевтическим стратегиям.
Ген риска с двойным эффектом
Ген APOL1 помогает защищать человека от некоторых паразитов — эволюционное преимущество, которое, вероятно, объясняет высокую частоту рискованных вариантов, называемых G1 и G2, в африканских популяциях. К сожалению, люди, унаследовавшие две копии этих вариантов, сталкиваются со значительно повышенным риском заболеваний почек, объединяемых как APOL1-опосредованные заболевания почек. Ранее показали, что при повышении уровня APOL1 — часто в ответ на воспаление — белок может становиться токсичным, особенно для хрупких фильтрующих клеток почки, называемых подоцитами. Но большинство исследований сосредотачивалось на том, что включает APOL1. Намного меньше известно о том, как клетки выключают его, например через разрушение белка.
Отслеживание нестойкого белка внутри клетки
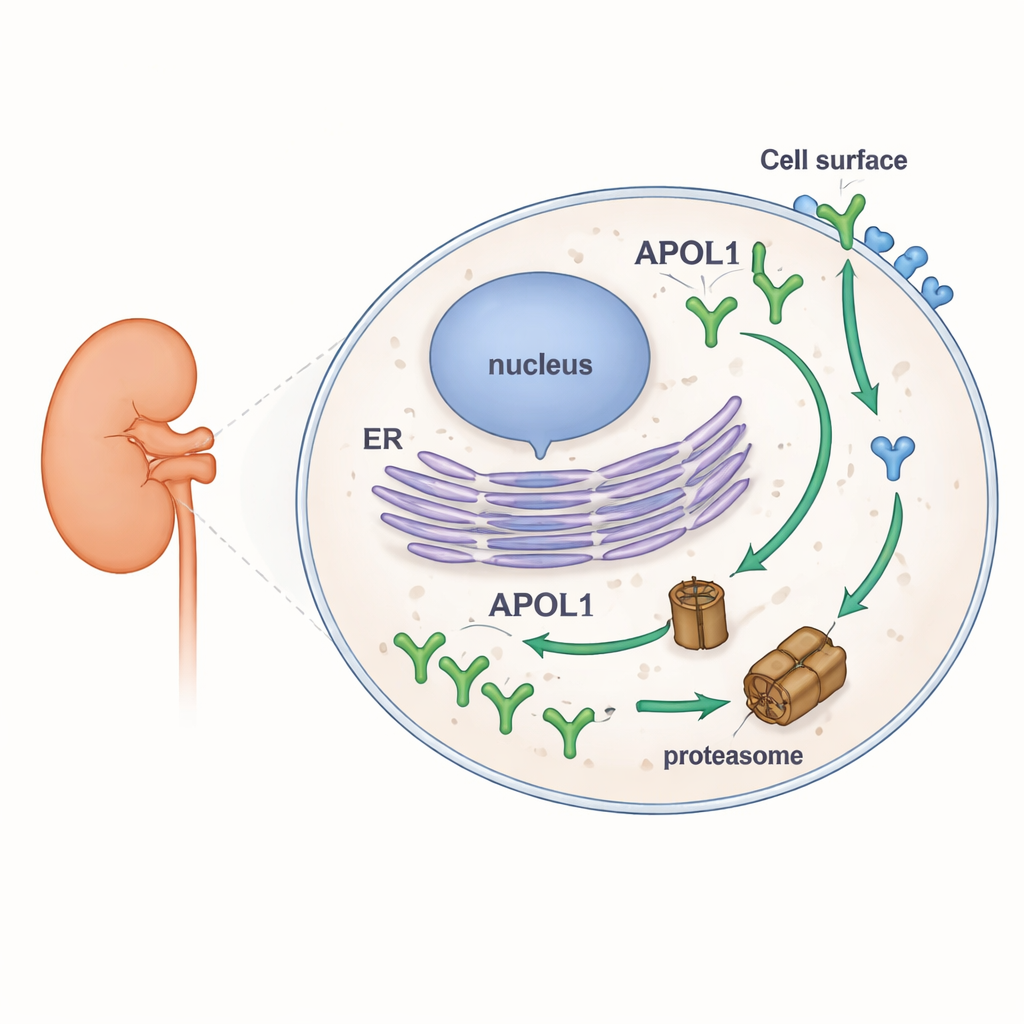
Чтобы изучить стабильность APOL1, исследователи создали линии человеческих клеток, производившие флуоресцентно меченые версии APOL1 и его ближайшего родственника APOL2. Это позволило наблюдать, как меняется количество каждого белка при разных условиях с помощью вестерн-блоттинга, микроскопии и проточной цитометрии. Они блокировали основную систему разрушения белков в клетке — протеасому, и отдельно останавливали синтез новых белков. При ингибировании протеасом уровень APOL1 быстро повышался, что указывает на его обычное быстрое расщепление. Когда синтез новых белков прекращали, APOL1 быстро исчезал. В резком контрасте APOL2 почти не менялся ни при одном из этих воздействий, показывая, что он гораздо более стабильный белок. Важно, что высокая смена APOL1 была одинакова для нормальной версии (G0) и вариантов риска (G1 и G2), и это сохранялось для нескольких естественно встречающихся форм APOL1, различающихся по тому, как они ориентируются в мембранах.
Последовательностные подсказки и история двух «районов»
Изучая структуру белка, команда использовала компьютерные инструменты для поиска гибких, неструктурированных сегментов, известных как интринзиково дисордерные регионы. Такие участки часто служат «съедай меня» сигналами для протеасомы. Они выявили два сильных кандидатных региона в APOL1, которые по большей части отсутствовали в APOL2. Чтобы проверить, вносит ли уникальная передняя часть APOL1 вклад в его хрупкость, они создали гибриды: укороченную версию APOL1 без первых 59 аминокислот и химеру APOL2, несущую этот участок APOL1. Добавление N‑концевого фрагмента APOL1 к APOL2 сделало APOL2 более быстро деградирующим, в то время как усечённый APOL1 оставался нестабильным, что указывает на то, что более чем одна часть APOL1 способствует его быстрому разрушению. В совокупности эти результаты связывают необычные гибкие сегменты APOL1 с его быстрой сменой, не связывая это поведение напрямую с болезнетворными вариантами.
Упрямый белок на поверхности клетки
Самое поразительное наблюдение появилось, когда авторы разделили APOL1, находящийся внутри клетки, и APOL1 на поверхности клетки. С помощью антител, распознающих только ту часть APOL1, которая обращена наружу, они измерили уровни на поверхности отдельно от общего уровня. Внутри клетки APOL1 вел себя ожидаемо: он накапливался при блокаде протеасом и быстро исчезал при остановке синтеза. Однако поверхностный APOL1 почти не менялся ни при одном из этих воздействий. Оказалось, что достигнув плазматической мембраны, молекулы APOL1 очень устойчивы к быстрому разрушению. Более того, хотя варианты риска давали меньший общий уровень APOL1, их уровни на поверхности были схожи с нормальной версией. Это указывает на то, что варианты риска и нормальный APOL1 удаляются с сопоставимой скоростью внутри клетки, но встроенные в мембрану пула — которые, как полагают, формируют ионные каналы и вызывают токсичность — сохраняются во всех вариантах.
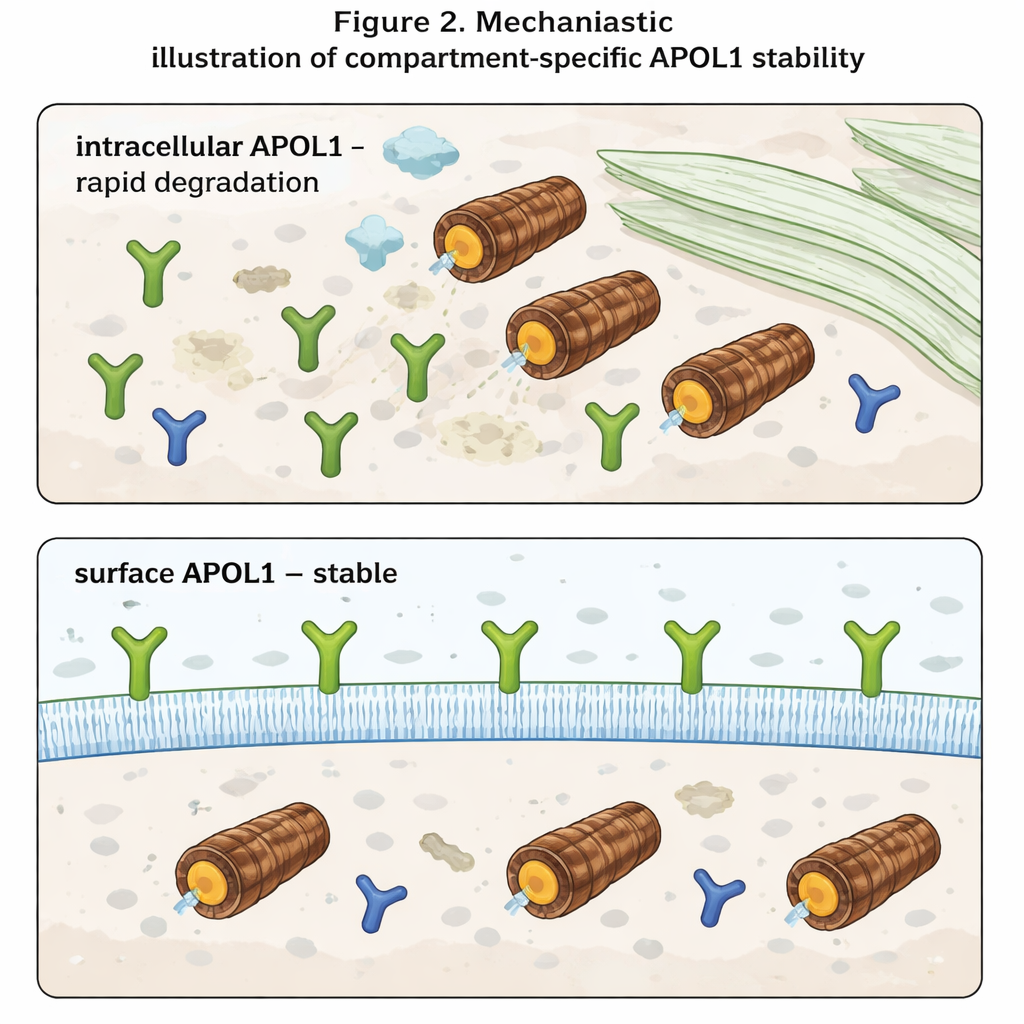
Что это значит для будущих лечений
Для неспециалистов ключевая мысль такова: поведение APOL1 сильно зависит от его локализации. Внутри клетки это короткоживущий белок, быстро распознаваемый и разрушаемый. На поверхности клетки он становится долгоживущим и относительно защищённым, даже при изменении системы разрушения клетки. Поскольку заболевание, по-видимому, возникает, когда каналы APOL1 на поверхности нарушают баланс ионов, таких как натрий и калий, терапиям, возможно, стоит сосредоточиться не столько на общем уровне APOL1, сколько на том, сколько его достигает и удерживается в плазматической мембране. Стратегии, уменьшающие транспорт APOL1 к поверхности или избирательно дестабилизирующие поверхностный пул, теоретически могли бы смягчить повреждение почек, не полностью блокируя полезные иммунные функции гена.
Цитирование: Höffken, V., Alvermann, L., Niggemeier, D. et al. APOL1 plasma membrane pools resist rapid protein degradation. Sci Rep 16, 6718 (2026). https://doi.org/10.1038/s41598-026-37647-z
Ключевые слова: APOL1, болезнь почек, разрушение белка, плазматическая мембрана, протеасома