Clear Sky Science · ru
Характеризация in vitro каталитического домена человеческой гистондеацетилазы 5
Почему маленькие переключатели в упаковке ДНК имеют значение
Внутри каждой клетки наша ДНК намотана на белки, которые действуют как шпульки, помогая уместить метры генетического материала в микроскопическое пространство. То, включен ли ген или выключен, часто зависит от небольших химических меток на этих белках-шпульках. В этом исследовании внимание сосредоточено на одном таком белковом «переключателе» — HDAC5, который связан с заболеваниями сердца, расстройствами нервной системы, раком и другими состояниями. Понимание молекулярного механизма работы HDAC5 может проложить путь к более точным лекарствам с меньшими побочными эффектами.
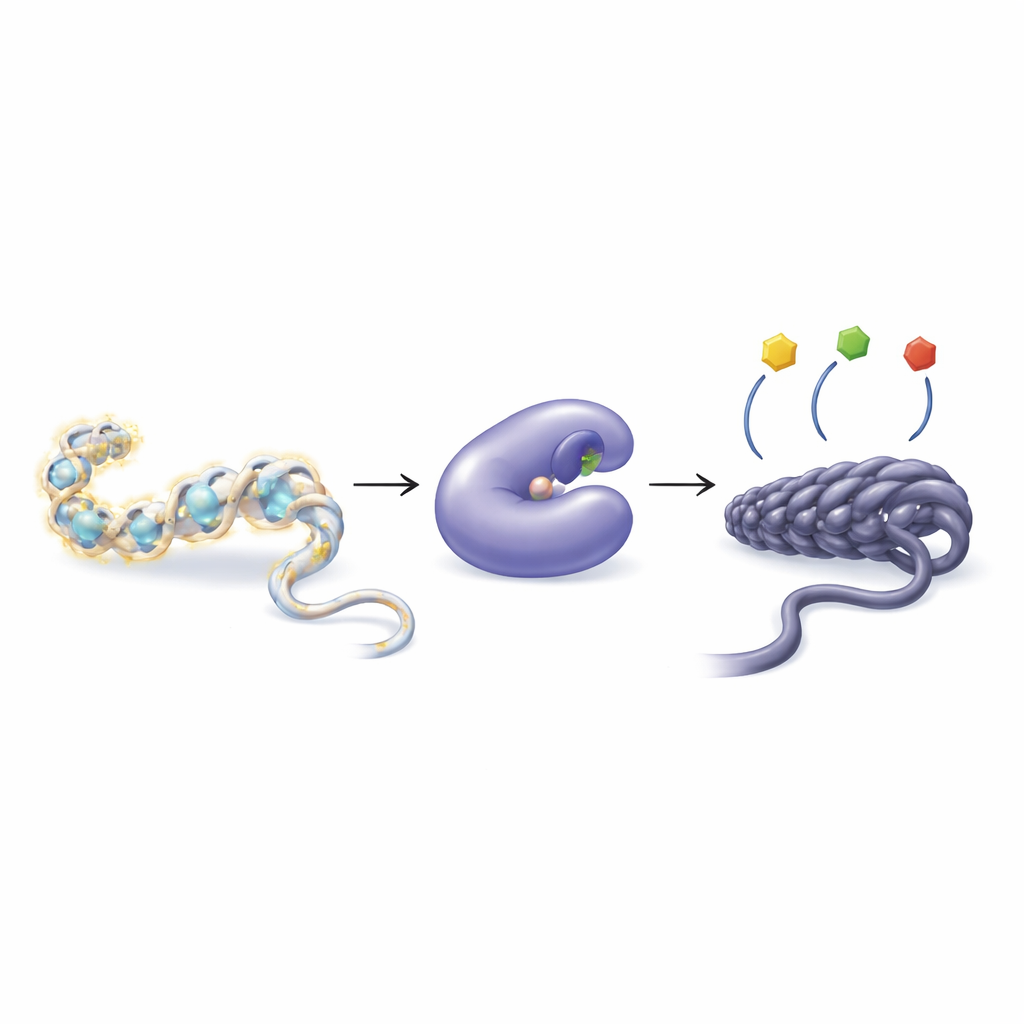
Как клетки настраивают гены с помощью крошечных химических меток
Наша ДНК не плавает свободно, она обёрнута вокруг белков, называемых гистонами, образуя структуру, известную как хроматин. Клетки могут присоединять или удалять небольшие химические группы, такие как ацетильные группы, с хвостов гистонов, чтобы сделать хроматин более рыхлым или более плотным. Более рыхлая упаковка обычно облегчает считывание генов; более плотная упаковка обычно их подавляет. За этот баланс отвечают две группы ферментов: гистон-ацетилтрансферазы добавляют ацетильные группы, а гистондеацетилазы (HDAC) их удаляют. Нарушение этого баланса может способствовать широкому спектру заболеваний, включая рак, сердечные болезни, мышечную атрофию и нарушения иммунной системы.
Почему HDAC5 обещает быть хорошей, но сложной мишенью для лекарств
HDAC представляют собой большое семейство родственных ферментов, разделённых на несколько классов. Многие лекарства, уже применяемые в клинике, блокируют сразу несколько типов HDAC, что может нарушать важные нормальные функции и вызывать серьёзные побочные эффекты. HDAC класса IIa, включая HDAC5, выделяются тем, что обогащены в определённых тканях — например в мозге, сердце и скелетных мышцах — и работают в комплексе с другими белками для регулирования ключевых генетических сетей. HDAC5 часто выполняет роль «моста», привлекая к определённым генам высокоактивный партнёрный фермент (HDAC3), чтобы уплотнить хроматин и подавить эти гены. Благодаря таким направленным функциям HDAC5 рассматривают как привлекательную мишень для более селективных препаратов, но отсутствие детальных биохимических данных и структуры его активного ядра высокого разрешения затрудняло рациональную разработку лекарств.
Сборка HDAC5 в пробирке
Чтобы устранить этот пробел, исследователи произвели только каталитическое ядро человеческой HDAC5 — ту часть, которая выполняет химическую реакцию — в бактериях, очистили его и подтвердили, что в растворе он образует стабильный одноцепочечный белок. Затем они проверили его активность при разных уровнях солёности и кислотности. Активность HDAC5 оставалась высокой в широком диапазоне солей и достигала максимума при слабощелочных условиях, сходных с условиями в многих клетках. С помощью специальных флуоресцентных тестовых молекул оказалось, что природная форма HDAC5 распознаёт только один конкретный тип субстрата, обычно используемый для исследования ферментов класса IIa. Ориентируясь на предыдущие работы по родственным HDAC, они заменили одну аминокислоту (гистидин) на тирозин в критическом месте. Поразительно, что это небольшое изменение позволило мутантной версии HDAC5 эффективно обрабатывать оба типа тестовых субстратов, показывая, как одна резидуя в активном сайте управляет химическими предпочтениями фермента.
Испытание и сравнение двух новых кандидатов в лекарства
Далее команда изучила два экспериментальных молекул-блокатора HDAC5, известные как NT160 и FFK24. Эти соединения используют новую группу, связывающую цинк, что позволяет избежать части токсичности и плохой селективности, наблюдавшихся у старых препаратов на основе гидроксаматов. Измеряя, насколько каждый ингибитор замедляет HDAC5 в точно контролируемых реакциях, авторы определили чрезвычайно низкие константы ингибирования в наномолярном диапазоне, что означает, что оба соединения прочно связываются с ферментом. NT160 стабильно связывался примерно в десять раз сильнее, чем FFK24. Чтобы понять причину, исследователи использовали молекулярное докирование с предсказанной AlphaFold структурой каталитического ядра HDAC5. Оба ингибитора имели общую головную часть, которая углублялась в активный карман и контактировала с ионом металла, но хвост NT160 формировал дополнительные стабилизирующие контакты с конкретными аминокислотами в кармане. Эти дополнительные взаимодействия, вероятно, объясняют его большую эффективность.
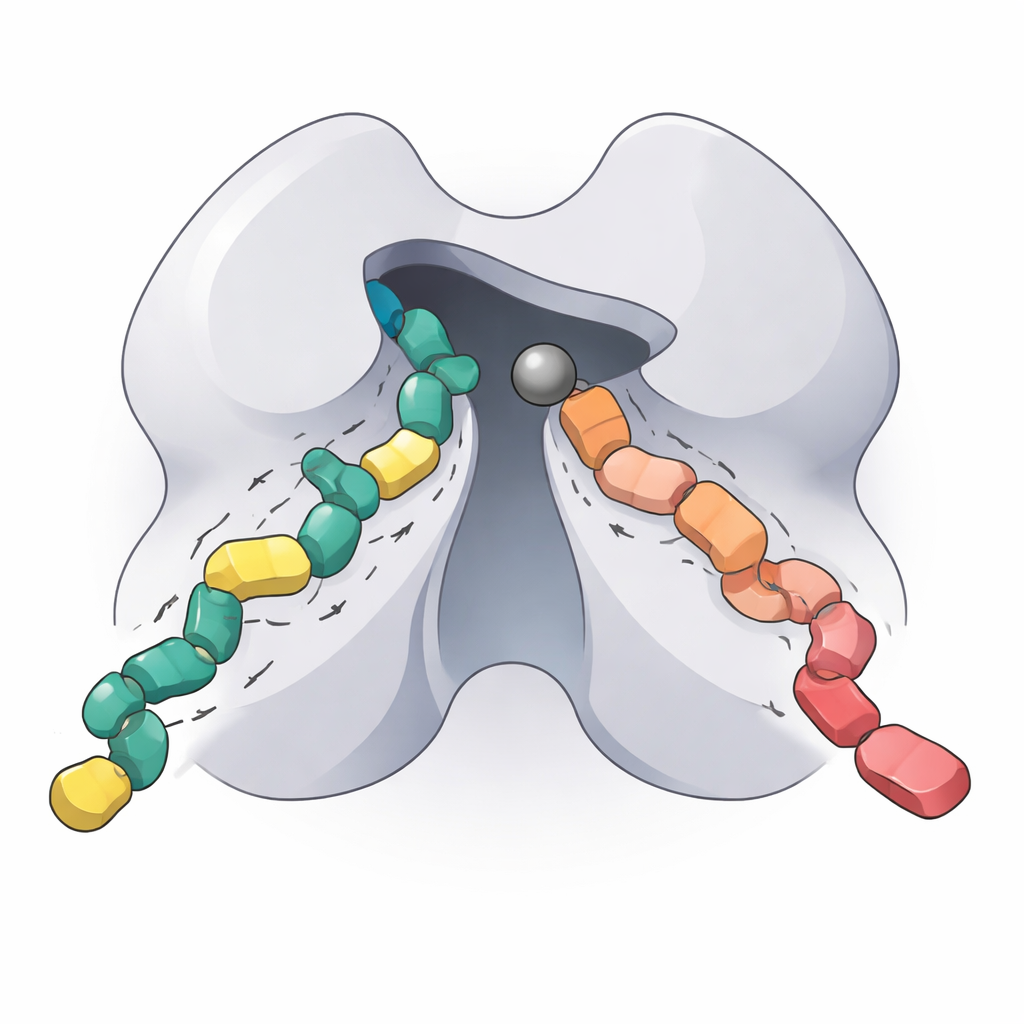
Что это означает для будущих таргетных терапий
Воссоздав рабочее ядро HDAC5, определив оптимальные условия его работы, разобравшись, как одна аминокислотная замена меняет его поведение, и количественно оценив связывание двух ингибиторов следующего поколения, это исследование предоставляет детальный биохимический «отпечаток» важного, но ранее слабо охарактеризованного фермента. Для неспециалистов главный вывод таков: HDAC5 помогает контролировать, включены ли определённые гены, и точная настройка этого переключателя может быть полезна при лечении сердечных заболеваний, нейродегенерации, рака и иммунных расстройств. Новые данные и инструменты здесь должны помочь исследователям разработать селективные для HDAC5 и класса IIa препараты, которые будут действовать там, где нужно, и минимизировать нежелательные эффекты в других тканях организма.
Цитирование: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
Ключевые слова: гистондеацетилаза 5, эпигенетическая регуляция, ингибиторы HDAC, таргетная терапия рака, структура хроматина