Clear Sky Science · ru
Модель описания взаимодействий эллагитанинов с ионами Fe(II)
Почему растительные соединения важны в корме для животных
Антибиотикоустойчивые бактерии вызывают всё большую тревогу у фермеров и специалистов по общественному здравоохранению. Многие из этих трудноизлечимых микроорганизмов появляются у животных, где антибиотики по‑прежнему широко используются в кормах. В этом исследовании рассматриваются таннины — природные соединения растений — как перспективная альтернатива. В частности, объясняется, как особая группа таннинов из каштановой древесины может захватывать железо таким образом, что это помогает «лишать голода» бактерии, лишая их жизненно важного для роста элемента.
Природные «защитники», скрытые в древесине
Таннины — горькие молекулы растительного происхождения, которые придают вину терпкость и веками использовались при дублении кожи и для производства чернил. Они широко распространены в кормах и продуктах питания и в целом безопасны для животных и человека. Некоторые типы, называемые эллагитанинами, особенно интересны, потому что у них много мелких «ручек», способных захватывать ионные металлы, такие как железо. Экстракт каштановой древесины, уже используемый в кормах, содержит несколько эллагитанинов, включая два крупных — робурин A и робурин D. Ранее показали, что более простые родственники этих соединений могут связывать железо и потенциально препятствовать доступу бактерий к этому необходимому элементу.
Лишая бактерий их любимого металла
Без железа бактерии не могут процветать: они используют его для дыхания, синтеза ДНК и множества ферментативных реакций. В кишечнике животных или в питательных средах они обычно добывают железо при помощи собственных низкомолекулярных захватывающих молекул. Эллагитаннины вмешиваются в этот процесс, формируя прочные комплексы с ионами железа и фактически «закрывая» металл для бактерий. Авторы сосредоточили внимание на железе в форме Fe(II), потому что именно эта форма быстро захватывается таннинами в воде до тех пор, пока не происходит медленное окисление до Fe(III). Выделив робурин A и D из каштанового экстракта и изучая их в строго контролируемых растворах, команда проследила, насколько эффективно эти крупные таннины удаляют железо из жидкой фазы.
Изучая, как таннины захватывают железо
Чтобы понять детали, исследователи сначала изучили, как робурины принимают и теряют протоны (процесс, называемый кислотно‑основным равновесием) при изменении pH. С помощью УФ–видимой спектроскопии они отслеживали, как меняется поглощение света робуринами на разных уровнях pH. Эти изменения показали, что робурин A и D ведут себя похоже на своих более простых родственников — вескаллагин и касталлагин — но примерно с вдвое большим числом сайтов, которые могут терять протон и затем участвовать в связывании железа. Затем они смешивали таннины с железом в различных соотношениях и снова использовали спектроскопию для построения так называемых графиков Джоба, показывающих, при каком соотношении смеси образуется максимальное количество комплекса «железо–таннин». По этим данным авторы пришли к выводу, что каждая молекула робурина может связать шесть ионов Fe(II) — вдвое больше, чем более мелкие эллагитаннины.
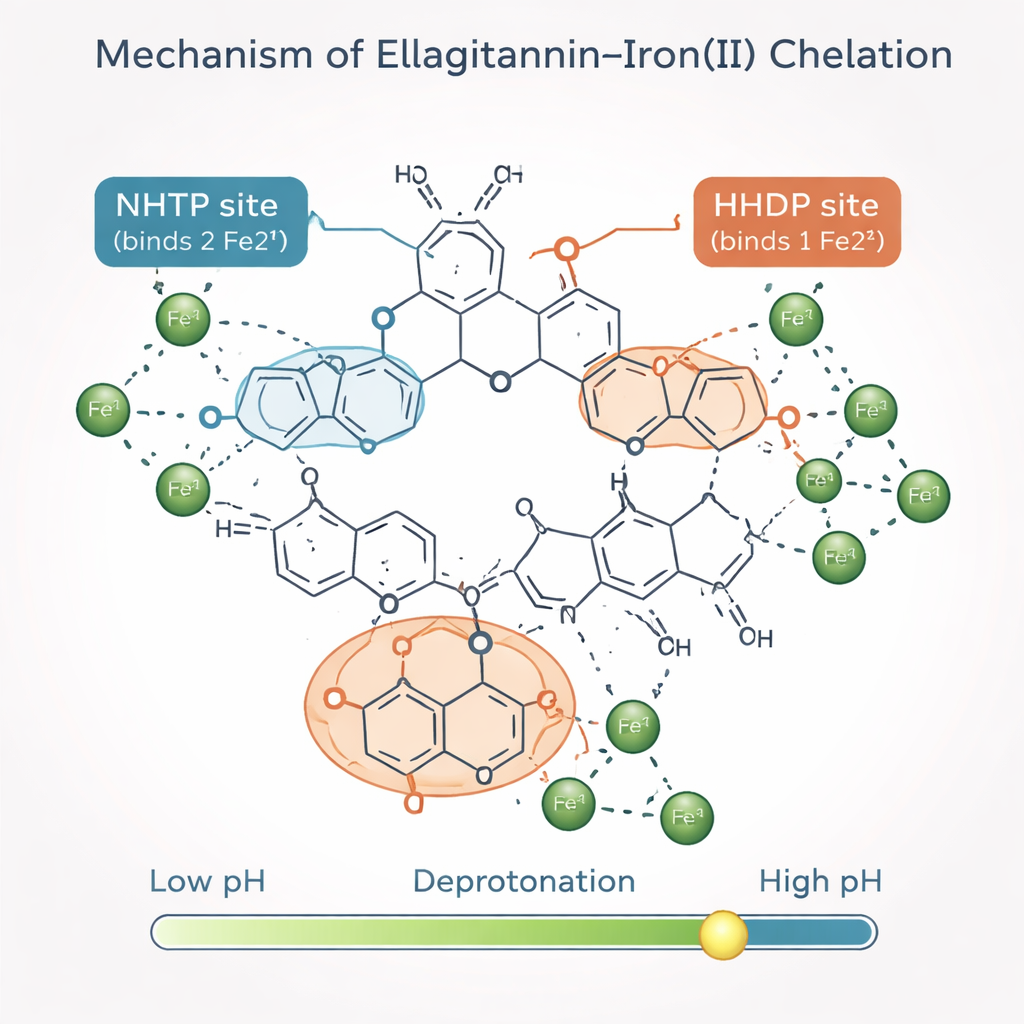
Прогностическая карта «горячих точек» связывания железа
Помимо подсчёта числа захватываемых ионов железа, авторы хотели выяснить, какие структурные «модули» эллагитанинов выполняют основную работу. Они построили математическую модель, рассматривающую каждую молекулу эллагитанина как набор повторяющихся строительных блоков. Два ключевых модуля, называемые группами NHTP и HHDP, предоставляют конкретные точки связывания для железа после того, как они потеряют свои наиболее кислые протоны. Объединив новые измерения с ранними данными ЯМР и спектроскопии, команда показала, что каждая группа NHTP обычно связывает по два иона железа, тогда как каждая группа HHDP — по одному. С помощью всего нескольких настраиваемых параметров их модель точно воспроизвела экспериментальные графики Джоба не только для более простых эллагитанинов, но и для больших робуринов, которые не использовались при обучении модели.
Последствия для более экологичного сельского хозяйства
Проще говоря, эта работа превращает сложную химию таннинов и железа в практическое руководство. Она показывает, что, подсчитав блоки NHTP и HHDP в эллагитанине, учёные могут предсказывать, сколько ионов железа конкретная молекула захватит в диапазоне слабо‑кислых условий. Поскольку экстракты каштановой древесины, богатые робуринами, захватывают больше железа, чем более мелкие таннины или простые растительные кислоты, они представляются многообещающими кандидатами для ограничения доступа вредных кишечных бактерий фермерских животных к железу. Хотя требуется дальнейшее исследование — особенно других структур таннинов и форм железа — эта модель помогает направлять разработку и выбор растительных кормовых добавок, которые могли бы сократить зависимость от традиционных антибиотиков и способствовать более устойчивому, «зелёному» животноводству.
Цитирование: Frešer, F., Hostnik, G. & Bren, U. Model for the description of interactions between ellagitannins and Fe(II) ions. Sci Rep 16, 6631 (2026). https://doi.org/10.1038/s41598-026-37616-6
Ключевые слова: эллагитанины, хелатирование железа, таннины в кормах для животных, альтернативы антибиотикам, экстракт каштановой древесины