Clear Sky Science · ru
Инактивация LIMK2 подавляет дифференцировку дермальных фибробластов и устойчивость к апоптозу, вызванные механической стимуляцией
Почему некоторые рубцы разрастаются неконтролируемо
Большинство порезов и хирургических ран оставляют после себя тонкую, ровную линию. Но у некоторых людей процесс заживления выходит из-под контроля, формируя толстые, приподнятые рубцы — гипертрофические рубцы или келоиды, которые могут зудеть, болеть и ограничивать движение. В этом исследовании изучают, почему обычные кожные клетки иногда превращаются в чрезмерно активных «строителей» рубцов, и указывают на один молекулярный переключатель, называемый LIMK2, который можно было бы подавить, чтобы не допустить чрезмерного разрастания рубцов.
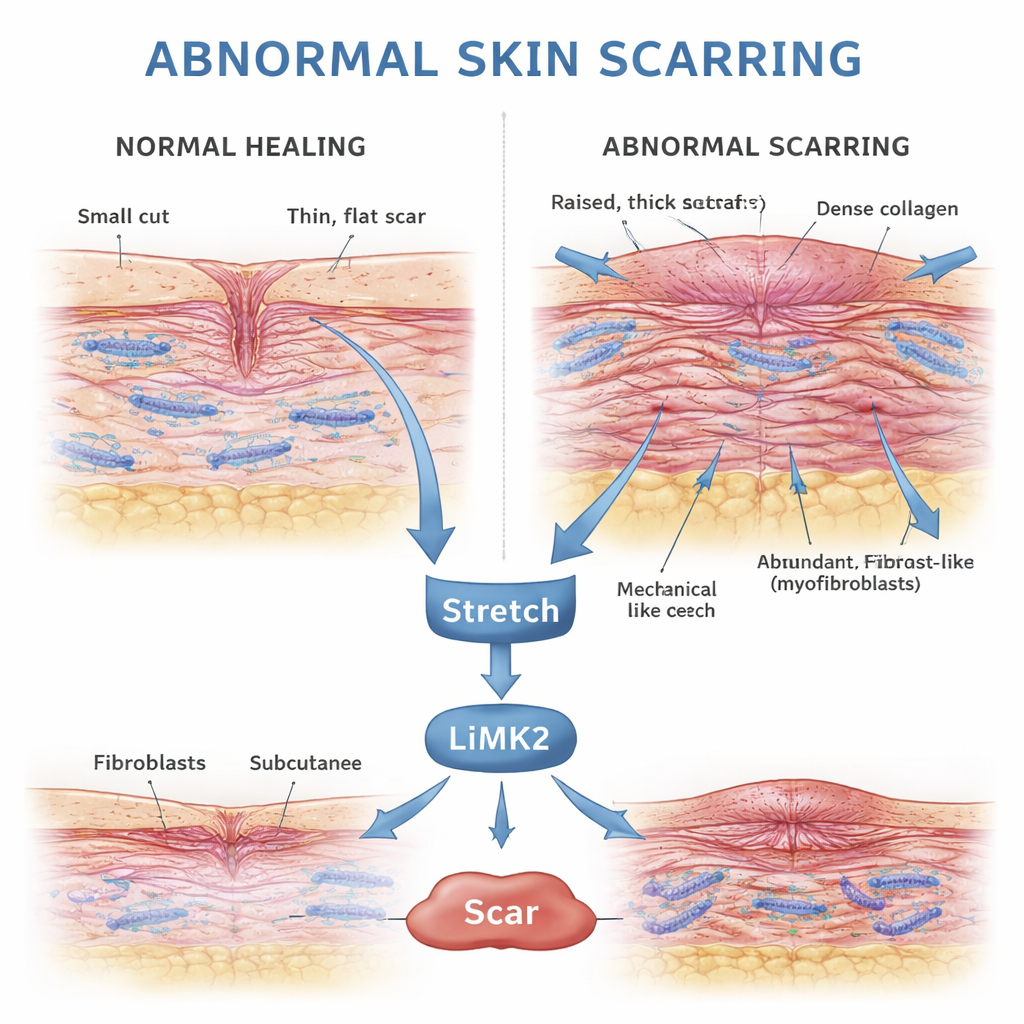
Как кожа обычно заживает после травмы
При повреждении кожи организм запускает тщательно скоординированную программу восстановления. Фибробласты — клетки-строители в глубоком слое кожи — мигрируют в рану, размножаются и откладывают коллаген, белковый каркас новой ткани. Многие из этих фибробластов временно переходят в более сильную, сократительную форму, называемую миофибробластами, которые помогают сближать края раны. После того как поверхность закрывается и новая ткань стабилизируется, эти миофибробласты должны погибнуть через контролируемый процесс, известный как апоптоз, оставляя после себя умеренный, гибкий рубец.
Как повседневные силы усугубляют рубцы
Аномальные рубцы часто появляются там, где кожа постоянно растягивается — на груди, плечах или нижней части живота. Это наблюдение привело исследователей к предположению, что механические силы, такие как натяжение и растяжение заживающей раны, могут заставлять фибробласты оставаться активными слишком долго. Ранее показали, что растяжение этих клеток в лаборатории повышает уровень белка α-SMA, маркера миофибробластов, и включает гены, помогающие клеткам сопротивляться апоптозу. Новое исследование сосредоточено на LIMK2 — ключевом звене в механическом сигнальном каскаде внутри клетки, которое связывает физическое растяжение с изменениями внутреннего каркаса из актиновых филаментов.
Ключевой переключатель для клеток, формирующих рубцы
Чтобы проверить роль LIMK2, исследователи использовали человеческие дермальные фибробласты из нормальной кожи и из келоидной ткани. В некоторые клетки вводили неактивную версию LIMK2, другие оставляли без изменений или давали постоянно активную версию в качестве контроля. При механическом растяжении нормальные фибробласты реагировали как ожидалось: быстрый рост фосфорилированного кофилина и усиление актиновых фибрилл, повышение α-SMA, усиленное производство коллагена и более высокий уровень Bcl-2 — белка, защищающего от гибели клетки, вместе со снижением уровня проапоптотического белка BAX. В поразительном контрасте фибробласты с неактивным LIMK2 почти не менялись при растяжении. Они не увеличивали α-SMA, не повышали защитный Bcl-2 и не снижали BAX, а также синтезировали меньше коллагена. Эти клетки также меньше сокращали коллагеновые гели и медленнее передвигались в имитации раны, что указывает на более слабую сократительную силу и сниженную способность вторгаться в окружающую ткань.
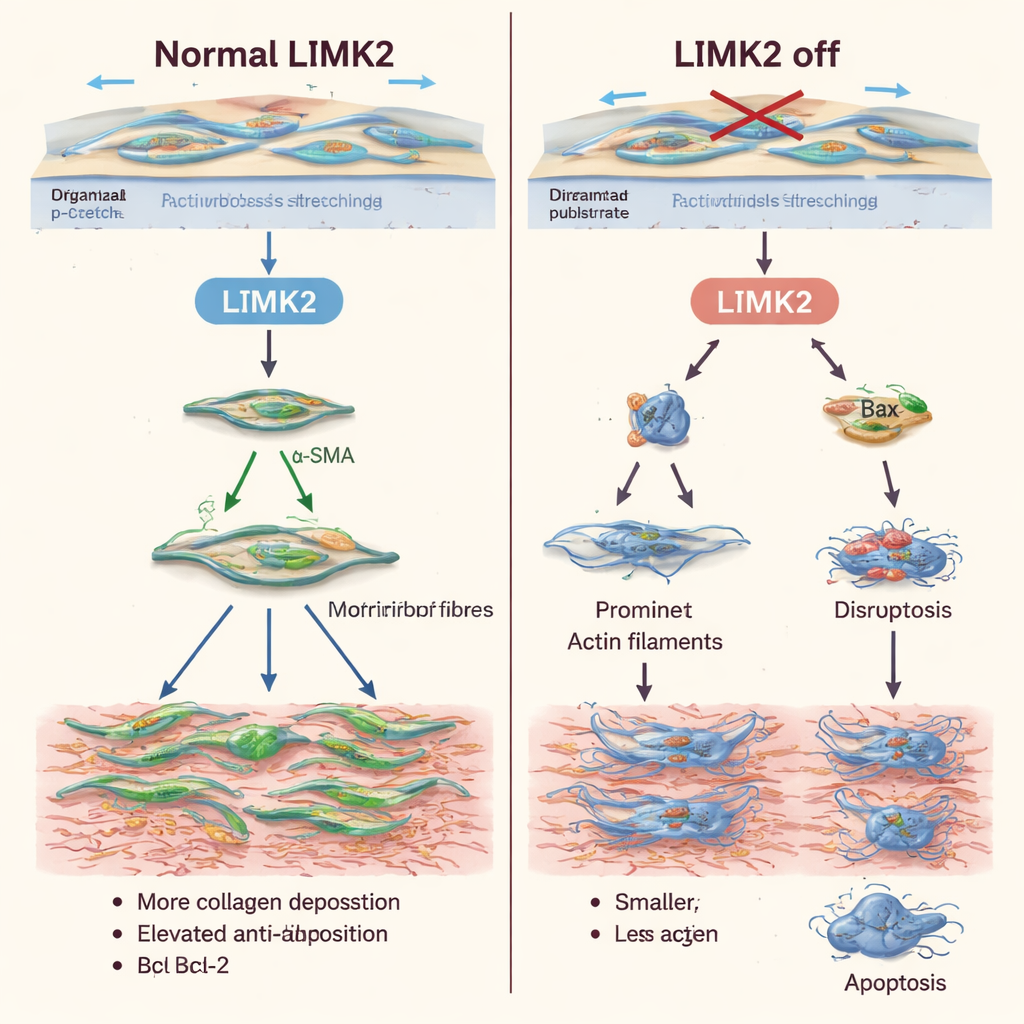
Делаем упрямые клетки рубца легче устраняемыми
Кроме изменения поведения фибробластов при растяжении, подавление LIMK2 делало их более восприимчивыми к гибели и менее склонными к делению. Клетки с неактивным LIMK2 демонстрировали более высокий базовый уровень апоптоза, и механическое растяжение — которое обычно является сигналом выживания — больше не защищало их. Проточная цитометрия и флуоресцентная окраска подтвердили, что больше клеток находилось на ранних или поздних стадиях программируемой гибели. Одновременно подсчёт клеток и тесты с метками ДНК показали, что эти клетки делились значительно реже, чем нормальные. Похожие закономерности наблюдались при использовании латрункулина A — препарата, разрушающего актиновые филаменты, — что подтверждает идею о том, что LIMK2 действует главным образом через контроль внутреннего каркаса клетки.
Что это может означать для будущих методов лечения рубцов
Результаты указывают на то, что LIMK2 находится на перекрестке, где пересекаются механические силы, выживание клеток и активность по построению рубца. Когда LIMK2 активен, растяжение направляет фибробласты в прочное, персистирующее состояние миофибробластов: они сильно сокращаются, сопротивляются гибели и вырабатывают лишний коллаген — все это способствует образованию толстых, приподнятых рубцов. Выключение LIMK2 обращает большую часть этих эффектов: фибробласты становятся менее сократительными, менее подвижными, менее плодовитыми и более склонными к апоптозу. Для пациентов это означает, что в будущем кремы, инъекции или повязки, мягко блокирующие LIMK2 или связанные с ним актиновые изменения, могли бы помочь ранам с высоким риском заживать с более плоскими и более комфортными рубцами.
Цитирование: Ishii, M., Kuroda, K., Otani, N. et al. LIMK2 inactivation suppresses mechanical stimulation-induced dermal fibroblast differentiation and resistance to apoptosis. Sci Rep 16, 7453 (2026). https://doi.org/10.1038/s41598-026-37610-y
Ключевые слова: келоидные рубцы, заживление ран, фибробласты, механическое напряжение, апоптоз