Clear Sky Science · ru
Убиквитинирование SMAD2 через мотив PY регулирует массу скелетных мышц и фибротическое перерождение
Почему это исследование мышц важно
С возрастом многие замечают, что мышцы становятся слабее и мельче, а при хронических заболеваниях или травмах мышечную ткань со временем может замещать плотный рубец. В этом исследовании решается фундаментальный вопрос, лежащий в основе таких изменений: как мышечные клетки не дают мощному сигнальному пути TGF‑beta зайти слишком далеко и вызвать потерю мышечной массы и фиброз (рубцевание)? Раскрывая крошечный встроенный «выключатель» в ключевом белке TGF‑beta, авторы демонстрируют новый механизм, который помогает сохранять мышечную массу и здоровую структуру ткани.
Встроенный тормоз для мощного сигнала
TGF‑beta — это сигнальная молекула, которая подсказывает клеткам, когда замедлить рост, сменить идентичность или начать синтез соединительной ткани. В скелетных мышцах избыточный TGF‑beta уменьшает волокна и способствует фиброзу; недостаток же может нарушить нормальный контроль роста. Внутри клеток TGF‑beta действует преимущественно через релейный белок SMAD2. После связывания TGF‑beta с рецепторами на поверхности клетки SMAD2 активируется и перемещается в ядро, изменяя активность генов. Чтобы это не стало постоянным, клетки химически помечают SMAD2 маленькими молекулами убиквитина, направляя его на удаление. Короткая последовательность в SMAD2, известная как мотив PY, служит сайтом прикрепления для ферментов, навешивающих эти убиквитиновые метки. Исследователи задали вопрос: если этот сайт удаления убрать у живого животного, даст ли сбой «тормоз» SMAD2, и что произойдет с мышцами со временем?
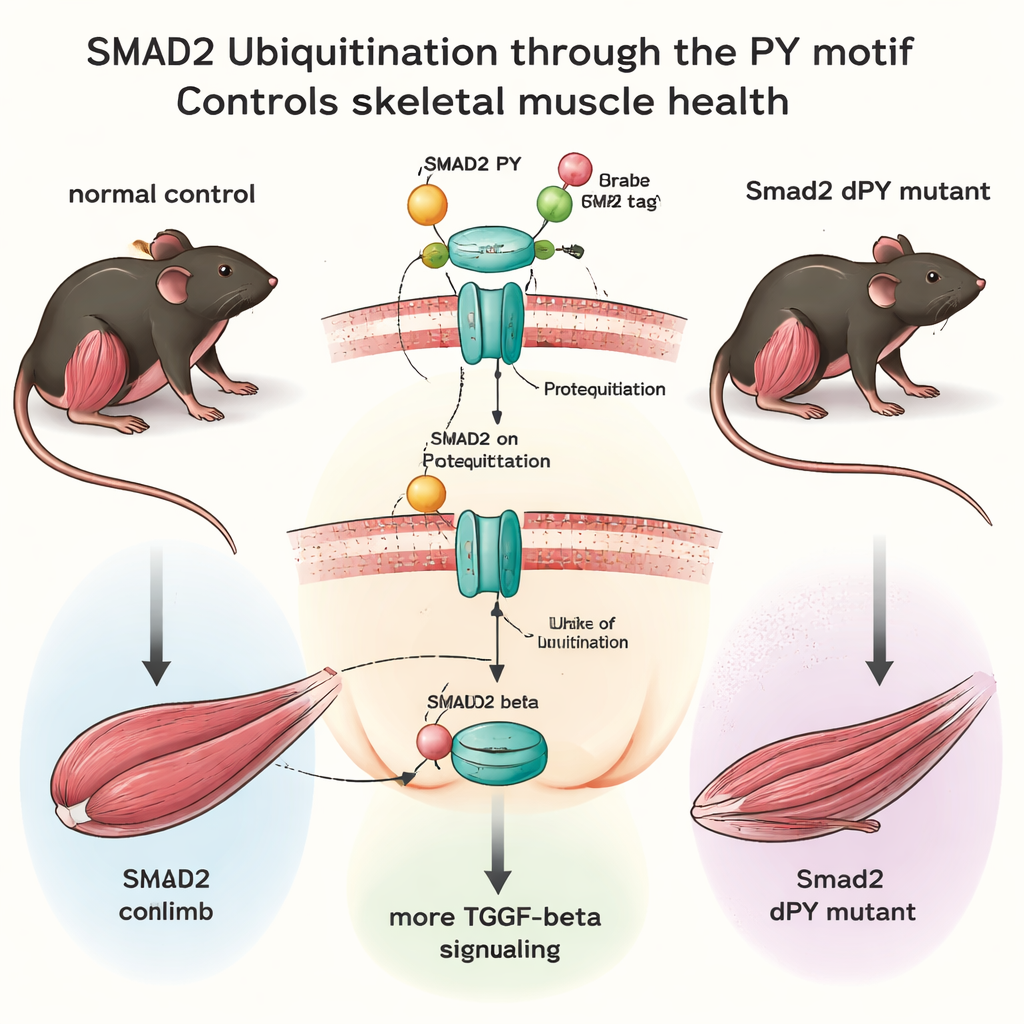
Генетические мыши без предохранительной метки
С помощью современных инструментов редактирования генома команда создала мышей, у которых было удалено всего 15 «букв» ДНК в гене Smad2, точно устранив мотив PY, не затрагивая остальную часть белка. Эти Smad2dPY‑мыши рождались нормально, выросли до взрослого возраста и были плодовиты, что показывает: эта тонкая система регулирования не необходима для базового развития в стандартных условиях лаборатории. Однако при более тщательном изучении мышц картина изменилась. У молодых взрослых мышей наблюдались лишь незначительные изменения, но к 12 месяцам — примерно в среднем возрасте для мыши — основные мышцы задних лап весили меньше, а отдельные волокна были мельче по сравнению с нормальными собратьями. Внутри этих мышц уровни белка SMAD2 были выше, тогда как его убиквитинирование снижалось, что подтверждает: удаление мотива PY сделало SMAD2 более стабильным и менее поддающимся деградации.
Чрезмерно чувствительные мышечные клетки и остановленный ремонт
Чтобы понять значение этих изменений на клеточном уровне, исследователи выделили из мутантных мышей миобласты — предшественники мышечных клеток. При обработке TGF‑beta в культуре эти миобласты демонстрировали более сильную активацию SMAD2 и более выраженную индукцию генов, ответственных на TGF‑beta, чем клетки от нормальных мышей. В то же время их способность сливаться в длинные многоядерные мышечные волокна — ключевой этап роста и регенерации мышц — была нарушена. Похожие изменения наблюдались и в фибробластах, клетках соединительной ткани между мышечными волокнами: мутантные фибробласты сильнее реагировали на TGF‑beta и чаще выражали гены, связанные с миофибробластами, образующими рубцовую ткань. В совокупности эти результаты указывают на то, что при отсутствии мотива PY как миогенные клетки, так и клетки‑поддержки становятся гиперчувствительными к TGF‑beta, сдвигая баланс в сторону более мелких волокон и большего объёма фиброзной ткани.
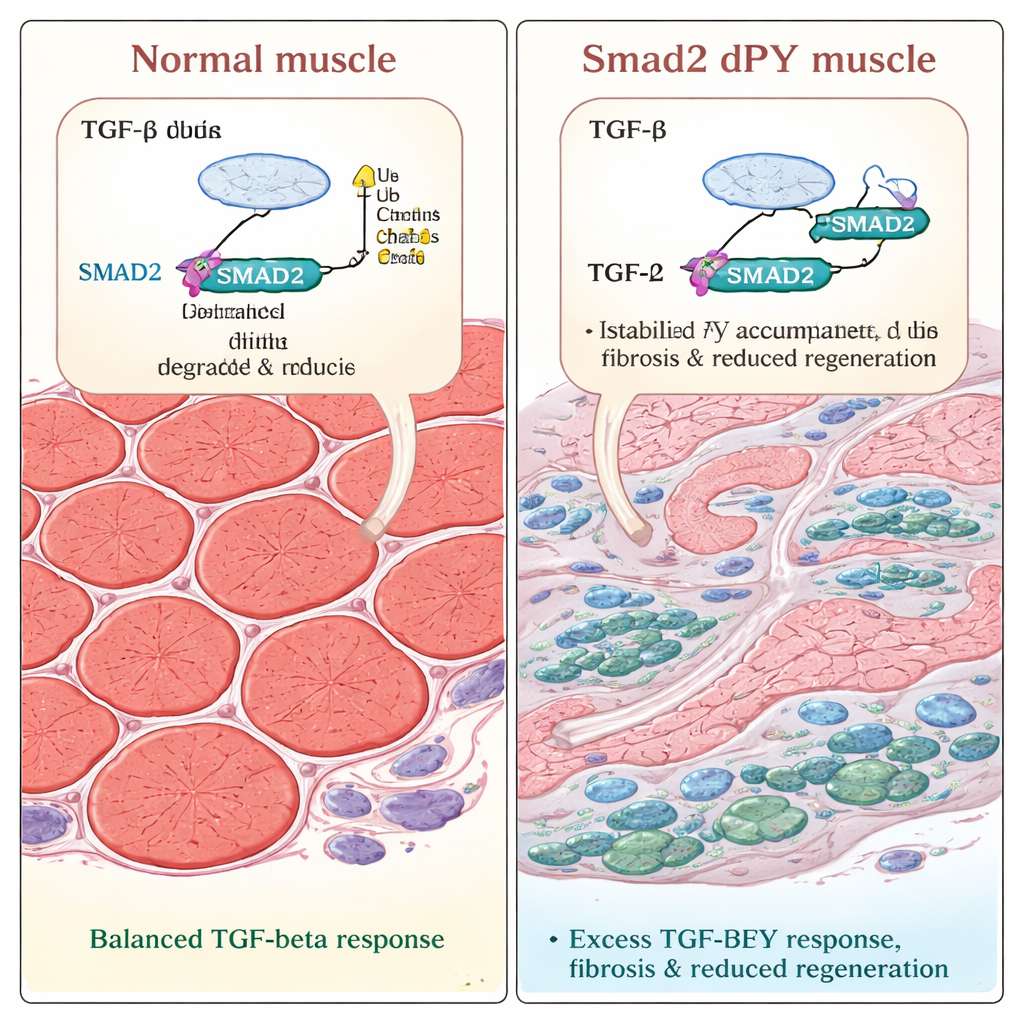
Когда наступает травма, побеждает рубцевание
Команда затем проверила, как такие изменённые мышцы справляются с повреждением. Они ввели в мышцы ноги токсин, чтобы вызвать травму и последующую регенерацию — хорошо зарекомендовавшую себя модель восстановления. И у нормальных, и у мутантных мышей повреждённые волокна сначала разрушались, а затем начинали заново расти. Но через три недели после травмы регенерировавшие волокна в Smad2dPY‑мышах были заметно тоньше. Микроскопия показала большие участки, заполненные коллагеном — основным компонентом рубцовой ткани, — а также увеличение числа миофибробластов, положительных по альфа‑гладкомышечному акту, клеток, известных как драйверы фиброза. Эти результаты демонстрируют: когда SMAD2 нельзя правильно пометить и утилизировать, процесс восстановления искажается — вместо полного восстановления прочной мышц ткань заживает с избытком рубцевания и уменьшенной сократительной массой.
Что это значит для здоровья мышц
Для неспециалистов главный вывод таков: очень небольшая молекулярная деталь — мотив PY на SMAD2 — действует как тихая, но важная защита в скелетных мышцах. Она позволяет клеткам ослаблять сигнал TGF‑beta, способствуя удалению SMAD2, поддерживая нормальный размер мышц и ограничивая фиброз, особенно когда уровни TGF‑beta естественно повышаются с возрастом или при хроническом повреждении. Когда эта защита отключена у мышей, мышцы постепенно становятся меньше и более склонными к образованию рубцов, и они не в состоянии полностью восстановиться после повреждения. Хотя работа проведена на животных, она выделяет убиквитинирование SMAD2 как потенциально перспективное звено для будущих стратегий, направленных на сохранение мышечной массы и предотвращение фибротического перерождения при старении или болезни.
Цитирование: Yamasaki, Y., Sakamoto, K., Yashiro, S. et al. SMAD2 ubiquitination through PY motif regulates skeletal muscle mass and fibrotic degeneration. Sci Rep 16, 6666 (2026). https://doi.org/10.1038/s41598-026-37582-z
Ключевые слова: скелетная мышца, сигнализация TGF-beta, SMAD2, убиквитинирование, фиброз