Clear Sky Science · ru
Изменения активности EGFR после редактирования домена связывания EGF с помощью CRISPR/Cas9
Почему важно перенастройка ракового сигнала
Рак шейки матки часто зависит от мощного переключателя роста — рецептора эпидермального фактора роста (EGFR). Во многих опухолях этих рецепторов очень много, но препараты, направленные на их подавление, помогают лишь части пациентов. В этом исследовании поставлен принципиальный вопрос с важными терапевтическими последствиями: что произойдёт, если лишить EGFR способности захватывать его любимый сигнальный фактор, эпидермальный фактор роста (EGF), не удаляя сам рецептор?
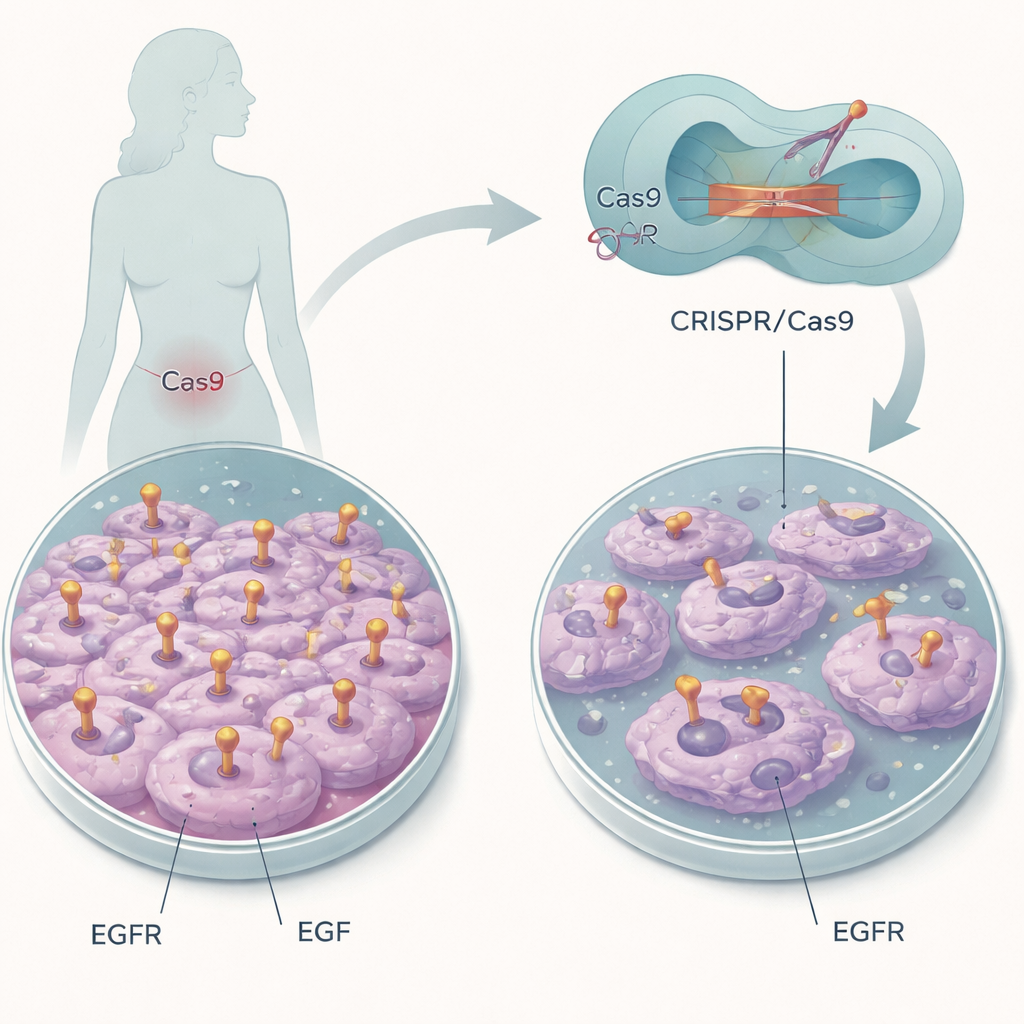
Выключение молекулярного «включателя»
Исследователи сосредоточились на клеточной линии рака шейки матки, которая экспрессирует большое количество в остальном нормального EGFR. Вместо разрушения гена они использовали CRISPR/Cas9 как молекулярный скальпель, чтобы изменить всего несколько аминокислот в кармане связывания EGF рецептора. Две конкретные позиции, обозначенные как L14 и Y45, помогают EGF «пристыковаться» к рецептору. Заменяя эти строительные блоки другими, команда стремилась сохранить присутствие EGFR, но сделать его слепым к EGF, что позволило изолировать роль именно этого взаимодействия в поведении раковых клеток.
Создание дизайнерских раковых линий клеток
На первом этапе команда протестировала эти мутации в клетках с помощью плазмид, которые временно синтезировали либо нормальный, либо модифицированный EGFR. Флуоресцентно меченый EGF показал, что все мутантные формы связывали лиганд значительно слабее, чем нормальный рецептор, особенно когда были изменены оба положения L14 и Y45 вместе. Затем исследователи ввели эти изменения непосредственно в геном раковых клеток с помощью CRISPR/Cas9, получив несколько новых клонов. Некоторые несли одну мутацию, другие — двойную мутацию на одной копии EGFR и инактивирующие изменения на другой. Компьютерное моделирование получившихся форм белка показало, что эти изменения искажают сайт связывания настолько, что ослабляют или устраняют посадку EGF, что согласуется с результатами тестов на связывание.
Когда рецептор перемещается, но клетки выживают
Детальная визуализация показала, что отредактированные рецепторы ведут себя совсем иначе внутри клетки. В неотредактированных раковых клетках EGFR располагается на поверхности мембраны, захватывает EGF, а затем внутрь клетки перемещается активированным посредством фосфорилирования. В клонах с двойной мутацией связывание EGF фактически исчезло, и EGFR больше не наблюдали на мембране; вместо этого небольшое количество оставшегося рецептора накапливалось во внутренней части клетки. Даже одна замена Y45 существенно снизила связывание и уменьшила общие уровни EGFR. Тем не менее, несмотря на такое нарушение канонического пути EGF–EGFR, раковые клетки оставались жизнеспособными и продолжали расти в культуре с лишь умеренными изменениями в цикле клеточного деления.
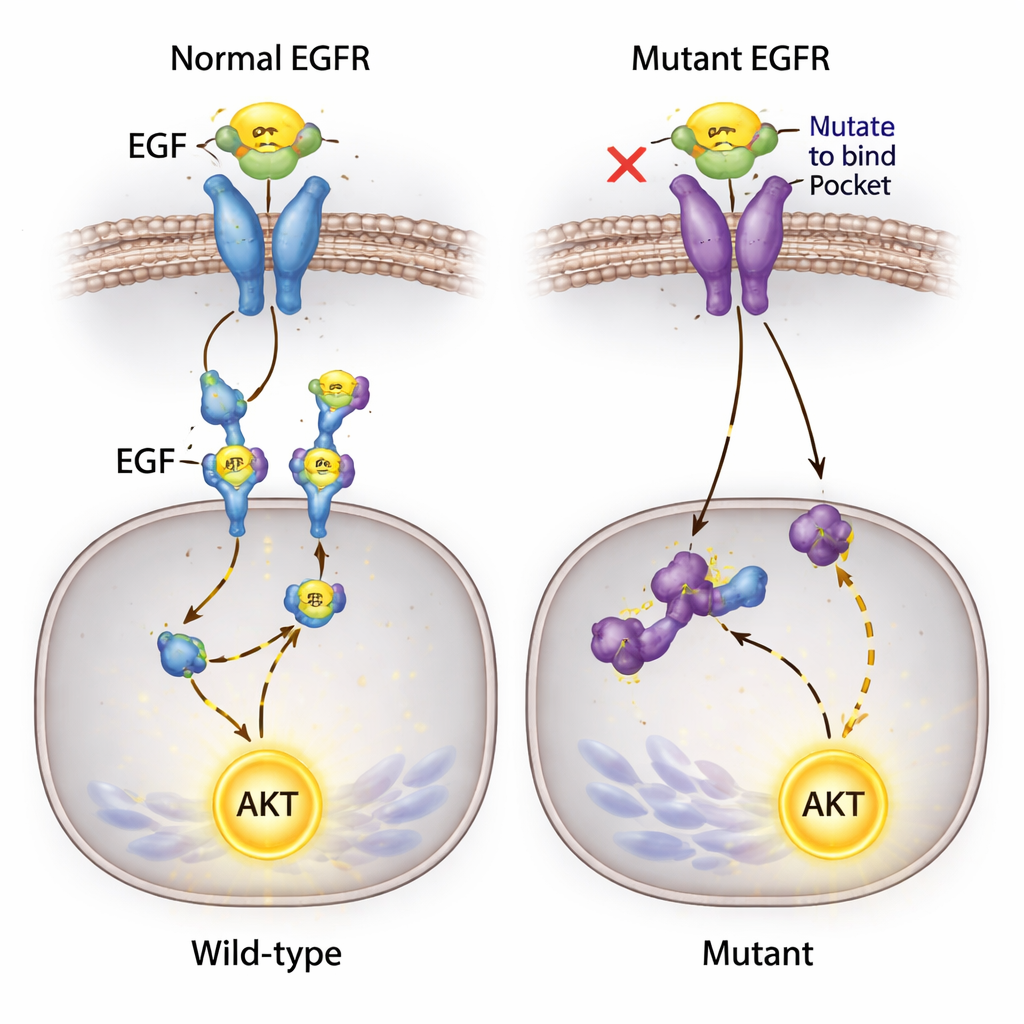
Неожиданный сигнал, который не утихает
Одно из самых удивительных наблюдений касалось AKT — ключевого белка, способствующего выживанию клеток и обычно активируемого вниз по потоку от EGFR. Исследователи ожидали, что блокирование связывания EGF с EGFR заглушит этот путь. Вместо этого, при добавлении EGF в среду, AKT сильно активировался во всех клеточных линиях — включая те, где EGF больше не мог связываться с EGFR и где фосфорилирование рецептора было не обнаружимо. Поскольку в этих клетках известна мутация в другом сигнальном гене, PIK3CA, команда предполагает, что альтернативные маршруты могут позволять EGF приводить к активации AKT, возможно через другие белки на поверхности или фоновыми мутациями, обходя отредактированный EGFR.
Скрытые генетические изменения и будущие терапии
Чтобы убедиться, что CRISPR не вызывает массовых непреднамеренных правок, учёные секвенировали полные геномы новых клеточных линий. Они подтвердили наличие целевых мутаций в EGFR и не нашли свидетельств разрезов в предсказанных оф‑таргетных участках для направляющих CRISPR. Однако были обнаружены многочисленные спонтанные мутации, разбросанные по геному, некоторые из которых могут влиять на поведение клеток. Это подчёркивает, что даже при точном попадании CRISPR нестабильная ДНК раковых клеток может осложнять интерпретацию экспериментальных результатов и разработку прецизионных генно‑ориентированных терапий.
Что это значит для пациентов
Для непрофессионала основной вывод таков: простое блокирование рукопожатия между EGF и EGFR — даже очень точно на атомарном уровне — не обязательно останавливает клетки рака от получения команд «расти и выживать». Исследование показывает, что раковые клетки могут перенаправлять ключевые сигналы, например активацию AKT, мимо заблокированного рецептора, и что само редактирование CRISPR требует тщательной оценки в условиях нестабильных геномов. Эти созданные клеточные линии теперь предоставляют мощную лабораторную модель для поиска резервных путей, поддерживающих опухоли, зависимые от EGFR, — сведения, которые в конечном счёте могут привести к комбинированным терапиям, нацеленным как на EGFR, так и на его скрытых соучастников.
Цитирование: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
Ключевые слова: EGFR, рак шейки матки, CRISPR, сигнализация EGF, путь AKT