Clear Sky Science · ru
Связывание ДНК на функционализированных пластиковых поверхностях для последовательного, итеративного секвенирования одиночных молекул
Хранение данных будущего в крошечных нитях
Представьте, что вы можете сохранять свои фотографии, книги или научные записи в форме, которая переживёт столетия и поместится в частице меньшей, чем песчинка. ДНК — та же молекула, которая несёт наши гены — становится перспективным носителем для ультроплотного и долговечного хранения данных. В этой статье изучается новый способ «парковки» цифровых данных в виде ДНК на внутренней поверхности обычных пластиковых пробирок, с возможностью многократного считывания без разрушения исходных молекул.
Новый вид «флешки»
Современные жёсткие диски и флеш-память со временем изнашиваются и по ёмкости на грамм значительно уступают потенциалу ДНК. Исследователи уже показали, как переводить цифровые файлы в последовательности «букв» ДНК. Но каждый раз при копировании или секвенировании эти фрагменты расходуются, как чернила, бледнеющие при многократном ксерокопировании страницы. В этом исследовании авторы превратили простую пластиковую ПЦР-пробирку — стандартный предмет лабораторий биологов — в многоразовое физическое хранилище. Они химически прикрепили ДНК, несущую закодированные данные, к внутренней поверхности пробирки, так что молекулы остаются на месте, пока из них многократно делают копии и считывают информацию. 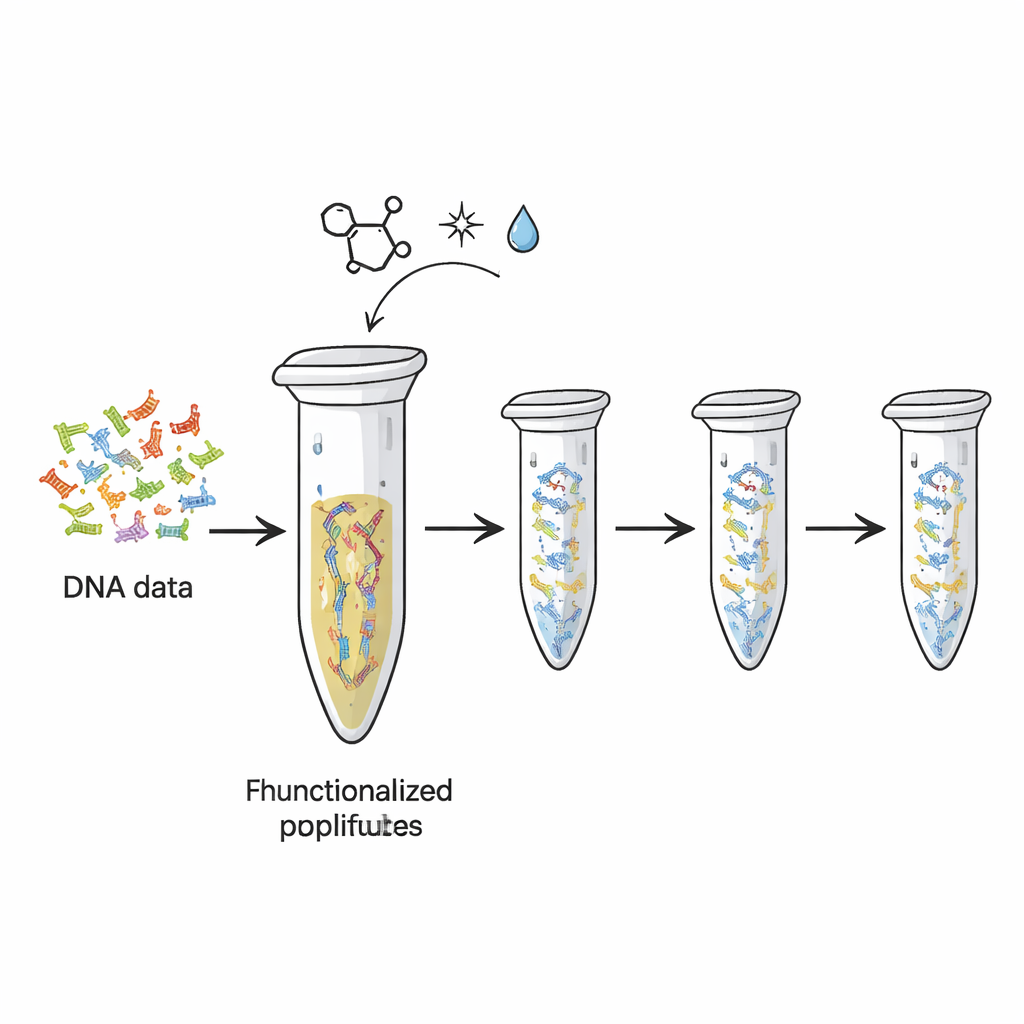
Приклеивание ДНК к пластику с помощью «клика»
Команда опиралась на тип высокоспецифичной «клик-химии» — реакции, ценимые за скорость, надёжность и мягкость. Сначала они добавили особые химические «хвосты» к концам фрагментов ДНК, представляющих разные «файлы» данных. Эти хвосты, основанные на молекуле TCO, предназначены для сцепления с подходящими группами (MTz), заранее нанесёнными на пластик пробирки. При встрече образуется стабильная ковалентная связь, фактически «склеивающая» ДНК с пластиком. Контрольные тесты с фрагментом ДНК показали, что после инкубации почти вся ДНК исчезла из раствора, что указывает на её иммобилизацию на стенке пробирки. Платформа могла удерживать порядка сотен фемтомолей ДНК, что предполагает достаточную ёмкость для практических наборов данных.
Извлечение цифровых «файлов» по требованию
Чтобы проверить, сохраняет ли связанная с поверхностью ДНК свойства рабочего архива, исследователи закодировали текст и другие данные в пуле примерно из 15 000 коротких фрагментов ДНК, сгруппированных в 18 «групп файлов». Каждую группу можно было выборочно копировать с помощью собственной пары праймеров — коротких начальных последовательностей, которые направляют механизм копирования к нужным целям. Команда многократно выполняла стандартные ПЦР-реакции в той же пробирке, каждый раз выбирая для амплификации другую группу файлов. После каждого цикла они удаляли скопированную ДНК, очищали пробирку ферментами, расщепляющими оставшиеся в растворе продукты, и переходили к следующему файлу. Нанопоровое секвенирование копий показало, что большинство групп файлов извлекались с высокой точностью, а перекрёстное загрязнение от предыдущих запусков оставалось крайне низким, обычно около 1 процента или меньше.
Поиск более бережного способа чтения
Однако был один нюанс: при повторении ПЦР в одной и той же пробирке до 18 циклов количество извлекаемой ДНК устойчиво уменьшалось. ПЦР требует быстрого нагрева и охлаждения, и авторы предположили, что многократные высокие температуры повреждают иммобилизованную ДНК или её связь с пластиком, хотя контрольные тесты показали, что ДНК просто не смывается в раствор. В качестве решения они обратились к рекомбиназно-полимеразному усилению (RPA), более новому методу, работающему при единственной, сравнительно низкой температуре, близкой к температуре тела. Используя RPA на свежих ДНК-покрытых пробирках, они вновь опросили все 18 групп файлов по очереди. На этот раз выходы были высокими — около 60 нг/мкл — и не демонстрировали нисходящей тенденции. Распределение того, какие фрагменты при копировании предпочтительны или не предпочтительны, также хорошо соответствовало наблюдаемому при свободной ДНК в растворе. 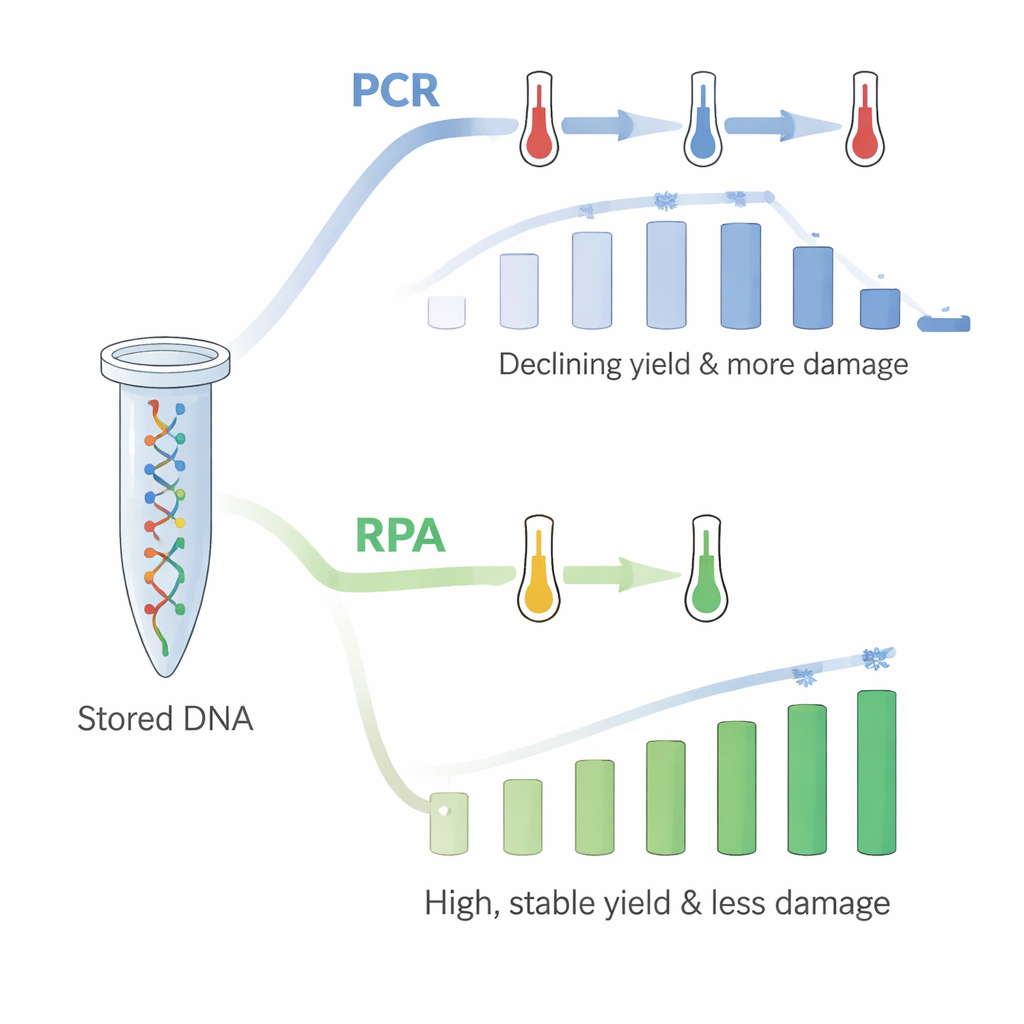
К портативной, долговечной памяти на основе ДНК
Сочетая надёжную клик-химию с низкотемпературным копированием ДНК, эта работа указывает на практический путь превращения простых пластиковых пробирок в многоразовые картриджи для хранения данных в ДНК. Молекулы физически зафиксированы на стенке пробирки, где их можно многократно опрашивать для извлечения конкретных «файлов» без расходования исходных молекул, особенно при использовании более бережного метода RPA. Для неспециалистов ключевая идея такова: ДНК — это не только код жизни, но и компактный, долговечный носитель цифровой информации. Подобные методы приближают нас к будущему, где долгосрочные резервные копии хранятся не на вращающихся дисках, а в тщательно сконструированных молекулах, тихо хранящихся на лабораторной полке.
Цитирование: Roy, S., Ji, H.P. & Lau, B.T. DNA conjugation on functionalized plastic surfaces for sequential, iterative single molecule sequencing. Sci Rep 16, 6467 (2026). https://doi.org/10.1038/s41598-026-37575-y
Ключевые слова: хранение данных в ДНК, клик-химия, сопряжение с пластиковой поверхностью, изотермическое усиление с помощью рекомбиназы и полимеразы, нанопоровое секвенирование