Clear Sky Science · ru
Амплификация числа копий стимулирует сверхэкспрессию IFI30 и координированную активацию иммунитета, выявляя новый диагностический и терапевтический мишень при аденокарциноме желудка
Почему белок в желудке важен
Рак желудка — один из самых смертоносных видов рака в мире, в основном потому, что зачастую выявляется на поздних стадиях и его трудно лечить. В этом исследовании внимание сосредоточено на малоизученном белке IFI30, который присутствует в клетках, помогающих иммунной системе распознавать угрозы. Проследив, как IFI30 изменяется в опухолях желудка и как он формирует защитные реакции организма, авторы предполагают, что он может стать мощным инструментом для ранней диагностики и для подбора более эффективных персонализированных схем лечения.
Скрытый сигнал в опухолях желудка
Команда начала с базового вопроса: различается ли уровень IFI30 в здоровой и в раковой ткани желудка? Используя крупные общедоступные наборы данных, объединяющие активность генов тысяч образцов, они обнаружили, что IFI30 стабильно значительно выше при аденокарциноме желудка — самом распространенном типе рака желудка — по сравнению с нормальной слизистой. Это подтверждалось в нескольких независимых группах пациентов и на уровнях как РНК, так и белка. При оценке способности IFI30 самостоятельно отличать опухолевую ткань от здоровой его эффективность оказалась впечатляющей: диагностическая точность (AUC) составила 0,92, что считается отличным показателем для одного маркера. Микроскопические изображения также локализовали IFI30 внутри внутриклеточной системы переработки, где антигены готовятся для распознавания иммунной системой.
Изменения ДНК, которые усиливают IFI30
Далее исследователи разобрались, почему IFI30 так повышен в этих опухолях. Сканируя геномы раковых образцов из The Cancer Genome Atlas, они обнаружили, что основной причиной его сверхэкспрессии являются дополнительные копии гена IFI30 — так называемые амплификации числа копий. Опухоли с амплификацией IFI30 обычно демонстрировали большую общую нестабильность генома и часто несли известные онкогенные мутации, такие как TP53 и PIK3CA. С ростом числа копий IFI30 повышались и уровни его РНК, что указывает на прямую связь между структурными изменениями ДНК и усиленным синтезом этого белка. Это изображает IFI30 не как пассивного наблюдателя, а как часть более широкой картины агрессивной опухолевой биологии.
Иммунный диалог вокруг опухоли
Поскольку IFI30 участвует в переработке материалов, которые иммуноциты представляют Т-клеткам как «расписки о розыске», команда исследовала, где именно он располагается в микроокружении опухоли. Секвенирование отдельных клеток, которое считывает экспрессию генов в каждой клетке, показало, что IFI30 особенно обогащен в дендритных клетках, макрофагах и CD8+ Т-клетках — ключевых участниках запуска и поддержания противоопухолевого иммунного ответа. Сетевые анализы выявили плотную коммуникацию между IFI30-обогащенными иммунными клетками и окружающими опухолевыми и стромальными клетками. В опухолях с высоким уровнем IFI30 наблюдалась сильная активация путей, связанных с презентацией антигенов, провоспалительными сигналами и молекулами, привлекающими и организующими иммунные клетки. В то же время такие опухоли демонстрировали черты инвазии и стресса, такие как ускорение клеточного цикла, перестройка ткани и адаптация к гипоксии, что подчеркивает роль IFI30 на пересечении атакующих и защитных механизмов в раке.
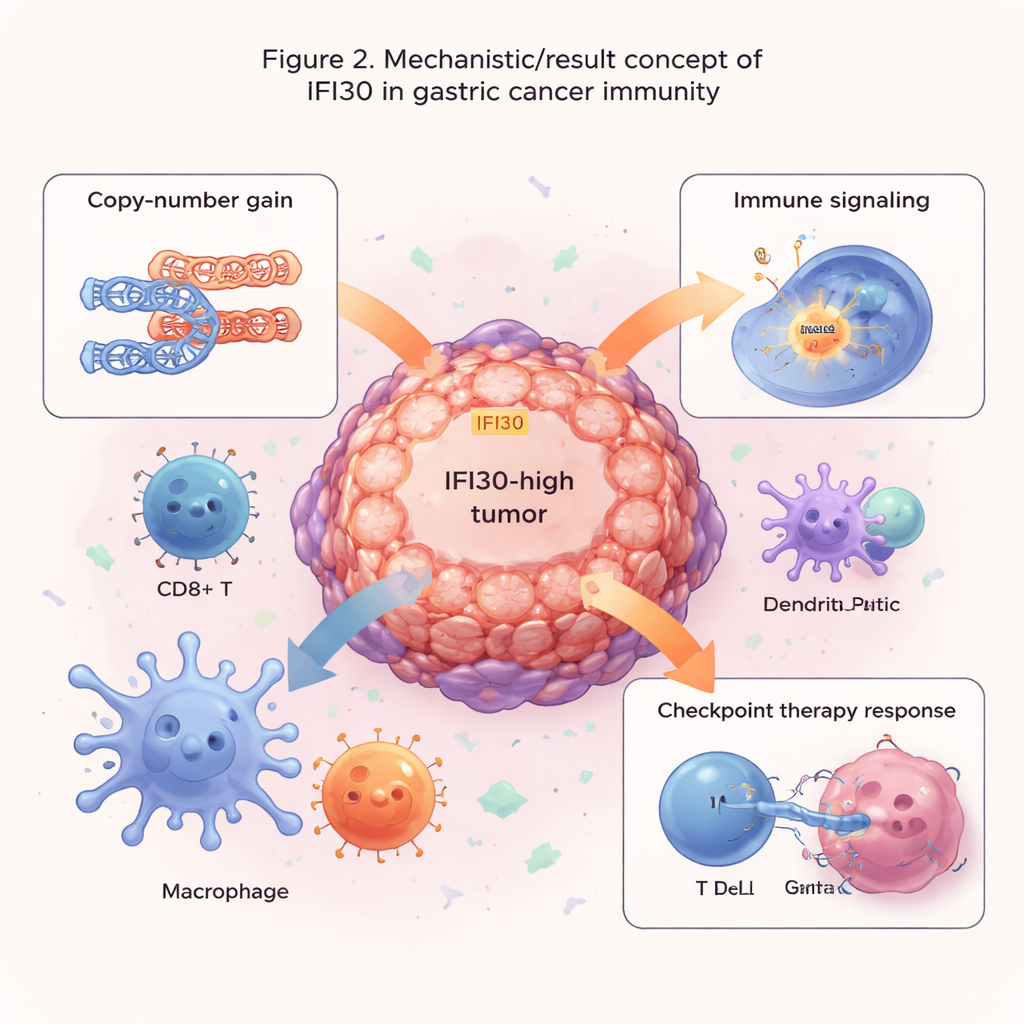
Указания для выбора лекарств и иммунотерапии
Авторы также изучили, может ли IFI30 предсказывать реакцию опухолей на лечение. Сопоставляя уровни IFI30 с крупными наборами данных по чувствительности к препаратам, они обнаружили, что опухоли с высоким IFI30 чаще устойчивы к некоторым средствам, нацеленным на деление клеток или на общий путь роста (MAPK), но кажутся более чувствительными к препаратам, блокирующим сигналы EGFR и PI3K/AKT. Примечательно, что уровни IFI30 тесно коррелировали с PD-L1 — важным тормозным сигналом для Т-клеток, на который направлены современные ингибиторы контрольных точек. В нескольких исследованиях по иммунотерапии пациенты с опухолями, характеризовавшимися высокой экспрессией IFI30, с большей вероятностью отвечали на блокаду контрольных точек, чем пациенты с низким уровнем. Балл, основанный на IFI30, превзошел устоявшиеся показатели, такие как нагрузка мутаций в опухоли и PD-L1 по отдельности, и был особенно выражен в опухолях с высокой микросателлитной нестабильностью — подгруппе, уже известной более высокой чувствительностью к иммунотерапии.
От лаборатории к потенциальной новой мишени
Чтобы проверить, является ли IFI30 лишь маркером или также способствует росту рака, команда снизила его уровень в клеточных линиях рака желудка с помощью генетических инструментов. При подавлении IFI30 раковые клетки росли медленнее, что указывает на прямую роль в поддержании пролиферации опухоли. В совокупности данные свидетельствуют о том, что IFI30 одновременно отражает активность иммунитета и вносит вклад в злокачественное поведение. Для пациентов это означает, что простой тест на IFI30 однажды может помочь врачам надежнее выявлять рак желудка, предсказывать, кто может получить пользу от определенных таргетных препаратов или иммунотерапии, и, возможно, направлять разработку новых методов лечения, которые прямо или косвенно блокируют опухоле-стимулирующие действия IFI30.
Цитирование: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
Ключевые слова: рак желудка, IFI30, биомаркер, опухолевый иммунитет, иммунотерапия