Clear Sky Science · ru
Гибридная новая структура глубокого обучения для классификации болезни Паркинсона
Почему это важно для пациентов и семей
Болезнь Паркинсона нередко начинается с тонких изменений — замедленных движений, более тихого голоса или слабого тремора — которые легко принять за обычное старение. К моменту, когда диагноз становится очевидным, значительная часть повреждений мозга уже произошла. В этом исследовании представлен компьютерный подход, который анализирует снимки мозга и с очень высокой точностью выявляет болезнь Паркинсона, даже когда признаки ещё слабо выражены. Если такие инструменты заслужат доверие и будут широко внедрены, они могли бы помочь врачам ставить диагноз раньше, начинать лечение своевременно и дать пациентам и семьям больше времени на планирование.
Заглядывая в мозг с помощью умных снимков
Исследователи сосредоточились на магнитно-резонансной томографии (МРТ) — исследовании, которое уже широко применяется в больницах и не связано с радиацией. Они использовали большую публичную коллекцию изображений мозга из инициативы Parkinson’s Progression Markers Initiative, в которую входят сканы людей с болезнью Паркинсона и здоровых добровольцев. Вместо анализа всего 3D-скана целиком команда работала с послойными изображениями мозга, особенно с участком среднего мозга, где расположены клетки, вырабатывающие дофамин. Эти клетки критичны для плавности движений, и их утрата является ключевой чертой болезни Паркинсона. Чтобы сделать слабые структуры более заметными для компьютера, изображения сначала подвергались тщательной настройке, которая стандартизирует яркость и усиливает контраст в ключевых областях.
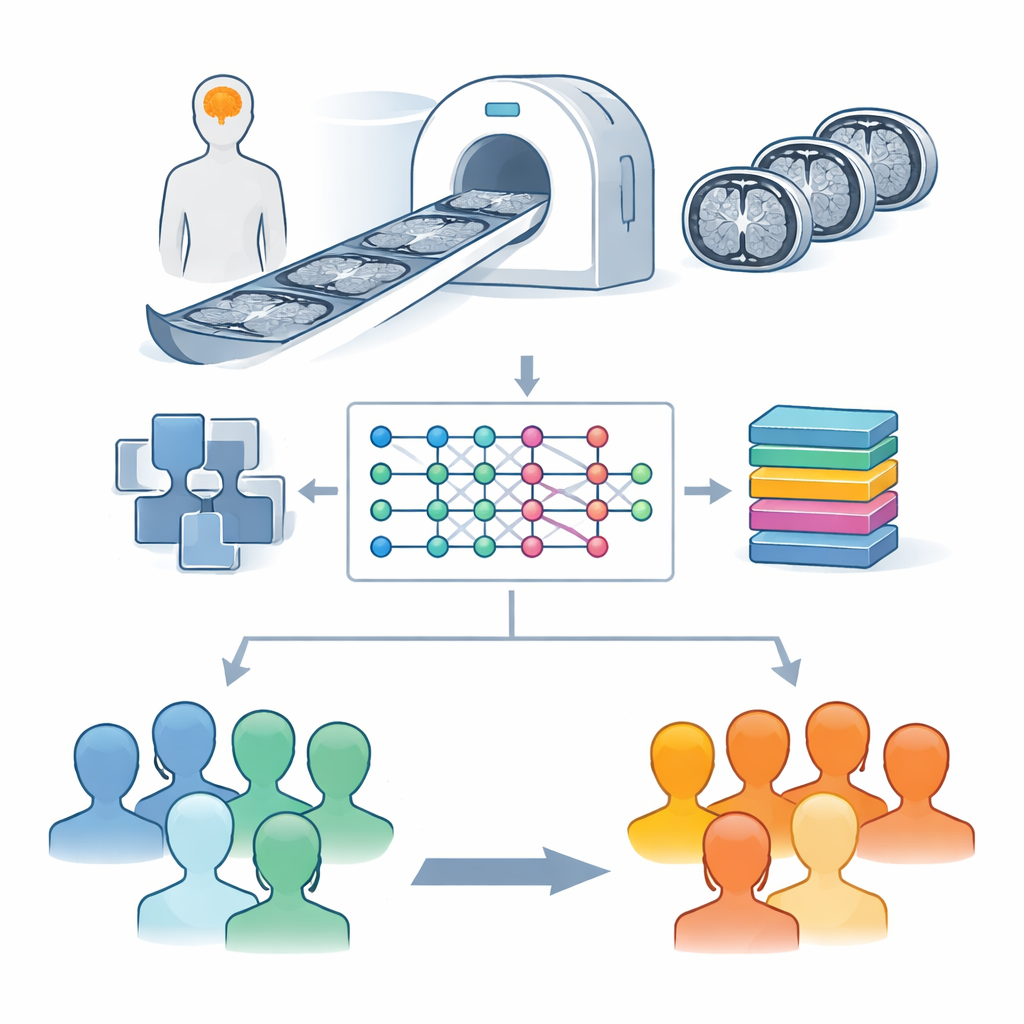
Обучение гибридной модели распознавать паттерны
В центре исследования — гибридная система, объединяющая две мощные идеи современной вычислительной науки. Первая — это сеть глубокого обучения EfficientNetB0, изначально разработанная для задач распознавания изображений. Здесь она выполняет роль натренированного глаза, просматривающего каждый срез мозга и извлекающего тонкие шаблоны формы и текстуры, которые могут отличать здоровый мозг от поражённого болезнью Паркинсона. Вторая — метод принятия решений XGBoost, который хорошо справляется с проведением чётких границ между классами, когда ему даны информативные признаки. Проще говоря, EfficientNetB0 сводит каждый МРТ-срез к компактной «подписи», а XGBoost использует эти подписи, чтобы решить, принадлежит ли снимок здоровому человеку или пациенту с болезнью Паркинсона, а также к какому типу МРТ относится изображение.
Балансировка ограниченных и несбалансированных данных
Одна из крупнейших практических проблем в медицинском ИИ — данные часто бывают скудными и несбалансированными: может быть намного больше снимков больных, чем здоровых, или наоборот. В этом исследовании команда начала со 77 сканов здоровых и 223 сканов пациентов с Паркинсоном — скромного объёма для глубокого обучения. Чтобы не обучить систему односторонним выводам, они расширили набор изображений контролируемым образом. Каждый оригинальный срез мозга поворачивали или отражали, чтобы имитировать небольшие различия в положении головы, которые встречаются при реальных сканированиях. Также применили метод усиления контраста CLAHE, который подчёркивает мелкие детали, не усиливая шум. Такое осторожное «растягивание» набора данных дало более 26 000 изображений, обеспечив модели достаточное разнообразие для обучения устойчивым признакам и снизив риск переобучения на особенностях исходных сканов.
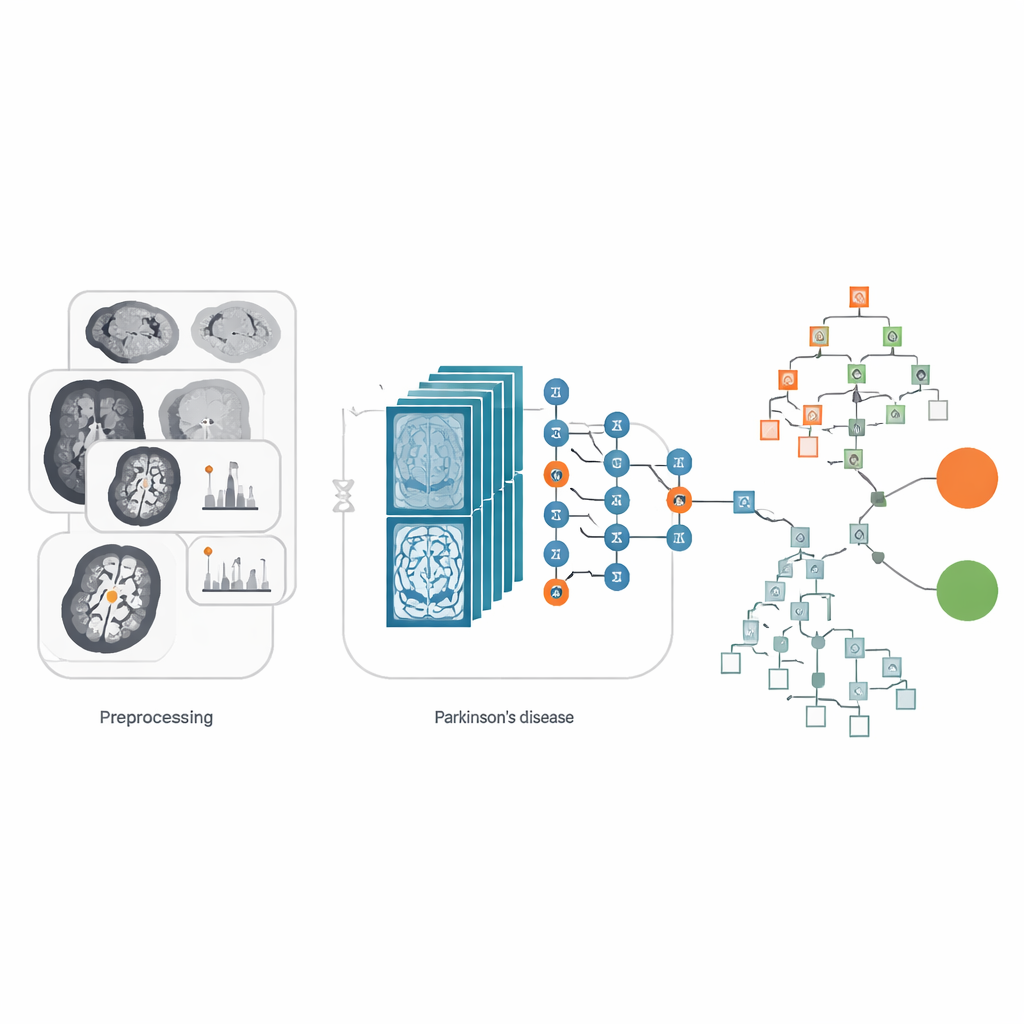
Насколько хорошо работает система?
Для оценки надёжности исследователи сравнили несколько вариантов своего подхода. Они протестировали три распространённые сети для изображений — VGG16, ResNet50 и EfficientNetB0 — в трёх режимах: «как есть», с дообучением и в сочетании со стадией принятия решений XGBoost. Во всех вариантах гибридные конфигурации показывали лучшие результаты. Победившая комбинация EfficientNetB0 плюс XGBoost правильно классифицировала сканы в 99,02% случаев на тестовом наборе. Она успешно справлялась со всеми четырьмя категориями: здоровые и с болезнью Паркинсона, каждая с использованием и без использования особой настройки МРТ, известной как FLAIR. Показатели, ориентированные на пропущенные случаи и ложные срабатывания, такие как полнота и F1‑мера, также были очень высоки, что говорит о том, что инструмент не просто жертвует одним типом ошибок ради другого. Важно, что модель оставалась эффективной по времени вычислений, что делает её более реалистичной для применения в загруженных клинических условиях.
Что это может значить для клиники
Хотя никакая компьютерная система не может заменить опытного невролога, эта работа показывает, что тщательно спроектированная гибридная модель может выступать мощным помощником. Быстро анализируя рутинные МРТ-изображения на предмет тонких признаков болезни Паркинсона, такие инструменты могли бы отмечать пациентов с повышенным риском для более тщательного наблюдения задолго до появления явных симптомов. Авторы отмечают, что их подход ещё необходимо проверить на более крупных и разнородных группах пациентов и в конечном счёте сочетать с другой информацией, такой как тесты движений или маркеры в крови. Тем не менее полученные результаты указывают, что умное программное обеспечение на базе уже имеющихся клинических снимков может стать быстрым, недорогим и легко внедряемым помощником в раннем выявлении болезни Паркинсона.
Цитирование: Desai, S., Vora, M., Shah, S. et al. Hybrid deep learning novel framework for classification of parkinson’s disease. Sci Rep 16, 9143 (2026). https://doi.org/10.1038/s41598-026-37553-4
Ключевые слова: Болезнь Паркинсона, МРТ головного мозга, глубокое обучение, медицинская визуализация, ранняя диагностика