Clear Sky Science · ru
Подход со сплит‑биотиновым лигазом выявляет белки, ассоциированные с олигомерным альфа‑синуклеином во время агрегации
Почему скомплексованные белки мозга важны
При болезни Паркинсона и родственных состояниях обычно полезный белок мозга альфа‑синуклеин может собираться в липкие отложения, известные как тельца Леви. Эти отложения появляются задолго до появления симптомов и являются характерной находкой при патологоанатомии, однако мы до сих пор не знаем, какие другие белки способствуют переходу альфа‑синуклеина из безвредного состояния в опасные агрегаты. В этом исследовании использован хитрый молекулярный «меточный» механизм близости, который позволяет картировать белки, находящиеся рядом с альфа‑синуклеином по мере его перехода от одиночных молекул к небольшим сгусткам, что даёт новые подсказки о том, как начинается заболевание и какие пути можно нацелить, чтобы замедлить или предотвратить его.
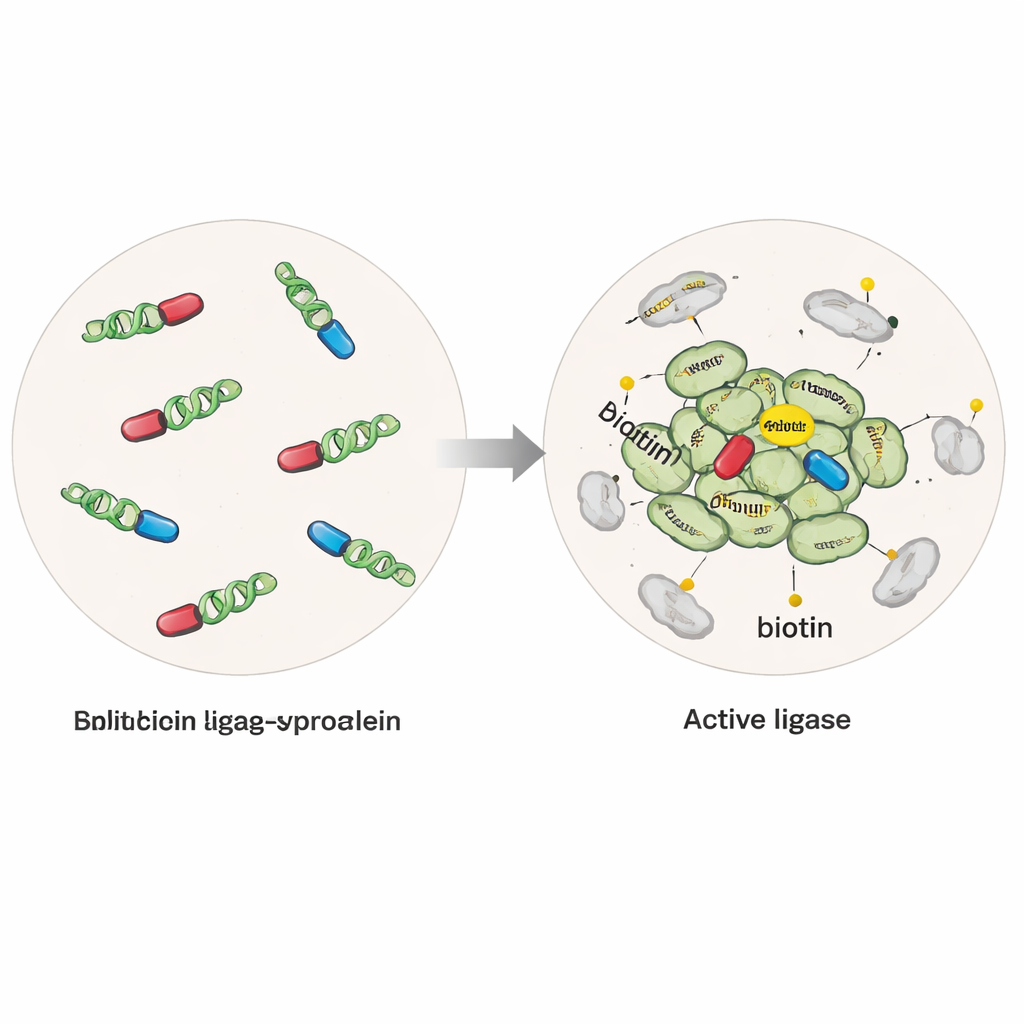
Молекулярный «ярлык», который подсвечивает соседей
Исследователи генетически модифицировали человеческие клетки так, чтобы они вырабатывали альфа‑синуклеин, слитый с модифицированным ферментом, который может прикреплять небольшой биотиновый ярлык к любому белку в радиусе нескольких миллиардных долей метра. В одной версии фермент был целым и активным всякий раз, когда присутствовал альфа‑синуклеин, захватывая белки рядом как с одиночными молекулами, так и с сгустками. Во второй, более селективной «сплит»‑версии фермент был разрезан на две неактивные половины, каждая из которых прикреплена к отдельной молекуле альфа‑синуклеина. Только когда молекулы альфа‑синуклеина собирались вместе в мультимеры или олигомеры, половинки воссоединялись в активный фермент, включая метку специально вокруг этих ранних агрегатов. Добавляя очищенные фибриллы альфа‑синуклеина в клетки, команда также могла индуцировать агрегацию, подобную заболеванию, и сравнивать нормальное и патологическое состояния.
Построение карты соседних белков
После периода маркировки команда извлекла все биотинированные белки и идентифицировала их с помощью масс‑спектрометрии — техники, которая с высокой точностью взвешивает и учитывает белки. Во всех условиях они обнаружили 1277 различных белков, а после тщательной фильтрации сузили список до 581 белка, которые с высокой вероятностью действительно находились вблизи альфа‑синуклеина. Сравнивая системы с целым и сплит‑ферментом, они смогли различить белки, которые в основном ассоциируют с одиночными молекулами, и те, что предпочитают мультимеры. Также сравнивали клетки с добавленными фибриллами и без них, чтобы увидеть, как меняется локальная белковая среда альфа‑синуклеина после запуска агрегации.
Ключевые клеточные пути, втянутые в сгустки
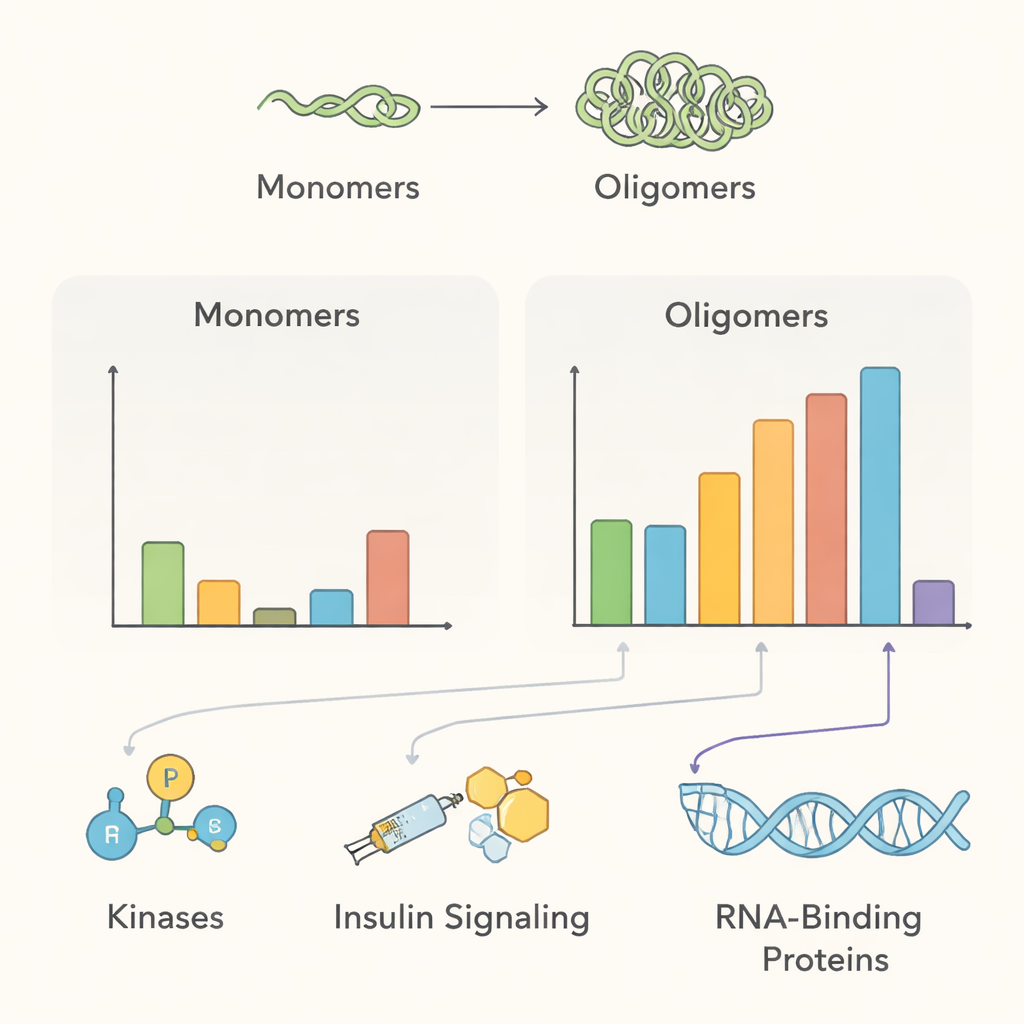
Полученная схема взаимодействий указывает на несколько важных биологических тем. В нормальных условиях мультимерный альфа‑синуклеин находился вблизи многих белков мембранного трафика и ферментов, модифицирующих белки — что согласуется с его предлагаемой ролью в помощи нейронам управлять синаптическими везикулами и поддерживать качество белков. Несколько ферментов, добавляющих фосфатные группы, включая киназы PAK4, RIPK2 и MAP4K4, были обогащены возле здоровых мультимеров, но, по‑видимому, теряли контакт после образования агрегатов, что указывает на то, что нарушение этих связей может способствовать образованию патогенных форм белка. Команда также обнаружила белки, связанные с сигналингом инсулиноподобного фактора роста, подтверждая клинические связи между инсулинорезистентностью и болезнью Паркинсона, и выяснила, что агрегация привлекает белки, участвующие утилизации повреждённых белков, такие как шапероны семейства 14‑3‑3 и определённые компоненты путей клеточной деградации.
Неожиданные мосты к другим заболеваниям мозга
За пределами болезни Паркинсона данные подчёркивают удивительную связь с боковым амиотрофическим склерозом (БАС) и лобно‑височной деменцией (ЛВД). РНК‑связывающий белок FUS, который смещается и агрегирует при этих состояниях, обнаруживался рядом с мультимерным альфа‑синуклеином как в нормальных, так и в индуцированных состояниях агрегации. Другие РНК‑связанные белки также меняли свою близость по мере агрегации альфа‑синуклеина. Эти наблюдения позволяют предположить, что небольшие сборки альфа‑синуклеина могут захватывать белки, работающие с РНК, в неправильные участки клетки, потенциально связывая биологию болезней с тельцами Леви и патологией БАС/ЛВД, хотя прямые физические взаимодействия ещё предстоит подтвердить.
Что это значит для понимания болезни
Для неспециалистов главный вывод состоит в том, что эта работа даёт раннюю «карту контактов» белков, которые сопровождают альфа‑синуклеин при переходе от нормальной вспомогательной функции к вредоносному сгустку. Исследование указывает на то, что утрата некоторых защитных связей — например с определёнными киназами или ферментами контроля качества — может быть столь же важна, как и приобретение новых токсичных партнёров. Хотя эксперименты проводились в упрощённой клеточной модели и пока не доказывают причинно‑следственной связи, они выделяют конкретные кандидаты и пути для дальнейшей проверки в нейронах и тканях мозга. В долгосрочной перспективе картирование этих меняющихся белковых соседств может направлять стратегии по восстановлению защитных взаимодействий, поддержке инсулин‑связанных сигналов или предотвращению захвата РНК‑связывающих белков, что потенциально замедлит путь от тонких молекулярных изменений до полного развития болезней с тельцами Леви.
Цитирование: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
Ключевые слова: альфа‑синуклеин, болезнь тел Леви, агрегация белков, проксимальная протеомика, болезнь Паркинсона