Clear Sky Science · ru
Клинически применимая и обобщаемая модель глубокого обучения для передних средостенных опухолей на КТ-изображениях в нескольких учреждениях
Почему важно выявлять редкие опухоли грудной клетки
Большинство из нас никогда не услышат в клинике фразу «передняя средостенная опухоль», потому что эти образования — часто затрагивающие тимусную железу перед сердцем — редки. Тем не менее, когда они появляются, их трудно распознать и ещё труднее точно измерить на КТ-снимках; эти задачи обычно требуют специалистов в крупных онкоцентрах. В этом исследовании проверяли, сможет ли тщательно обученная система искусственного интеллекта (ИИ) помочь врачам в разных больницах надёжно находить и очерчивать такие трудноуловимые опухоли на рутинных КТ-изображениях, что потенциально улучшит диагностику и планирование лечения для пациентов, которые иначе могли бы быть пропущены.
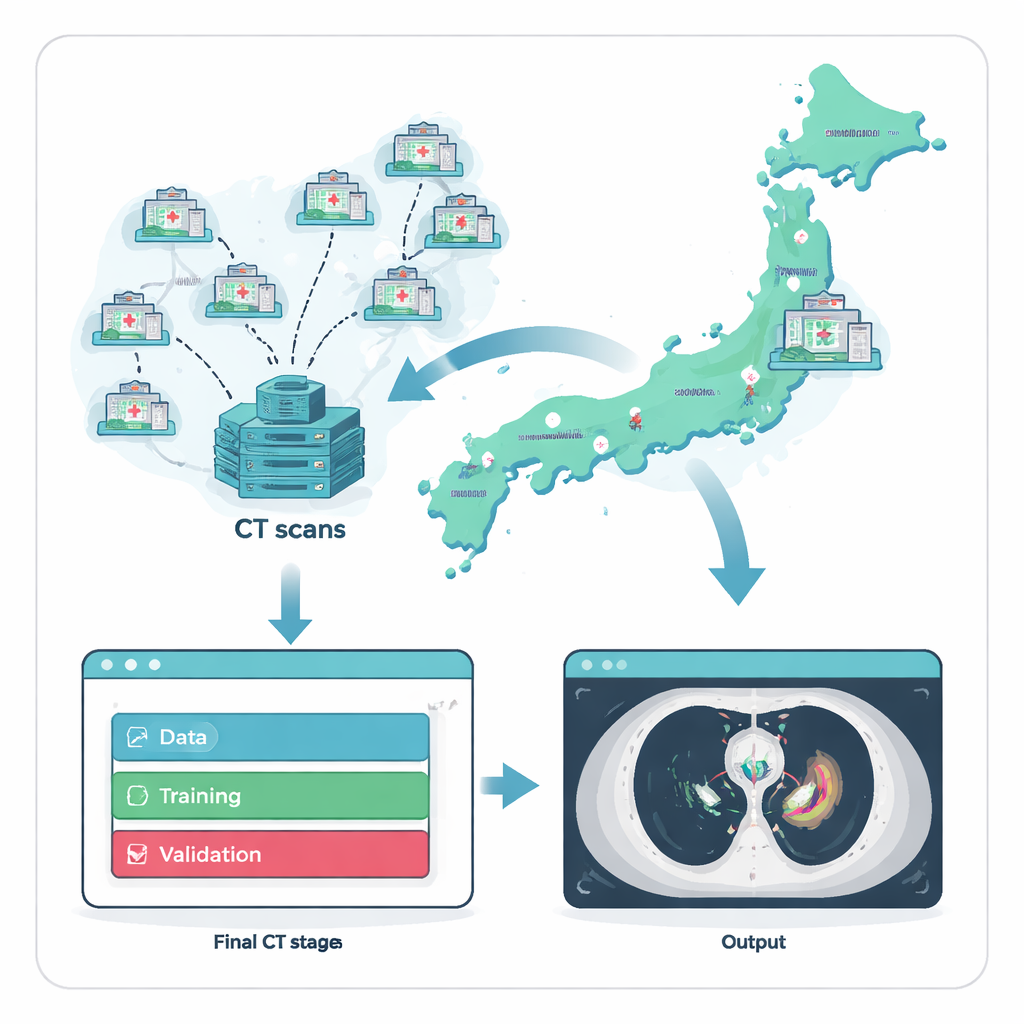
Сбор редких случаев по всей стране
Поскольку передние средостенные опухоли встречаются редко, первой задачей было просто найти достаточное число примеров для обучения ИИ. Исследователи решили эту проблему, сотрудничая с Национальным онкологическим центром Японии и 135 направляющими больницами по всей стране. В течение двух десятилетий они собрали 711 грудных КТ, каждый — от разного взрослого пациента с гистологически верифицированным диагнозом. Чтобы обеспечить честную и реалистичную проверку, данные разделили на три группы: большую для обучения, меньшую для дообучения и полностью отдельный внешний тестовый набор из 164 сканов, полученных в 121 больнице, которые не вносили изображения в обучающую выборку. Такое строгое разделение имитирует поведение системы при внедрении в новые больницы, которых она «не видела» ранее.
Преобразование снимков в надёжные учебные примеры
Модель ИИ хороша ровно настолько, насколько хороши примеры, на которых она учится, поэтому команда вложила значительные усилия в экспертную разметку. Для каждого КТ-скана специалисты обводили точные границы опухолей в передней части грудной клетки. Изначальные контуры рисовал торакальный хирург или рентген-лаборант, после чего их проверяли два опытных диагностических радиолога. Все разногласия обсуждали и разрешали, создавая высококачественную эталонную разметку, отражающую, как эксперты интерпретировали бы изображения на практике. С помощью коммерческой платформы для ИИ без программирования клиницисты — не пишущие код — затем строили и обучали трёхмерную модель, имитирующую эти экспертные контуры, что позволяло медицинскому персоналу напрямую управлять процессом разработки.
Как ИИ видит опухоли в трёх измерениях
В основе системы лежит 3D-версия нейронной сети, известной как U-Net, разработанная для анализа целых КТ-томов, а не отдельных срезов. Она принимает стек грудных изображений и предсказывает для каждого небольшого объёма, относится ли он к опухоли или к нормальной ткани, фактически создавая 3D-маску опухоли. Во время обучения модель подвергали случайным поворотам, изменению масштаба и обрезке изображений, чтобы она стала устойчивой к незначительным различиям в положении пациента и настройках сканера. Исследователи затем измеряли, насколько предсказанные моделью области опухоли совпадают с экспертной разметкой, используя стандартные показатели перекрытия, которые учитывают точность границ и полноту покрытия объёма опухоли.
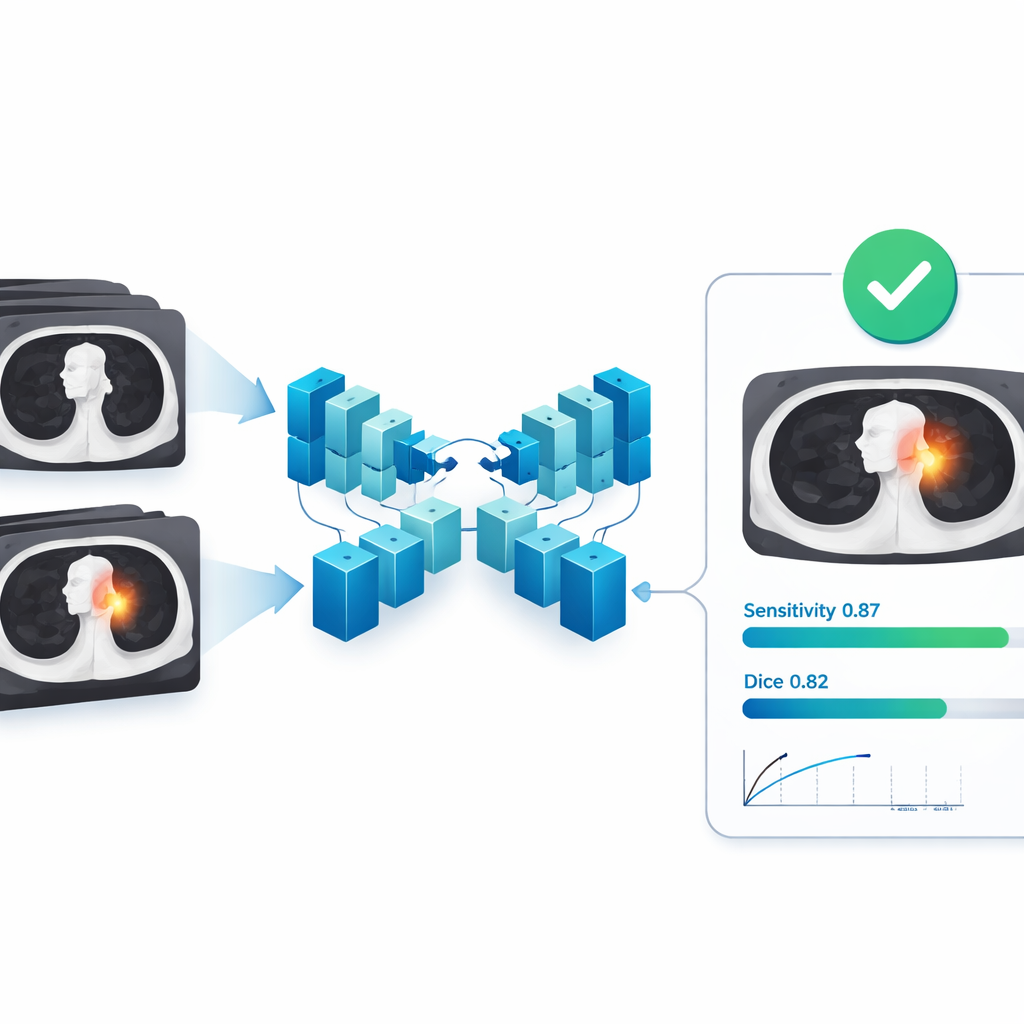
Результаты в разных больницах и при разных типах опухолей
На внешнем тестовом наборе из 121 независимой больницы модель ИИ продемонстрировала высокое согласие с экспертной сегментацией. В среднем показатель перекрытия (Dice) составил 0,82, сопутствующая метрика Intersection over Union — 0,72; точность и полнота находились примерно на уровне 0,82–0,85, что означает, что модель редко ошибочно помечала нормальную ткань как опухоль и успешно захватывала большую часть опухолевой ткани. Важно, что эти результаты сохранялись для аппаратов разных производителей, размеров и типов опухолей, что указывает на способность системы справляться с разнообразием, встречающимся в клинической практике. При оценке как детектора — просто обнаруживает ли она вообще каждое очаговое образование — модель достигла чувствительности примерно 0,87 даже при строгом критерии совпадения, при этом в среднем количество ложных срабатываний было значительно ниже одного на скан, что особенно привлекательно для поддержки скрининга рака.
Где система помогает, а где важна роль человека
Более детальный анализ удач и промахов выявил закономерность: ИИ показывал наилучшие результаты на крупных опухолях и испытывал трудности с очень маленькими или слабо контрастными очагами, частично пропуская их или путая с соседними нормальными структурами, такими как кровеносные сосуды или скопления жидкости. Это согласуется с повседневным опытом в радиологии, где крошечные или с низким контрастом находки легче всего упустить. Авторы утверждают, что инструмент лучше всего использовать в режиме «человек в цикле». Он может служить эффективным первым читателем, отмечая вероятные опухоли и очерчивая их границы, предоставляя готовые объёмы для таких задач, как планирование лечения и операции, в то время как радиологи сосредотачиваются на повторной проверке мелких, тонких или неоднозначных областей.
Что это значит для пациентов и будущих инструментов
Для неспециалиста главное послание таково: система ИИ, обученная на редкой, но тяжёлой группе опухолей грудной клетки, способна надёжно помогать врачам находить и очерчивать эти раки на КТ-сканах, даже в больницах, которые не предоставляли данные для её обучения. Предоставляя точные 3D-карты опухолей и удерживая количество ложных срабатываний на низком уровне, модель может ускорить диагностику, способствовать более точному планированию радиотерапии и операций и обеспечить дополнительную защиту от пропущенных очагов. В то же время работа подчёркивает, что ИИ не заменяет экспертную оценку — особенно для самых малых и слабых опухолей — а является многообещающим помощником, который становится мощнее по мере объединения клиницистов, изображений и простых в использовании платформ ИИ.
Цитирование: Takemura, C., Miyake, M., Kobayashi, K. et al. A clinically applicable and generalizable deep learning model for anterior mediastinal tumors in CT images across multiple institutions. Sci Rep 16, 6774 (2026). https://doi.org/10.1038/s41598-026-37504-z
Ключевые слова: передние средостенные опухоли, глубокое обучение в КТ-изображениях, сегментация медицинских изображений, поддержка диагностики рака, искусственный интеллект в радиологии