Clear Sky Science · ru
Исключительно селективное захватывание датчика напряжения каналов NaV1.5 Mg‑протопорфирином нарушает миграцию раковых клеток
Растительный пигмент указывает на новую стратегию в борьбе с раком
Наши сердца и опухоли могут иметь неожиданную уязвимость: особый тип электрического замка в мембране клетки, называемый NaV1.5. В этом исследовании показано, что природный родственник строительных блоков хлорофилла у растений — магний‑протопорфирин IX (MgPpIX) — способен с необычайной точностью блокировать этот замок. В результате он резко замедляет движение некоторых раковых клеток, что позволяет предположить: молекула, вдохновлённая химией фотосинтеза, может помочь сдерживать метастазирование, не нарушая при этом работу мозга или мышц.
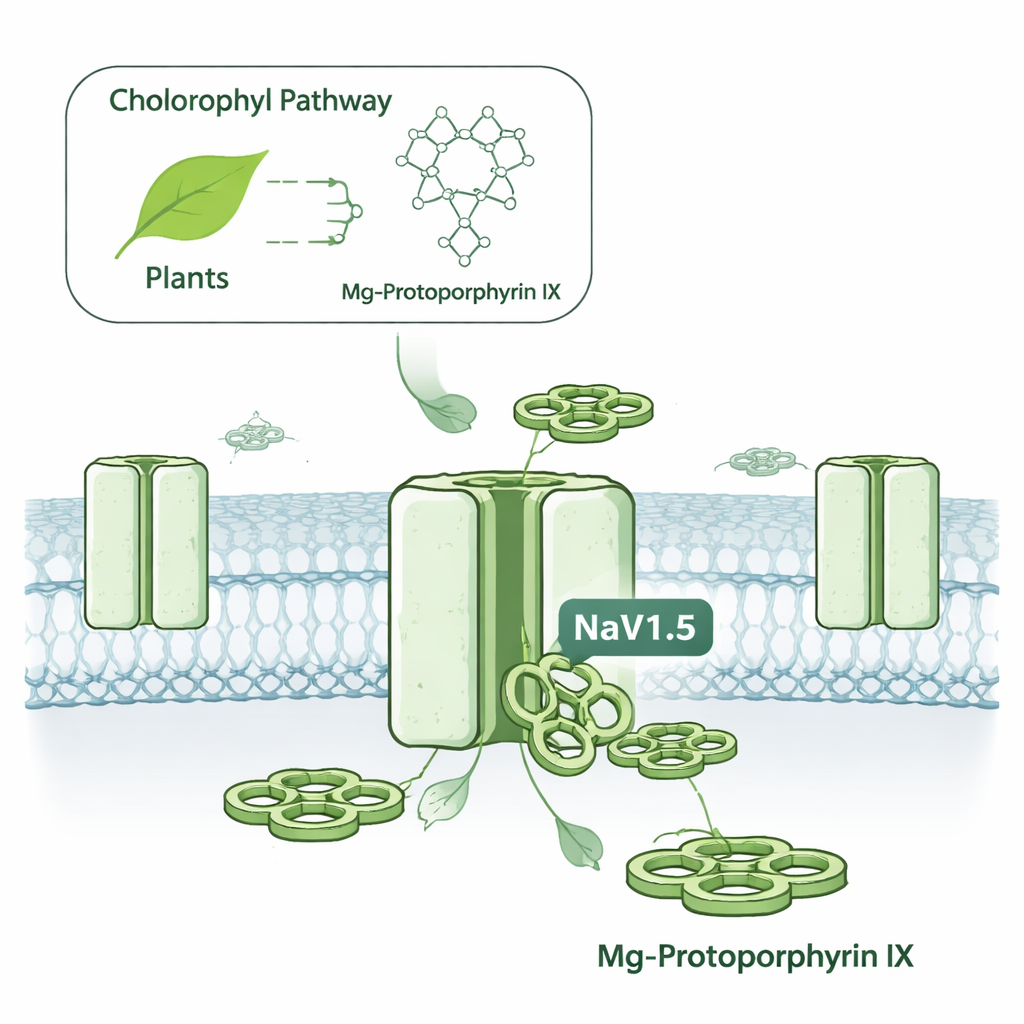
Скрытый электрический переключатель в раковых клетках
Клетки используют натриевые каналы с напряжением как крошечные дверцы, которые открываются и закрываются, пропуская заряженные частицы и создавая электрические сигналы. NaV1.5 наиболее известен по своей роли в сердечных сокращениях, где он помогает инициировать каждое сокращение. Но тот же канал встречается и в ряде опухолей, включая рак груди и толстой кишки, и его активность связывают с повышенной подвижностью и инвазивностью клеток. Нацеливание на NaV1.5 затруднено, потому что большинство препаратов против натриевых каналов также поражают родственные каналы в нервах и скелетных мышцах, что несёт риск побочных эффектов — судорог, онемения или слабости мышц. Авторы поставили цель выяснить, существуют ли малые молекулы, способные с гораздо более высокой селективностью отличать NaV1.5 от его родственников.
Блокатор, навеянный растениями, с рекордной точностью
Команда исследовала семейство кольцевых молекул, называемых металлическими протопорфиринами, которые напоминают ядра гема в крови и хлорофилла в растениях, но содержат разные центральные металлы. При нанесении различных вариантов на человеческие каналы NaV1.5, экспрессированные в клеточных культурах, один соединение выделялось: MgPpIX. Оно снижало электрический ток через NaV1.5 примерно на 99% в наномолярных концентрациях — примерно в 100 раз сильнее, чем железосодержащая версия (гемин). Другие металлические варианты, например с никелем или медью, по существу были неактивны. Поразительно, что MgPpIX не затрагивал несколько других типов человеческих натриевых каналов (используемых в мозге, периферических нервах и скелетной мышце) при тех же дозах, что делает его селективность одной из самых острых в этом семействе каналов.
Как молекула заклинивает маленький рычажок напряжения
Чтобы понять эту необычную точность, исследователи соединили генетические манипуляции с компьютерным моделированием. Натриевые каналы состоят из четырёх повторяющихся частей, каждая из которых содержит «датчик напряжения», смещающийся при изменении мембранного потенциала. Путём замены отдельных аминокислот между NaV1.5 и нечувствительными родственными каналами команда проследила действие MgPpIX до датчика напряжения во втором домене, в частности до двух остатков, обращённых наружу клетки. Молекулярно‑динамические симуляции в реалистичной мембранной среде показали, что MgPpIX располагается рядом с этим датчиком, когда тот находится в состоянии покоя, «вниз». Положительно заряжённый металлический центр MgPpIX притягивается к отрицательно заряженному боковому звену на канале, тогда как плоское кольцо взаимодействует с окружающими липидами. Это связывание, по-видимому, фиксирует датчик напряжения, не давая ему перейти в активное «вверх» состояние и тем самым удерживая канал закрытым. Интересно, что сильные деполяризации — например во время сердечного сокращения — могут временно сдвинуть молекулу, поведение, которое авторы описывают как «обратную зависимость от использования».
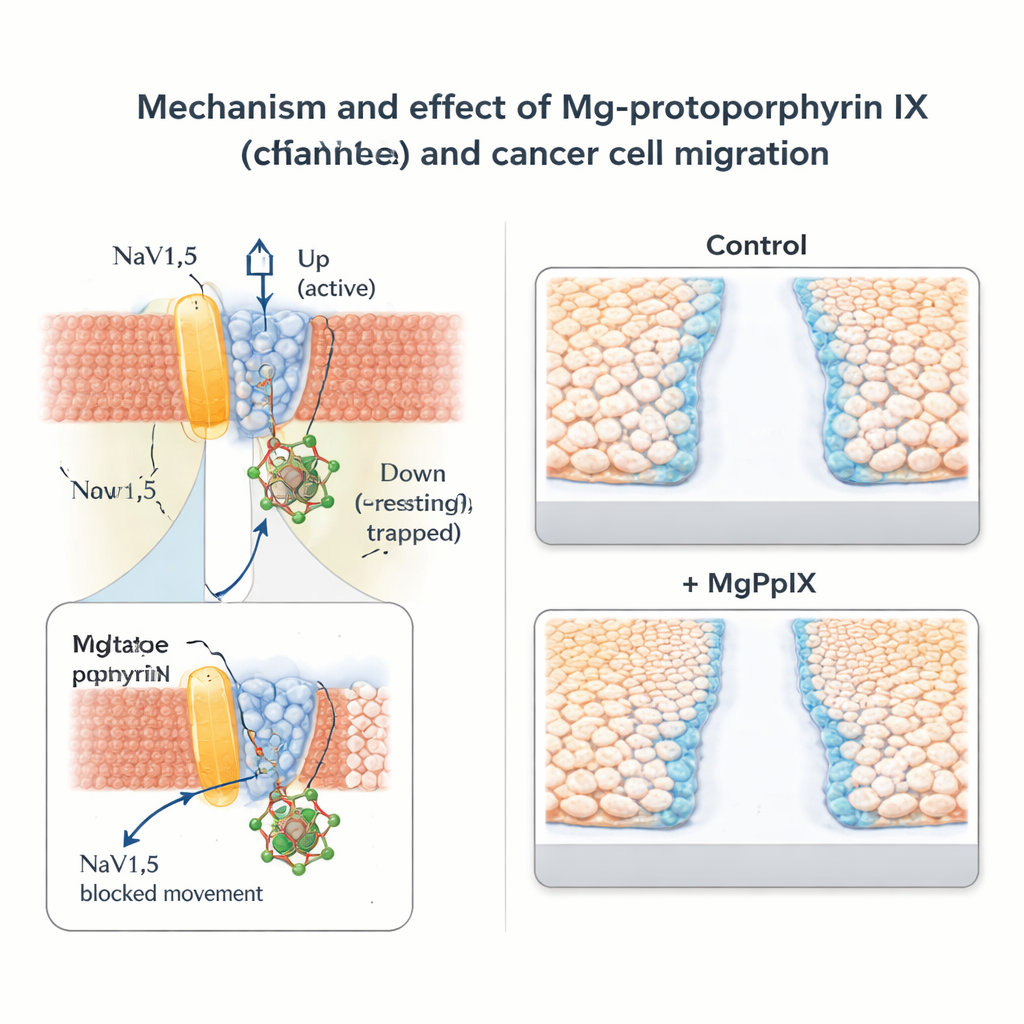
Замедление движения раковых клеток без широкого блока нервов
Далее команда изучила, что означает этот молекулярный тормоз для поведения раковых клеток. В линиях рака груди (MDA‑MB‑231) и рака толстой кишки (SW‑480), которые естественно экспрессируют NaV1.5, MgPpIX резко снижал натриевые токи и замедлял миграцию клеток в стандартных тестах «царапина» и трансуэлл. Чем сильнее данный металлический протопорфирин блокировал NaV1.5, тем больше он препятствовал движению клеток, что усиливает связь между активностью канала и подвижностью. Напротив, линии раковых клеток, лишённые NaV1.5, не реагировали на MgPpIX ни электрически, ни в тестах миграции, что поддерживает идею о высокой специфичности эффекта, а не общей токсичности. По сравнению с классическим токсином натриевых каналов тетродотоксином, MgPpIX достигал более сильного подавления миграции при гораздо более низких концентрациях.
Надежда и осторожность для будущих анти‑метастатических препаратов
Для неспециалиста основная идея такова: исследователи обнаружили растительное родственное соединение, которое действует как точный зажим на типе сердечного электрического замка, угнанного некоторыми опухолями. Захватывая маленький рычажок напряжения в положении покоя, MgPpIX способен сильно ограничивать подвижность раковых клеток в лабораторных условиях, при этом щадя другие натриевые каналы, важные для чувствительности и движения. Поскольку быстрая электрическая активность сердца может частично ослаблять этот блок, возможно существование окна безопасности, в котором опухолевые клетки будут подавлены сильнее, чем кардиальные. Хотя сам MgPpIX может не подойти в качестве лекарства, его уникальная сайт‑связываемость и механизм дают мощную схему для разработки будущих препаратов, направленных на остановку распространения рака путём целенаправленного ингибирования NaV1.5 с беспрецедентной селективностью.
Цитирование: Jamili, M., Ahmed, M., Bernert, A. et al. Exceptionally selective voltage-sensor trapping of NaV1.5 channels by Mg-protoporphyrin impairs cancer cell migration. Sci Rep 16, 4085 (2026). https://doi.org/10.1038/s41598-026-37492-0
Ключевые слова: натриевые каналы, Nav1.5, миграция раковых клеток, молекулы, производные хлорофилла, таргетная терапия ионных каналов