Clear Sky Science · ru
MiniPromoters Ple384 (TH) и Ple388 (PITX3) для нацеливания на дофаминергические нейроны среднего мозга у мышей и обезьян
Почему это исследование важно для здоровья мозга
Клетки мозга, вырабатывающие дофамин, помогают нам двигаться, учиться на основе вознаграждения и сохранять мотивацию. Именно эти клетки гибнут при болезни Паркинсона. Учёные и клиницисты хотят доставлять полезные гены или молекулярные инструменты непосредственно в эти уязвимые нейроны у лабораторных животных и, потенциально, у людей. Однако направить генную терапию так, чтобы она включалась только в нужных клетках, а не по всему мозгу, долгое время было серьёзным препятствием. В этом исследовании описаны два новых компактных ДНК «выключателя», которые надёжно активируют гены почти исключительно в дофаминергических нейронах среднего мозга у мышей и обезьян, открывая путь к более точным и потенциально безопасным лечениям.
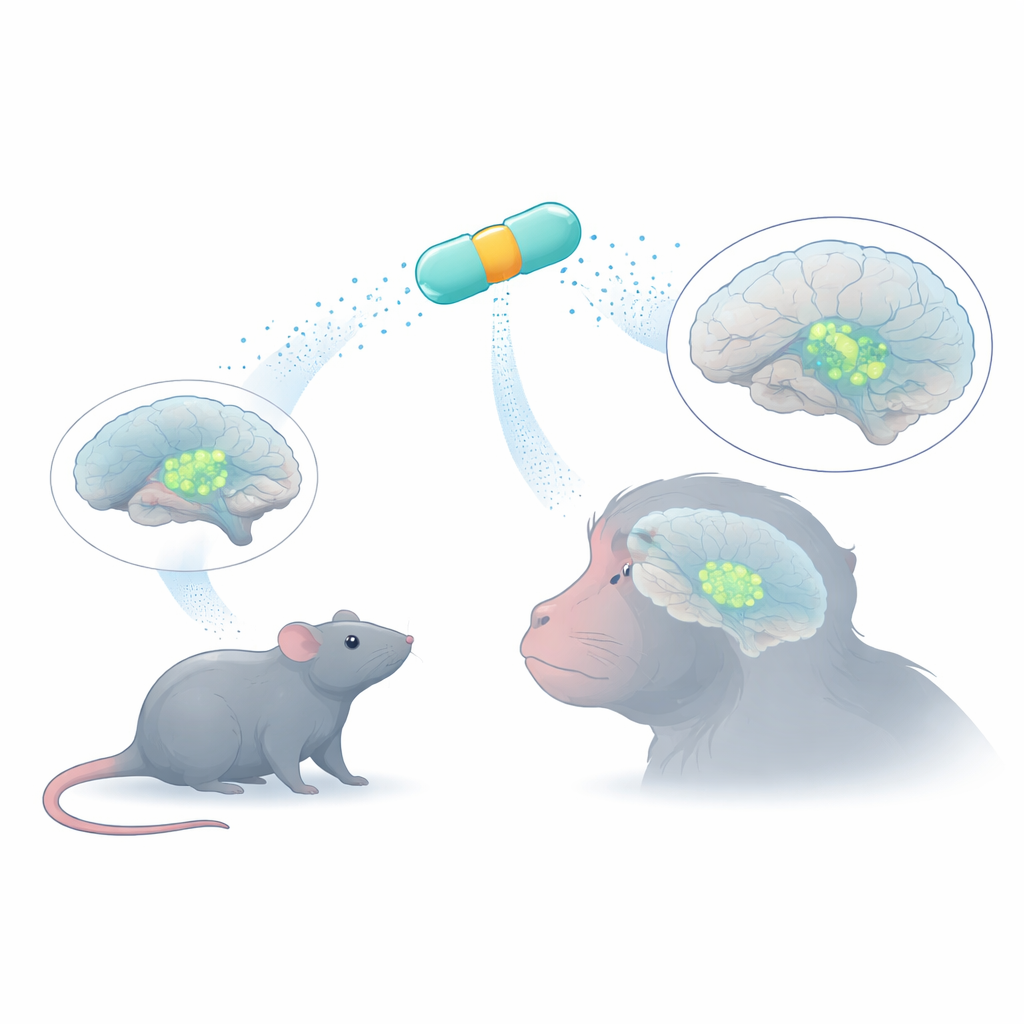
Маленькие генетические переключатели — большая задача
Для доставки терапевтического гена в клетки мозга исследователи часто используют адено-ассоциированные вирусы (AAV) — безопасные носители, которые могут переносить лишь ограниченное количество ДНК. Внутри каждого вируса короткая последовательность промотора действует как выключатель, определяя, где будет активен ген. Многие природные промоторы слишком большие или слишком неточные, в результате чего гены включаются во слишком многих типах клеток. Команда использовала биоинформатику, чтобы сконструировать восемь очень компактных «MiniPromoters» из человеческой ДНК — коротких комбинаций контрольных элементов, взятых из генов, известных как маркеры дофамин-продуцирующих нейронов. Их цель была создать набор переключателей, которые поместились бы в вектора AAV и при этом обеспечивали бы сильную, клеточно-специфичную экспрессию.
Поиск нужных мишеней в мозге мыши
Восемь кандидатных MiniPromoters сначала протестировали на мышах. Каждый промотор поместили в AAV, несущий зелёный флуоресцентный белок, что позволяло учёным увидеть, где выключатель активен. Вирусы вводили либо в кровоток, либо непосредственно в жидкостные пространства мозга. Большинство MiniPromoters не продемонстрировали требуемой селективности: некоторые подсвечивали многие недофаминовые клетки, другие практически не работали. Два промотора выделялись. Один, названный Ple384, был собран из регуляторных областей гена тирозингидроксилазы — ключевого фермента у всех катехоламин-продуцирующих нейронов. Другой, Ple388, происходил от PITX3, гена, важного для подмножества дофаминергических нейронов среднего мозга. И Ple384, и Ple388 давали яркий, строго ограниченный сигнал в компактной части субстанции нигры и в вентральной тегментальной области — центрах дофаминовых нейронов среднего мозга — при этом более 90% помеченных клеток также содержали характерную для дофамина молекулу.
От мышей к обезьянам без глубокого сверления мозга
Любая генная терапия для человека должна в итоге работать у приматов, чьи мозги больше и сложнее. Прямые инъекции в субстанцию нигру технически сложны и могут повредить эту маленькую глубокую структуру. Вместо этого исследователи проверили, можно ли доставить те же MiniPromoters в спинномозговую жидкость макак-резусов посредством одной инъекции в латеральный желудочек. Используя вариант капсида AAV, известный способностью широко распространяться от жидкостных пространств, они обнаружили, что и Ple384, и Ple388 обеспечивают устойчивую экспрессию в дофаминергических нейронах субстанции нигры и вентральной тегментальной области, при этом в значительной степени щадя другие богатые дофамином регионы, такие как гипоталамус и голубоватое пятно (locus coeruleus). Большинство помеченных клеток в целевой области оказались дофаминовыми нейронами, что подтверждает, что переключатели сохранили селективность между видами.
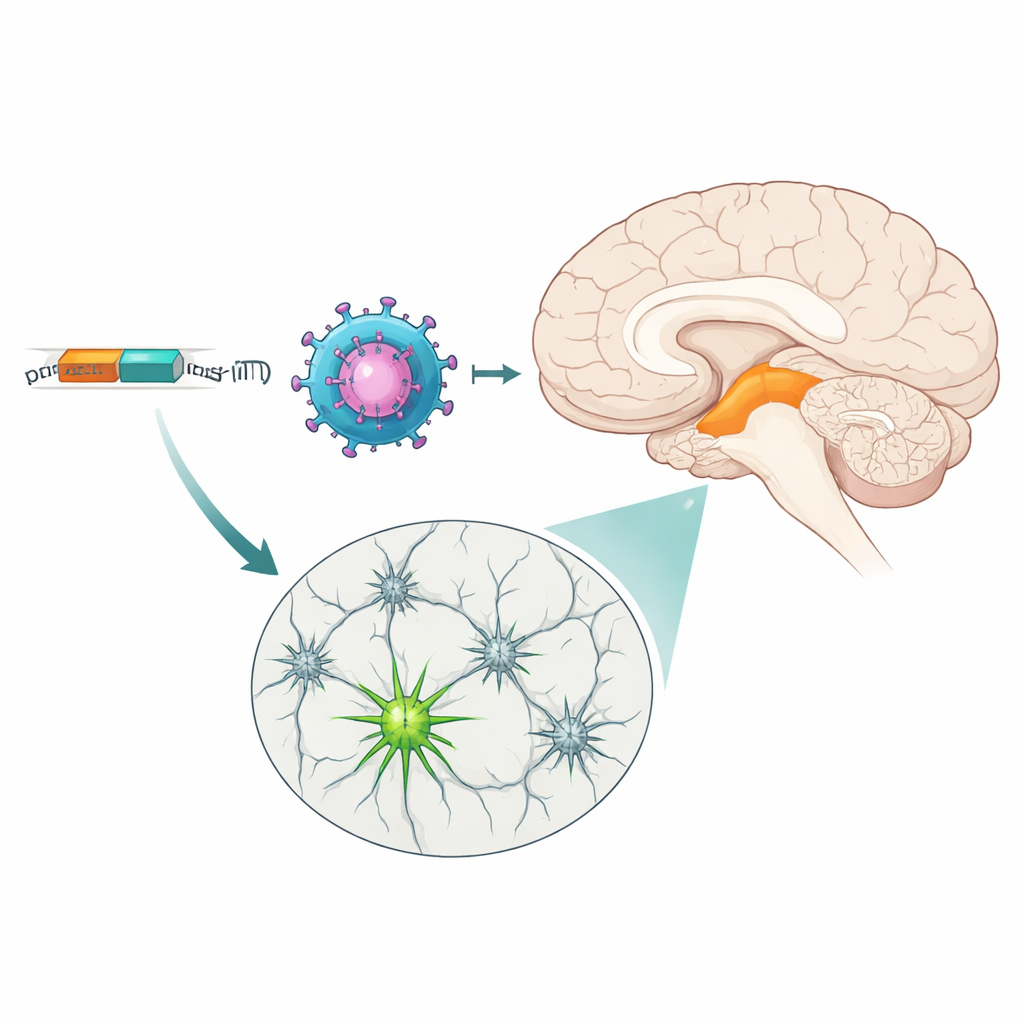
Два инструмента с разными сильными сторонами
Хотя оба MiniPromoters достигали целей, они демонстрировали разные паттерны. Ple384, основанный на более широкой экспрессии гена тирозингидроксилазы, подсвечивал больше нейронов в целом и охватывал как вентральные, так и дорсальные слои субстанции нигры, а также большую часть вентральной тегментальной области. Ple388, отражая более ограниченную экспрессию гена PITX3, в основном помечал подмножество вентральных нейронов и давал более слабую флуоресценцию. Внецелевое выражение наблюдали главным образом вблизи мест инъекций и в некоторых периферических органах после введения через кровоток, но тщательные контрольные эксперименты показали, что вирусные векторы способны достигать многих областей мозга; именно MiniPromoters ограничивали экспрессию преимущественно средней мозговой дофаминовой популяцией. Эта возможность регулировать силу — один переключатель более мощный и широкий, другой более селективный и умеренный — даёт исследователям выбор в зависимости от задач: от деликатной модуляции до масштабного вмешательства.
Что это значит для будущих терапий
Для неспециалиста ключевая мысль в том, что авторы создали два компактных генетических переключателя, которые действуют как точные, программируемые выключатели для дофаминовых нейронов у мышей и обезьян. Ple384 обеспечивает сильный и широкий доступ к этим клеткам, тогда как Ple388 ориентирован на более узкое, особенно уязвимое подмножество. Поскольку переключатели достаточно малы, чтобы удобно поместиться в обычно используемых вирусных векторах, они оставляют место для терапевтических генов и могут помочь снизить побочные эффекты, избегая ненужных участков мозга. По мере развития генной терапии болезни Паркинсона и родственных нарушений такие целевые регуляторные элементы станут ключевыми компонентами для лечения, которые будут одновременно мощными и точными.
Цитирование: Galvan, A., Choi, D., Korecki, A.J. et al. MiniPromoters Ple384 (TH) and Ple388 (PITX3) for targeting midbrain dopaminergic neurons in mice and monkeys. Sci Rep 16, 9277 (2026). https://doi.org/10.1038/s41598-026-37466-2
Ключевые слова: дофаминовые нейроны, генная терапия, болезнь Паркинсона, векторы AAV, клеточно-специфичные промоторы