Clear Sky Science · ru
Терапевтические эффекты IGF-2 при ДПОН через угнетение апоптоза астроцитов путем модуляции сигнального пути IGF-1R/PI3K/AKT
Защита мозга при малоизвестном аутоиммунном заболевании
Спектр нарушений, связанных с невромиелитом оптика (ДПОН), — редкое, но разрушительное аутоиммунное заболевание, которое поражает зрительные нервы и спинной мозг, часто оставляя пациентов с потерей зрения, параличом или серьёзными когнитивными нарушениями. Существующие препараты в основном подавляют иммунную систему, дорогие и не обеспечивают прямой защиты клеток мозга от повреждения. В этом исследовании изучают, может ли естественная молекула, связанная с ростом и присутствующая в крови — IGF‑2 — помочь защитить клетки мозга при ДПОН и предложить новый подход к лечению болезни.
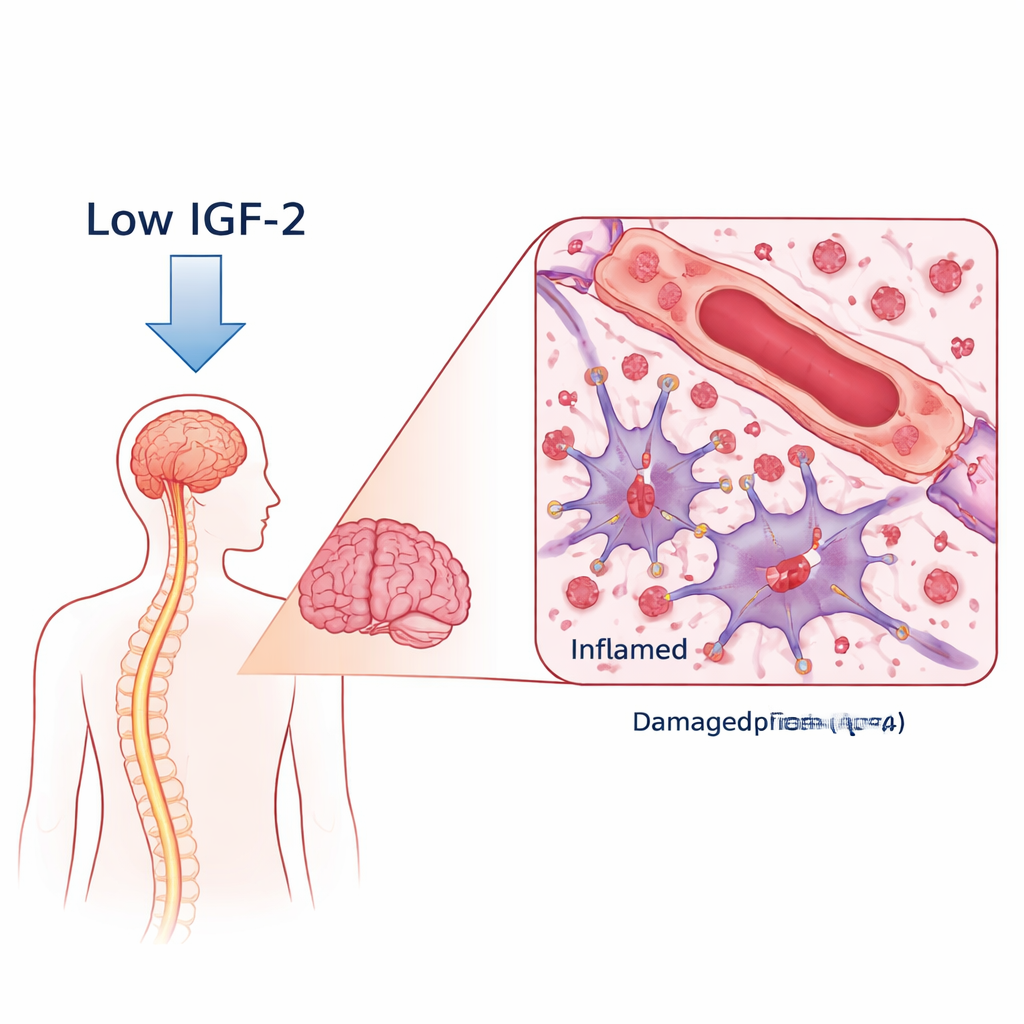
Вредное антитело и отсутствующий защитник
При ДПОН организм вырабатывает антитела против водного канала AQP4, расположенного на звездообразных поддерживающих клетках мозга — астроцитах. Когда эти антитела связываются с AQP4, они запускают иммунные атаки, которые повреждают астроциты, лишают аксоны миелина (изоляционной оболочки) и могут повредить нейроны. Исследователи сравнили кровь женщин с положительным на антитела к AQP4 ДПОН и кровь здоровых добровольцев. При широком профилировании белков они обнаружили, что уровни IGF‑2 у пациентов с ДПОН заметно ниже, тогда как два связывающих белка IGF, способные захватывать IGF‑2, были повышены. Важно, что у пациентов с наименьшим количеством IGF‑2, как правило, были более выраженные нарушения функций и худшие результаты тестов на мышление и память, что связывает эту молекулу с тяжестью заболевания и когнитивным здоровьем.
Стандартная терапия способствует восстановлению IGF-2
Многие пациенты с ДПОН получают ритуксимаб — препарат, уничтожающий B-клетки, продуцирующие антитела. Команда измерила белки в крови до и после лечения ритуксимабом. После терапии уровни IGF‑2 повысились, а связывающие белки снизились, приблизившись к образцу, наблюдаемому у здоровых людей. Это указывает на то, что успокоение иммунной системы может позволить организму восстановить некоторые собственные защитные факторы. Хотя ритуксимаб не нацелен специально на IGF‑2, сдвиг в этой молекуле намекает, что она может быть частью восстановительного ответа организма, и мониторинг IGF‑2 может помочь отслеживать состояние пациентов со временем.
Испытание IGF-2 на модельной мышиной версии болезни
Чтобы выяснить, может ли IGF‑2 делать больше, чем служить маркером тяжести болезни, учёные обратились к мышиной модели. Они вводили в мозг мышей человеческие антитела к AQP4 и человеческий комплемент, что воспроизвело ключевые черты ДПОН: потерю AQP4 на астроцитах, воспаление, повреждение миелина и слабость конечностей. Другая группа мышей сначала получила безвредный вирус, заставляющий клетки мозга продуцировать дополнительный IGF‑2. Эти мыши с повышенным IGF‑2 теряли меньше веса, имели более лёгкие нарушения подвижности и демонстрировали меньше потерь миелина и воспаления в тканях мозга и спинного мозга. Стандартное лечение ритуксимабом также помогало, но сверхэкспрессия IGF‑2, по-видимому, защищала ткань мозга более прямо, что указывает на нейропротекторную роль, а не только на иммуноподавляющий эффект.
Как IGF-2 подавляет гибель клеток и воспаление
Затем команда изучала астроциты в культурах, подвергнутые воздействию антител из ДПОН. Обычные действия этих антител снижали уровень ключевого рецептора IGF‑1R и угнетали нижестоящий защитный путь PI3K/AKT, одновременно активируя белки «самоуничтожения» и провоспалительные сигналы. Когда исследователи заставляли астроциты синтезировать больше IGF‑2, этот защитный путь снова включался, маркёры гибели клеток снижались, а клетки выделяли меньше провоспалительных молекул, таких как IL‑1β, IL‑6 и TNF‑α. Блокада рецептора IGF‑1R частично стирала эти преимущества, показывая, что IGF‑2 действует главным образом через активацию каскада IGF‑1R/PI3K/AKT внутри астроцитов. В живых мышах усиление IGF‑2 также снижало активацию микроглии — иммунных стражей мозга — и уменьшало уровни провоспалительных сигналов в крови.
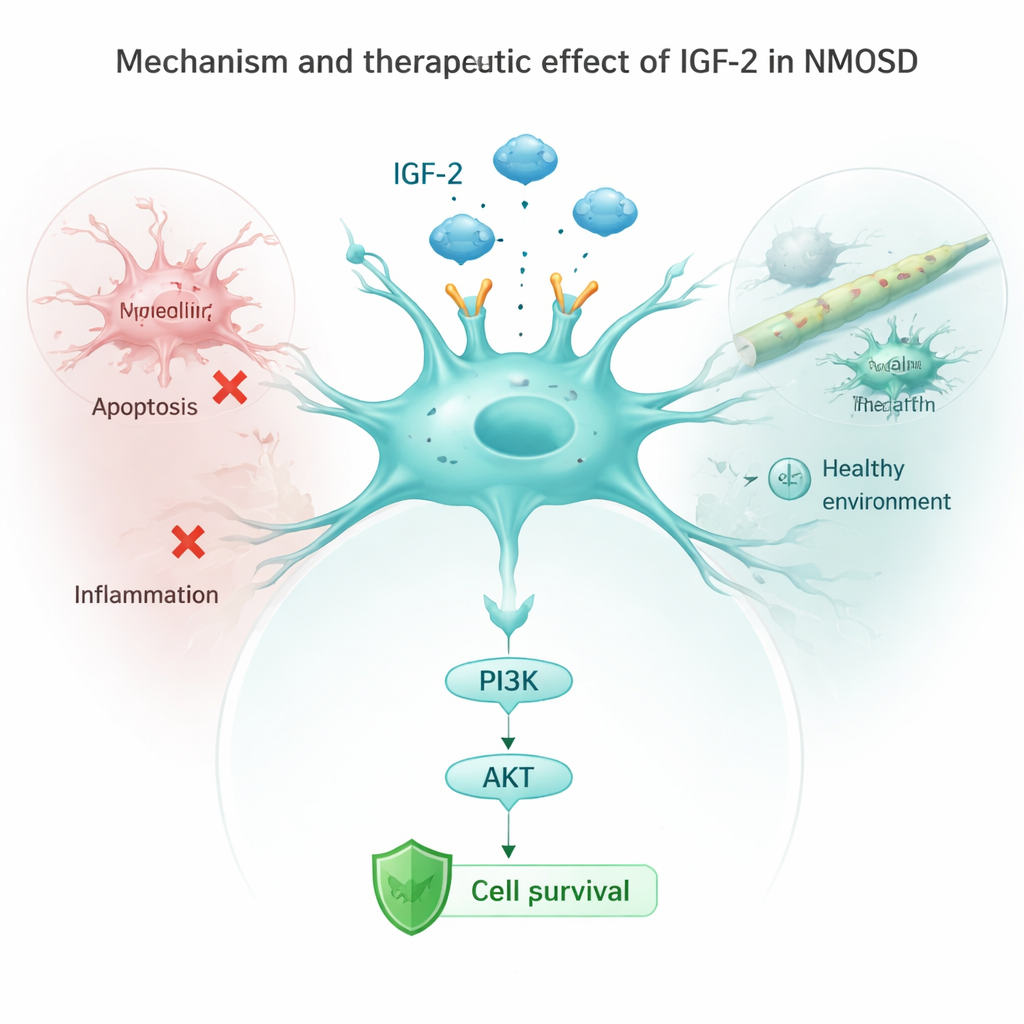
Что это может значить для пациентов
В сумме эти данные позволяют предположить, что низкий уровень IGF‑2 является и предвестником, и упущенной возможностью при ДПОН. У пациентов с меньшим количеством IGF‑2, как правило, более выраженная инвалидизация и ухудшение когнитивных функций, тогда как восстановление или усиление IGF‑2 в экспериментальных моделях помогает выживать астроцитам, снижает воспаление в мозге и уменьшает повреждение нервов. Хотя работа находится на ранней стадии и основана на небольших группах пациентов и на животных, она указывает на IGF‑2 как перспективную мишень для будущих терапий, которые могли бы не только ослаблять иммунную атаку, но и напрямую защищать уязвимые клетки мозга.
Цитирование: Zhang, Y., Xu, N., Yu, K. et al. Therapeutic effects of IGF-2 on NMOSD by inhibiting astrocyte apoptosis through modulation of the IGF-1R/PI3K/AKT signaling pathway. Sci Rep 16, 6312 (2026). https://doi.org/10.1038/s41598-026-37456-4
Ключевые слова: невромиелит оптика, астроциты, IGF-2, нейровоспаление, нейропротекция