Clear Sky Science · ru
Интеграция сетевой токсикологии, машинного обучения и молекулярно-динамических симуляций для раскрытия двойного механизма действия тансихинона IIA при ТНБК и доксорубицин-индуцированной кардиотоксичности
Почему это исследование важно для пациентов
Доксорубицин — ключевой препарат при раке молочной железы, но у него есть серьёзный недостаток: он может повреждать сердце, иногда спустя годы после завершения лечения. В то же время тройной негативный рак молочной железы — трудно поддающаяся терапии форма, лишённая привычных гормональных и факторных мишеней — по‑прежнему требует улучшенных методов лечения. В этом исследовании изучают, может ли тансихинон IIA, соединение из традиционного китайского растения Salvia miltiorrhiza, одновременно защищать сердце от токсичности доксорубицина и атаковать агрессивные опухоли, что потенциально сделает химиотерапию более безопасной и эффективной.
Одна молекула — две серьёзные проблемы
Доксорубицин спас бесчисленное количество жизней, но его преимущества ограничены зависящей от дозы кардиотоксичностью: при превышении определённой суммарной дозы риск сердечной недостаточности резко растёт. Врачи часто оказываются перед болезненным выбором между контролем опухоли и защитой сердца. Ранние лабораторные работы показали, что тансихинон IIA может усиливать антиоксидантные защиты в кардиомиоцитах и прямо убивать раковые клетки, но молекулярные механизмы оставались неясными. Авторы поставили цель системно проследить, как одно соединение может ослаблять повреждение сердца и одновременно поражать тройной негативный рак молочной железы, прокладывая мост между традиционной медициной и современной прецизионной онкологией. 
Поиск в больших биологических данных ради защиты сердца
Чтобы понять механизмы защиты сердца, команда сначала собрала тысячи генов, связанных с кардиотоксичностью, из нескольких крупных баз данных и объединила их с известными белковыми мишенями доксорубицина и тансихинона IIA. Выделились тринадцать «пересекающихся» мишеней — белков, связанных с повреждением сердца, взаимодействующих с доксорубицином и потенциально модулируемых тансихиноном IIA. С помощью карт белок–белковых взаимодействий исследователи сузили список до шести ключевых участников, включая CCND1 (регулятор клеточного цикла), APAF1 (инициатор программируемой клеточной смерти), AR (андрогеновый рецептор), TERT (важный для поддержания концов хромосом), MMP2 (фермент, участвующий в ремоделировании тканей) и NQO1 (антиоксидантный фермент). Компьютерное докирование и молекулярно-динамические симуляции показали, что и доксорубицин, и тансихинон IIA могут прочно связываться с этими белками, однако комплексы с тансихиноном IIA часто оказываются более стабильными и энергетически выгодными, что подразумевает: растительное соединение может перенаправлять или смягчать вредные сигналы доксорубицина в сердце.
Как он нацелен на агрессивные опухоли молочной железы
Со стороны онкологии исследователи сосредоточились на наборах данных экспрессии генов при тройном негативном раке молочной железы. Они сравнили образцы опухолей с нормальной тканью молочной железы, чтобы найти сотни генов, аномально включённых или выключённых. Затем применили методику взвешенного анализа ко‑экспрессии генов (WGCNA), чтобы выявить группы генов, наиболее тесно связанных с фенотипом тройного негатива. Пересечение этих онкологических генов с предсказанными мишенями тансихинона IIA позволило сузить список кандидатов, после чего были применены три независимых метода машинного обучения, чтобы определить, какие гены лучше всего отличают опухоль от нормальной ткани и наиболее вероятно имеют клиническое значение. Согласующиеся результаты выделили единственную заметную мишень: EZH2 — ген, участвующий в упаковке ДНК и часто гиперактивный в агрессивных опухолях.
Связь биологии опухоли и иммунной системы
Чтобы понять, почему EZH2 важен у реальных пациентов, команда проанализировала большие онкологические базы данных. Они обнаружили, что EZH2 выражён значительно сильнее в инвазивных опухолях молочной железы по сравнению с нормальной тканью. Хотя уровень его экспрессии не был прямо связан с общей выживаемостью во всех случаях рака молочной железы, EZH2 тесно коррелировал с особенностями иммунной микросреды опухоли. Более высокая экспрессия EZH2 сочеталась с большим проникновением нескольких типов иммунных клеток — таких как B‑ и T‑лимфоциты — и с повышенной экспрессией молекул, как стимулирующих, так и подавляющих иммунный ответ, включая известные контрольные белки (checkpoints) вроде CTLA‑4 и LAG‑3. Эти паттерны указывают на то, что EZH2 находится на перекрёстке роста опухоли и иммунного контроля, и что препарат вроде тансихинона IIA, влияя на EZH2, может помочь перестроить то, как иммунная система распознаёт и атакует тройной негативный рак молочной железы. 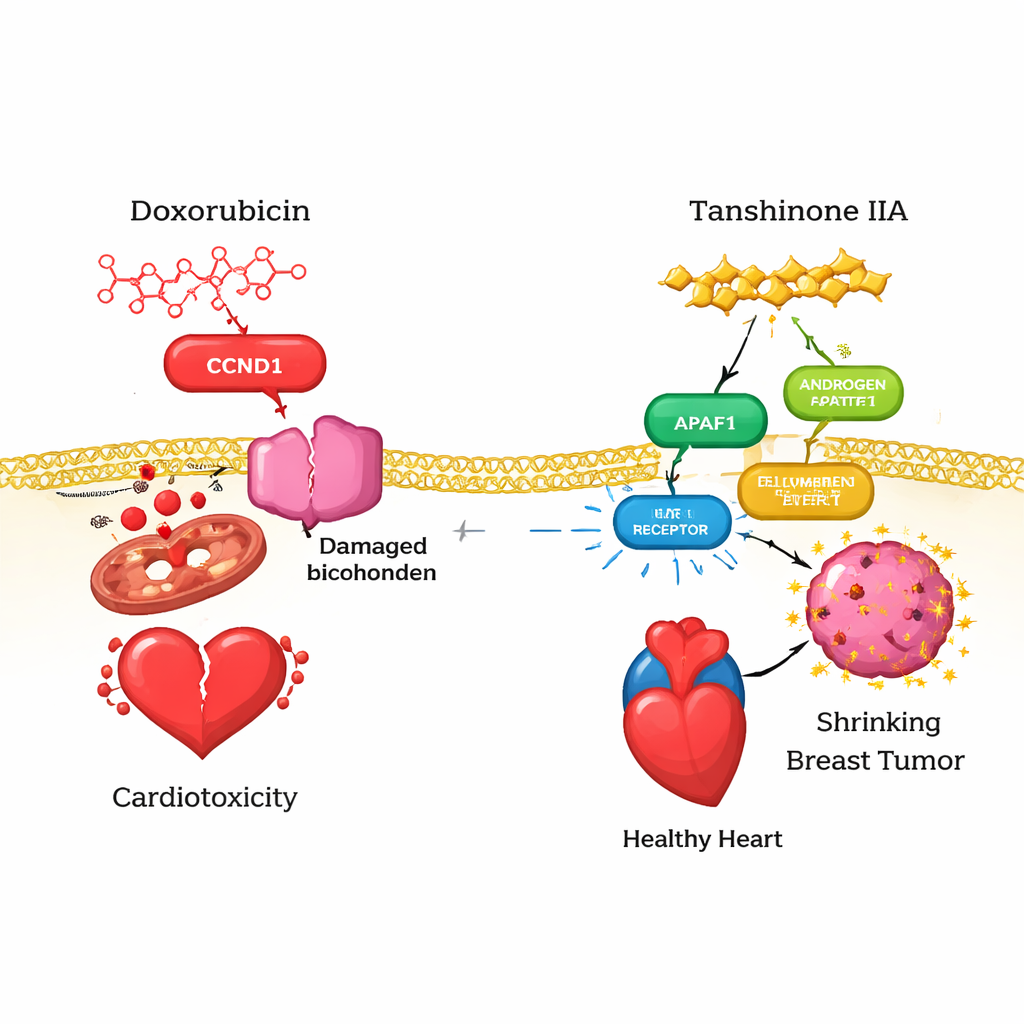
Что это может значить для будущего лечения
Проще говоря, работа предлагает, что тансихинон IIA может выполнять двойную роль в уходе за пациентами с раком молочной железы: выступать как нечто вроде «химического щита», уменьшающего повреждение сердца, связанное с доксорубицином, за счёт стабилизации ключевых кардиозащитных белков, и одновременно служить прицельным средством против тройного негативного рака молочной железы через влияние на EZH2 и связанные иммунные пути. Эти выводы основаны на вычислительных и статистических анализах, а не на исследованиях на животных или людях, поэтому они представляют собой раннюю «дорожную карту», а не готовую к клическому применению терапию. Тем не менее они дают подробную молекулярную схему для разработки комбинированных подходов, сохраняющих жизнь спасительную эффективность доксорубицина и уменьшающих его долгосрочные риски — а также для трансляции компонента традиционной медицины в современное, механистически обоснованное онкологическое дополнение.
Цитирование: Wu, B., Lan, Xh., Chen, Xq. et al. Integrating network toxicology, machine learning, and molecular dynamics simulations to reveal tanshinone iia’s dual mechanisms in TNBC and doxorubicin-induced cardiotoxicity. Sci Rep 16, 6861 (2026). https://doi.org/10.1038/s41598-026-37428-8
Ключевые слова: тансихинон IIA, кардиотоксичность доксорубицина, тройной негативный рак молочной железы, EZH2, сетевая фармакология