Clear Sky Science · ru
Анализ систолической функции сердца у мышей с нокаутом PERM1 с использованием больших когорт животных
Почему маленькие мышиные сердца важны для здоровья человека
Сердечную недостаточность часто описывают как уставший насос, но то, что делает сердце слабым, оказывается удивительно сложным. В этом исследовании учёные использовали необычно большую группу мышей, чтобы задать конкретный вопрос: приводит ли выключение одного гена PERM1, известного тем, что помогает сердечным клеткам вырабатывать энергию, к изменению силы сокращения сердца? Тщательно просканировав сердца более чем 170 животных, они показали, что этот ген слегка меняет форму сердца и снижает его сократительную силу, в то время как мыши в целом остаются внешне здоровыми. Полученные данные помогают разрешить спор в области и дают план для разработки более удачных экспериментов по изучению сердца в будущем.
Ген, соединяющий использование топлива и силу сокращения
PERM1 был впервые выявлен как переключатель, усиливающий выработку энергии в мышечных клетках, включая сердечные. Ранние работы показали, что уровень PERM1 снижается в ослабленных сердцах как у мышей, так и у людей, что поднимает гипотезу о том, что низкий PERM1 может действительно способствовать слабым ударам сердца. Но исследования на мышах с нокаутом PERM1 — животных, лишённых этого гена — дали противоречивые результаты относительно того, действительно ли их сердца перекачивают кровь менее эффективно. Поскольку PERM1 рассматривается как потенциальная мишень для новых терапий при сердечной недостаточности, авторы поставили задачу проверить его влияние на функцию сердца с достаточным числом животных и строгой статистикой, чтобы получить ясный ответ «да» или «нет».
Большой по числу взгляд на маленькие сердца
Команда собрала данные эхокардиографии — ту же ультразвуковую методику, которую используют в клиниках кардиологии — для каждой мыши с нокаутом PERM1 и её здорового родственного аналога, используемых в их лаборатории в течение 18‑месячного периода. Этот ретроспективный охват дал 84 нормальных (диких) и 88 нокаутных животных — размер выборки значительно больше типичного для исследований сердца у мышей. По ультразвуковым изображениям они измеряли стандартные показатели работы левого желудочка, основной камеры-насоса. Ключевой показатель — фракция выброса, процент крови, выбрасываемый при каждом сокращении, а также сопутствующие параметры: насколько уменьшается диаметр желудочка при сокращении, толщина стенок и общий объём крови, прокачиваемый в минуту.
Слабее сокращение, большая камера, похожий выброс
Результаты показывают последовательную картину. В среднем фракция выброса снизилась с примерно 65% у нормальных мышей до 54% у нокаутов PERM1 — разница, достаточная, чтобы иметь клиническое значение у людей, и подтверждённая очень сильными статистическими показателями. Другие меры сокращения, такие как фракционное укорочение и утолщение стенки, также уменьшились. В то же время левые желудочки нокаутов были заметно больше, особенно в конце сокращения, что указывает на то, что в камере оставалось больше крови. Несмотря на более слабое сокращение, общий объём перекачиваемой в минуту крови упал всего незначительно — примерно на 6% — потому что увеличенные камеры изначально могли содержать больше крови. Другими словами, сердце частично компенсировало плохое сокращение растяжением основной камеры.
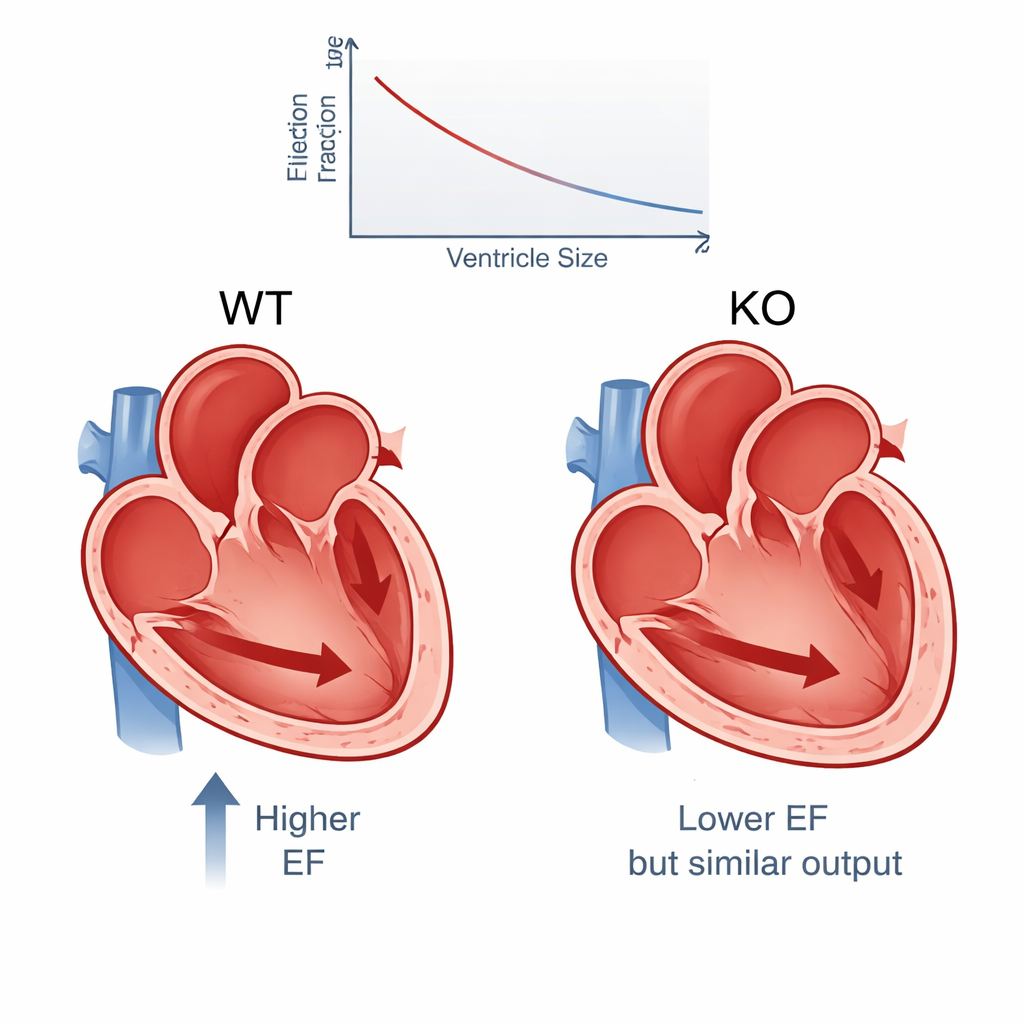
Скрытое разнообразие в «идентичных» сердцах
Поскольку в исследовании было много животных, исследователи могли заглянуть дальше средних значений и изучить, как варьировали отдельные сердца. Даже среди генетически идентичных здоровых мышей они обнаружили удивительно широкий разброс фракции выброса. Нокаут PERM1 сдвинул всё распределение вниз — появилось больше сердец с более низкой сократительной силой — но сам разброс не стал шире. Примерно у 7% нокаутных мышей фракция выброса была ниже 40% — уровень, который у людей квалифицируется как сердечная недостаточность с уменьшенной фракцией выброса — тем не менее эти мыши всё ещё сохраняли почти нормальный минутный объём крови. Статистический анализ показал, что пол, возраст и масса тела объясняли лишь небольшую часть изменчивости; большинство различий, вероятно, связано с труднее измеримыми биологическими факторами, такими как тонкие экологические влияния или эпигенетические изменения.
Что это значит для будущих исследований сердца
Чтобы помочь другим учёным лучше проектировать эксперименты, авторы использовали свою большую базу данных для расчёта того, сколько животных обычно нужно, чтобы обнаружить значимые изменения по каждому параметру сердца. Они обнаружили, что скромные размеры групп, часто используемые в этой области, легко пропускают реальные, но умеренные эффекты, особенно для тонких мер, таких как ударный объём или сердечный выброс. В целом исследование убедительно доказывает, что утрата PERM1 вызывает специфическое ремоделирование сердца — увеличение камер, ослабление сокращения — а не полную недостаточность, и что это ремоделирование частично компенсируется структурными изменениями, помогающими сохранить кровоток. Для неспециалистов главный вывод таков: один ген, регулирующий энергию, может сместить сердце в новый рабочий режим, который выглядит здоровым снаружи, но несёт за собой тихие изменения в конструкции насоса и в том, насколько сильно он работает.
Цитирование: Zaitsev, A.V., Sreedevi, K., Goode, B. et al. Analysis of systolic cardiac function in PERM1-knockout mice using large cohorts of animals. Sci Rep 16, 7705 (2026). https://doi.org/10.1038/s41598-026-37420-2
Ключевые слова: сердечная недостаточность, сердечная сократимость, митохондриальная энергетика, модельные мыши, эхокардиография