Clear Sky Science · ru
Мутация GJB2 c.109G > A активирует путь митохондриального апоптоза через IFI27, приводя к наследственной несиндромной тугоухости
Почему крошечные клетки уха важны для будущего детей
Глухота, присутствующая при рождении, затрагивает миллионы детей по всему миру и часто определяет, как они научатся говорить, добьются успеха в школе и наладят общение с окружающими. Одним из наиболее частых генетических виновников является ген GJB2, однако врачи до сих пор не полностью понимали, как изменения в этом гене повреждают внутреннее ухо. В этом исследовании на данио-рерио и человеческих клетках прослеживается цепочка событий от одной замены в ДНК GJB2 до гибели хрупких звукоощущающих клеток, а также указывают на новую молекулу IFI27 как возможную мишень для будущих лечений.
Распространённая генетическая замена, стоящая за детской глухотой
Учёные начали с анализа образцов крови от 1 199 детей с подозрением на наследственную тугоухость в провинции Фуцзянь, Китай. Они сосредоточились на нескольких хорошо известных генах, связанных с глухотой, и обнаружили, что изменения в GJB2 доминируют, составляя 85% всех выявленных мутаций. Среди них наиболее частой оказалась конкретная замена c.109G>A (также известная как p.Val37Ile). Этот вариант относительно распространён в общей популяции, но заметно обогащён среди людей с нарушением слуха, что указывает на его значительную роль в несиндромной тугоухости — проблемах со слухом, которые возникают без других медицинских проявлений.
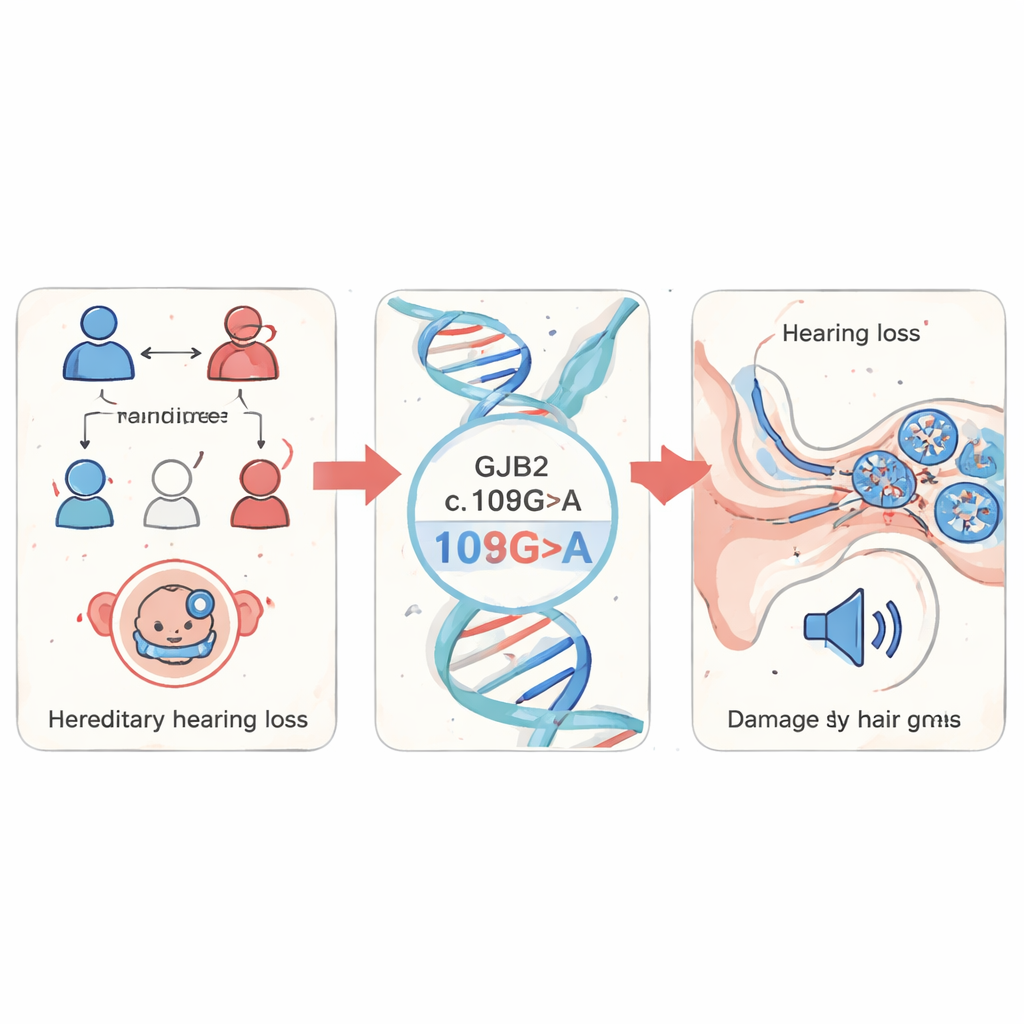
Проследить повреждения в прозрачной рыбке
Чтобы увидеть, что делает эта мутация в живом организме, команда обратилась к данио-рерио — маленькой пресноводной рыбке, эмбрионы которой прозрачны и которые имеют множество общих генов и структур уха с человеком. Они модифицировали эмбрионы, чтобы те экспрессировали либо нормальный человеческий GJB2, либо мутантную версию c.109G>A, а также использовали подход «подавления» (knockdown) для снижения активности собственного гена gjb2 у рыбы. Эмбрионы с мутантным или подавленным геном демонстрировали замедленное развитие, искривлённые хвосты и отёки вокруг сердца — признаки нарушения развития. Самое важное, что их внутреннее ухо было явно неправильным: ключевые структуры — отолиты — были меньшего размера и расположены дальше друг от друга, а заполненная жидкостью кохлеарная область была уменьшена. Когда учёные возвращали нормальный GJB2 вместе с мутантом, многие структурные дефекты улучшались, что показало, что именно мутация вызывает эти нарушения.
От повреждённых ушей к ухудшению слухового поведения
Поскольку слух зависит от крошечных «волосковых» клеток, превращающих звуковые колебания в нервные сигналы, команда окрашивала эти клетки у данио. У рыб с мутацией GJB2 или с подавлением гена число волосковых клеток было значительно меньше как во внутреннем ухе, так и по поверхности тела, где данио также воспринимают движение воды. Затем исследователи проверяли, насколько хорошо рыбы реагируют на звук. С помощью автоматизированной системы отслеживания они измеряли, как далеко и как быстро пятничные личинки в возрасте 5 дней плавали при кратковременных звуковых всплесках. Нормальные и дикотипные рыбы с GJB2 реагировали увеличением дистанции и скорости плавания, тогда как мутантные и подавленные рыбы практически не меняли поведение, что указывает на нарушение слуха. И снова добавление нормального GJB2 частично восстанавливало как число волосковых клеток, так и вызванные звуком движения.
Путь смерти внутри энергетических центров клетки
Чтобы понять происходящее внутри клеток, учёные провели секвенирование РНК и сравнили активность генов у нормальных данио и у тех, у кого был снижен gjb2. Набор генов, связанный с «митохондриальным апоптозом» — самоуничтожительным маршрутом, сосредоточенным в энергетических центрах клетки — был сильно активирован. В частности, выделялись несколько членов семейства IFI27, а также известные участники клеточной гибели, такие как Bax, цитохром c, Apaf1 и каспазы. Последующие эксперименты на человеческих клетках HEK293 подтвердили эту картину: клетки с мутантным GJB2 производили больше реактивных форм кислорода (ROS, форма окислительного стресса), сильнее высвобождали цитохром c из митохондрий и активировали белки апоптоза, что приводило к увеличению гибели клеток. Когда исследователи инактивировали IFI27 в клетках с мутантом, уровень ROS снизился, сигналы смерти ослабли, и меньше клеток подверглось апоптозу.
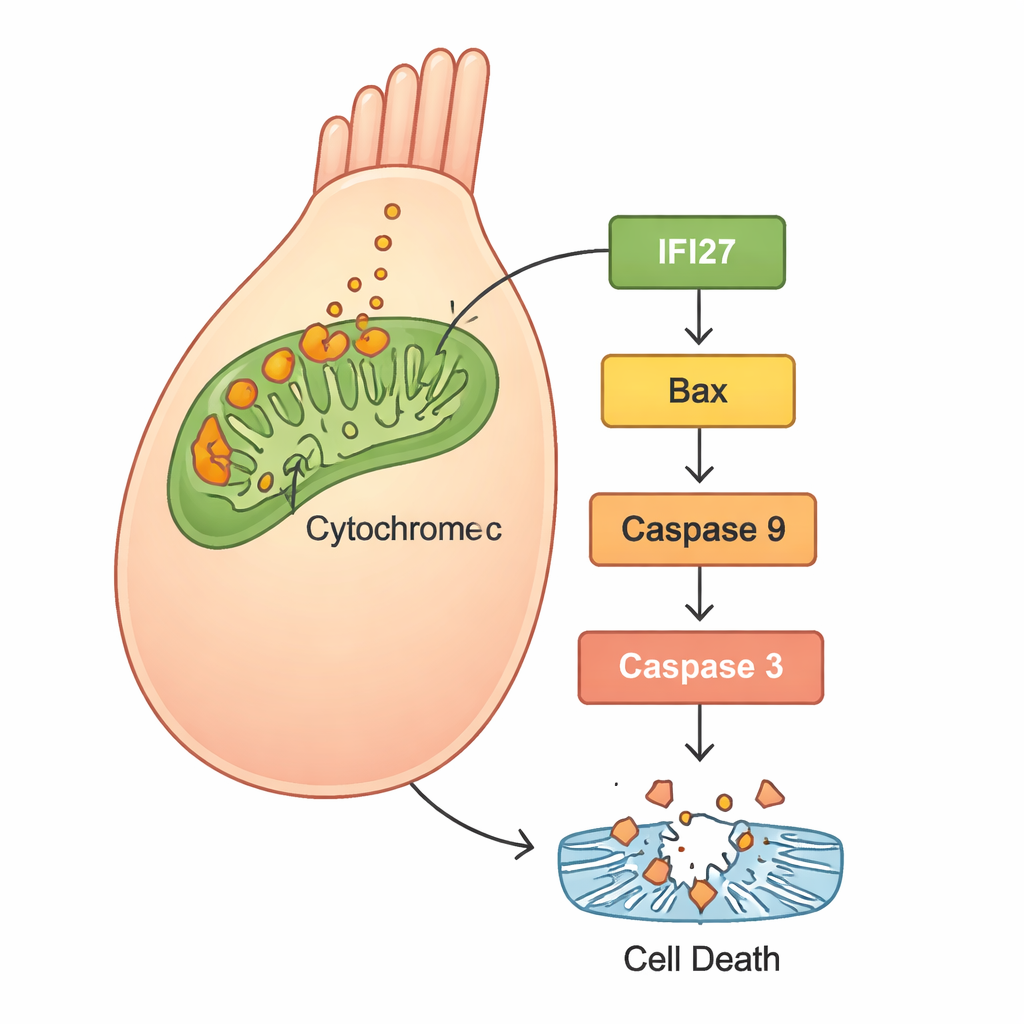
Что это значит для будущих терапий
В совокупности результаты предлагают ясный сценарий: мутация GJB2 c.109G>A нарушает нормальное развитие и функцию внутреннего уха не только за счёт изменения клеточной коммуникации, но и путём запуска стресса в митохондриях. Этот стресс усиливает экспрессию IFI27 и связанных генов, вызывает высвобождение цитохрома c и активирует каскад белков, толкающих волосковые клетки к программируемой гибели. Поскольку волосковые клетки у людей плохо восстанавливаются, их потеря приводит к постоянным нарушениям слуха. Показав, что подавление IFI27 может смягчить этот разрушительный каскад в человеческих клетках, исследование выделяет IFI27 как перспективную мишень для лекарственных или генетических вмешательств. Хотя такие подходы пока далеки от клиники — и, вероятно, потребуют очень ранней доставки — эта работа предлагает конкретную молекулярную дорожную карту для превращения ранее загадочной генетической мутации в потенциально предотвратимую причину детской глухоты.
Цитирование: Chen, Y., Zhao, P., Lin, Q. et al. GJB2 c.109G > A mutation activating IFI27-mediated mitochondrial apoptosis pathway leading to hereditary non-syndromic hearing loss. Sci Rep 16, 6240 (2026). https://doi.org/10.1038/s41598-026-37393-2
Ключевые слова: наследственная тугоухость, мутация GJB2, модель на данио, митохондриальный апоптоз, IFI27