Clear Sky Science · ru
Эффективный апоптоз через двойные разрывы ДНК в эпителиальных клетках человека, индуцируемый нетермическим эффектом широкополосных терахерцовых волн высоких полей
Новый свет на уничтожение раковых клеток
Лечение рака часто балансирует на тонкой грани: нужно уничтожить опухолевые клетки, не причиняя серьёзного вреда здоровой ткани и иммунной системе. В этом исследовании рассматривается необычный инструмент для этой задачи — интенсивные терахерцовые (THz) волны, вид невидимого излучения между микроволнами и инфракрасным диапазоном. Авторы демонстрируют, что тщательно настроенные импульсы THz высокого поля могут заставлять раковые клетки «совершать самоубийство» контролируемым образом, не перегревая ткань и не вызывая грубых форм гибели клеток, ведущих к воспалению.
Почему важна аккуратная гибель клеток
Многие распространённые методы борьбы с раком направляют клетки к гибели, но часто при этом наносят сопутствующий ущерб. Лекарства и биологические агенты могут терять эффективность по мере развития резистентности опухолей и ослаблять иммунную систему. Физические методы, такие как рентген, радиоактивность или термическая абляция, могут повредить соседние здоровые ткани, часто вызывая некроз — агрессивную форму смерти клетки, которая провоцирует воспаление и боль. Метод, который вместо этого вызывает апоптоз — аккуратный процесс самодеструкции, при котором клетка тихо распадается — мог бы обеспечить гораздо менее травматичный способ уменьшения опухолей, особенно расположенных близко к коже.
Терахерцовые волны и клетки рака молочной железы
Группа сосредоточилась на человеческих клетках рака молочной железы (MCF‑7), типе эпителиальных клеток, часто используемых в лабораторных исследованиях. Эти клетки подвергали воздействию очень сильных широкополосных импульсов THz до четырёх часов при поддержании нормальной телесной температуры. Интенсивности поля достигали нескольких миллионов вольт на сантиметр, что намного больше, чем в бытовых устройствах. При таких условиях доля клеток, вступивших в апоптоз, неуклонно увеличивалась с временем облучения. При максимальной проверенной интенсивности THz почти 99% раковых клеток вошли в апоптоз, тогда как менее 1% погибло от некроза. Эта массивная, чистая волна программируемой гибели клеток указывает на то, что импульсы THz действуют не только путём нагрева клеток.
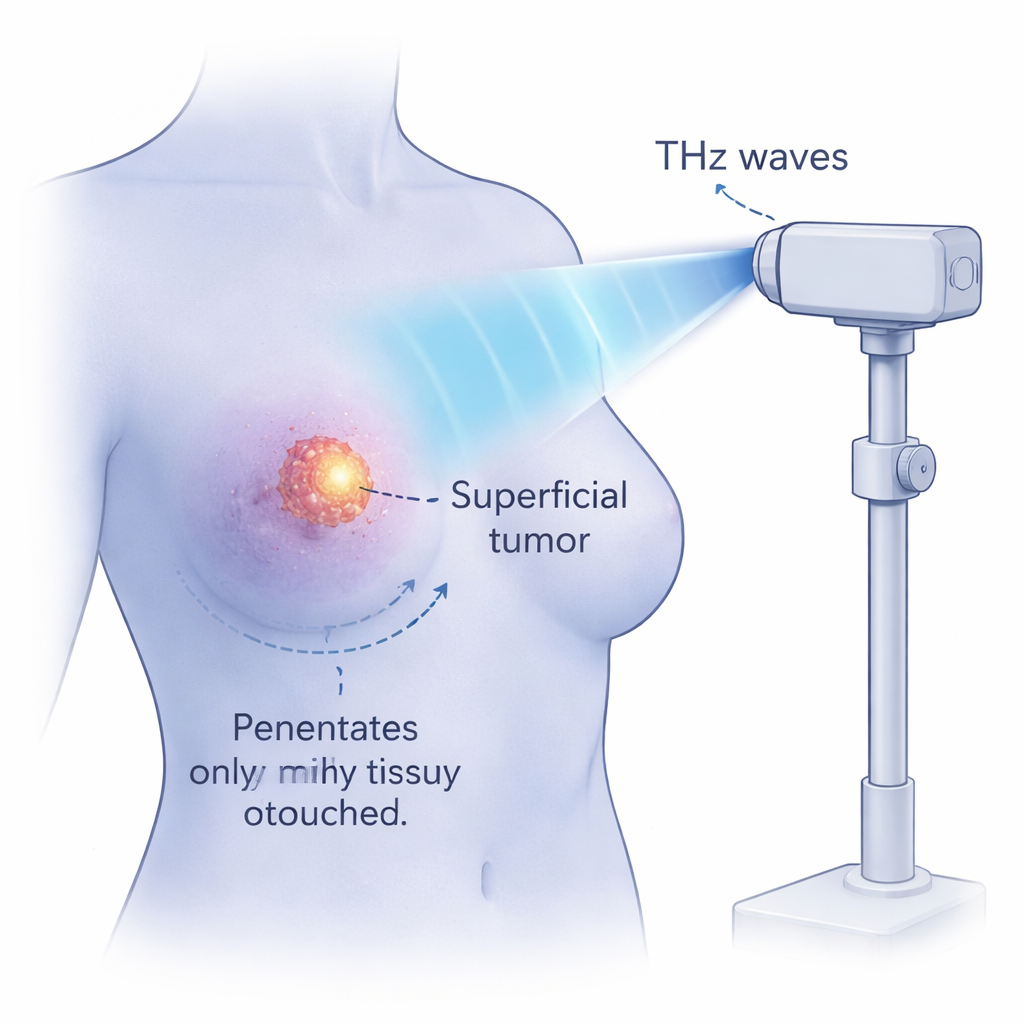
Нетермические эффекты и безопасные температурные пределы
Поскольку вода сильно поглощает THz-излучение, очевидной проблемой было случайное нагревание. Учёные использовали тепловизионную съёмку для отслеживания изменений температуры во время облучения. Даже после четырёх часов при умеренной интенсивности клетки нагрелись всего примерно на 3 °C, и доля некроза оставалась ниже 4%. В отдельных контрольных экспериментах, в которых клетки просто нагревали в течение четырёх часов, температуры ниже 41 °C вызывали почти никакой гибели, в то время как резкий рост некроза наблюдался выше 43 °C. Даже при самых интенсивных настройках THz исследователи держали температуру клеток на уровне не выше этого порога в 43 °C и при этом наблюдали почти полный апоптоз с минимальным некрозом. Понизив частоту повторения импульсов, они показали, что температуру можно контролировать, сохраняя при этом сильный противоопухолевый эффект, что подчёркивает наличие нетермического механизма действия.
Разрыв ДНК и включение генов смерти
Чтобы выяснить этот механизм, команда заглянула внутрь клеток. Под электронным микроскопом обработанные THz клетки показывали классические ранние признаки апоптоза: конденсированную генетическую материю, изменённые ядра и неповреждённые внешние мембраны. С помощью флуоресцентного маркера γ‑H2AX они обнаружили обширные двойные разрывы в ДНК — повреждения, которые были значительно чаще в облучённых клетках, чем в необработанных или слегка нагретых контролях. Картина повреждений соответствовала профилю интенсивности THz‑луча, усиливаясь к его центру. Анализ генов и белков показал сильную активацию набора молекул, реагирующих на стресс и повреждение, таких как GADD45B и c‑Jun, в то время как известные участники классических путей гибели клеток, включая p53 и многие каспазы, значительно не менялись. Авторы предполагают, что интенсивные поля THz могут вызывать сильные вибрационные «резонансы» в ДНК, физически нагружая и разрывая двойную спираль, а затем запускают отдельный путь апоптоза, независимый от p53 и каспаз.
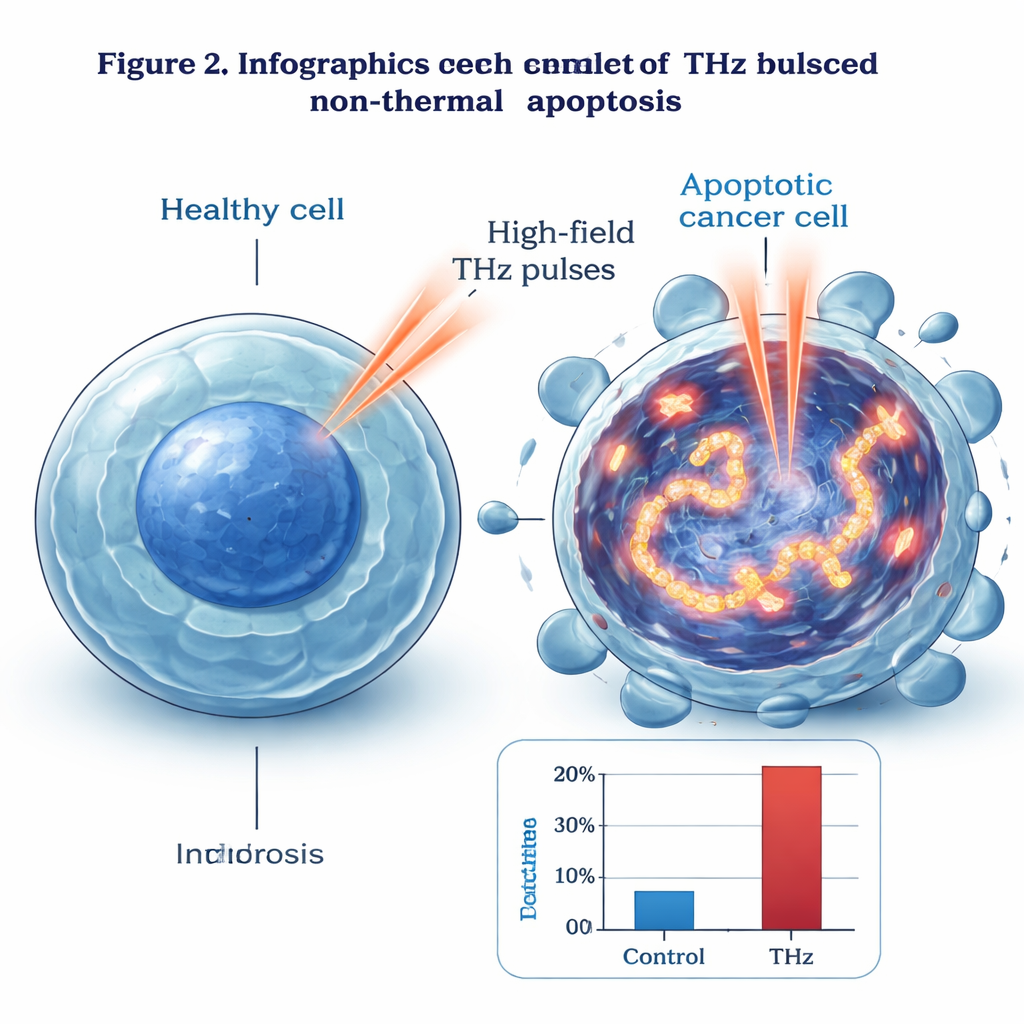
От чашки Петри к будущим терапиям
Хотя эти эксперименты проведены в культурах клеток, они намекают на новый подход к физической терапии рака. Терахерцовые волны высокого поля, по-видимому, способны проникать на несколько миллиметров в увлажнённую ткань — достаточно, чтобы достичь поверхностных опухолей — но быстро теряют мощность, возможно, щадя более глубокие органы. Поскольку эффект в основном нетермический, он теоретически мог бы уничтожать раковые клетки слой за слоем без прижигания окружающей ткани или вызова сильного воспаления. Остаётся много работы: предложенный механизм «резонанса» ДНК нужно подтвердить, безопасность для нормальных клеток тщательно проверить, а также провести исследования на животных и клинические испытания. Тем не менее это исследование открывает идею о том, что тщательно настроенные световые импульсы, резонирующие с естественными движениями биомолекул, однажды могут дать точный и относительно щадящий способ абляции некоторых видов рака.
Цитирование: Zhou, H., Wei, X., Peng, XY. et al. Efficient apoptosis via double-strand breaks of DNA in human epithelial cells induced by non-thermal effect of high-field broadband terahertz waves. Sci Rep 16, 6163 (2026). https://doi.org/10.1038/s41598-026-37373-6
Ключевые слова: терагерцовая терапия рака, нетермический апоптоз, двойные разрывы ДНК, клетки рака молочной железы, физическое удаление опухоли