Clear Sky Science · ru
Таргетирование оси Akt–EphA2 и клеточно‑клеточной адгезии повышает чувствительность к анойкису у раковых клеток
Почему важны свободно плавающие раковые клетки
Когда раковые клетки отрываются от опухоли и путешествуют по кровотоку, они в норме должны гибнуть, поскольку теряют опору на окружающую ткань. Эта встроенная защитная программа, называемая гибелью клетки, вызванной отделением, помогает не допускать роста тканей в неподходящих местах. Метастатические раковые клетки, однако, часто учатся игнорировать этот сигнал и сохранять жизнеспособность в состоянии «плавания», что облегчает им образование новых опухолей. В этом исследовании поставлен на первый взгляд простой вопрос: если мы восстановим ключевое механическое «ощущение прикосновения» в агрессивных клетках рака молочной железы, удастся ли нам заставить эти блуждающие клетки погибнуть, а если нет — какие запасные приемы они используют, чтобы выжить?
Пробуждение утраченного осязания
Клетки постоянно проверяют жесткость окружения, тянув структуры, которые их закрепляют. В здоровой ткани потеря контакта или посадка на очень мягкую поверхность, как правило, запускает самоуничтожение. Белок тропомиозин 2.1 (Tpm2.1) — важная часть этого внутреннего механизма натяжения и зачастую отсутствует или снижен в опухолевых клетках. Исследователи использовали широко изученную метастатическую линию клеток рака молочной железы и генетически модифицировали её так, чтобы она синтезировала больше Tpm2.1, восстановив значительную часть оценки жесткости. Когда эти модифицированные клетки выращивали в специальных нелипких чашках, предотвращающих прикрепление, они действительно испытывали больше гибели клеток, росли медленнее и меньше мигрировали по сравнению с немодифицированными раковыми клетками. Тем не менее даже после нескольких дней в суспензии примерно 70% клеток, экспрессировавших Tpm2.1, оставались живыми, что говорит о том, что простое восстановление осязания не полностью решает проблему.
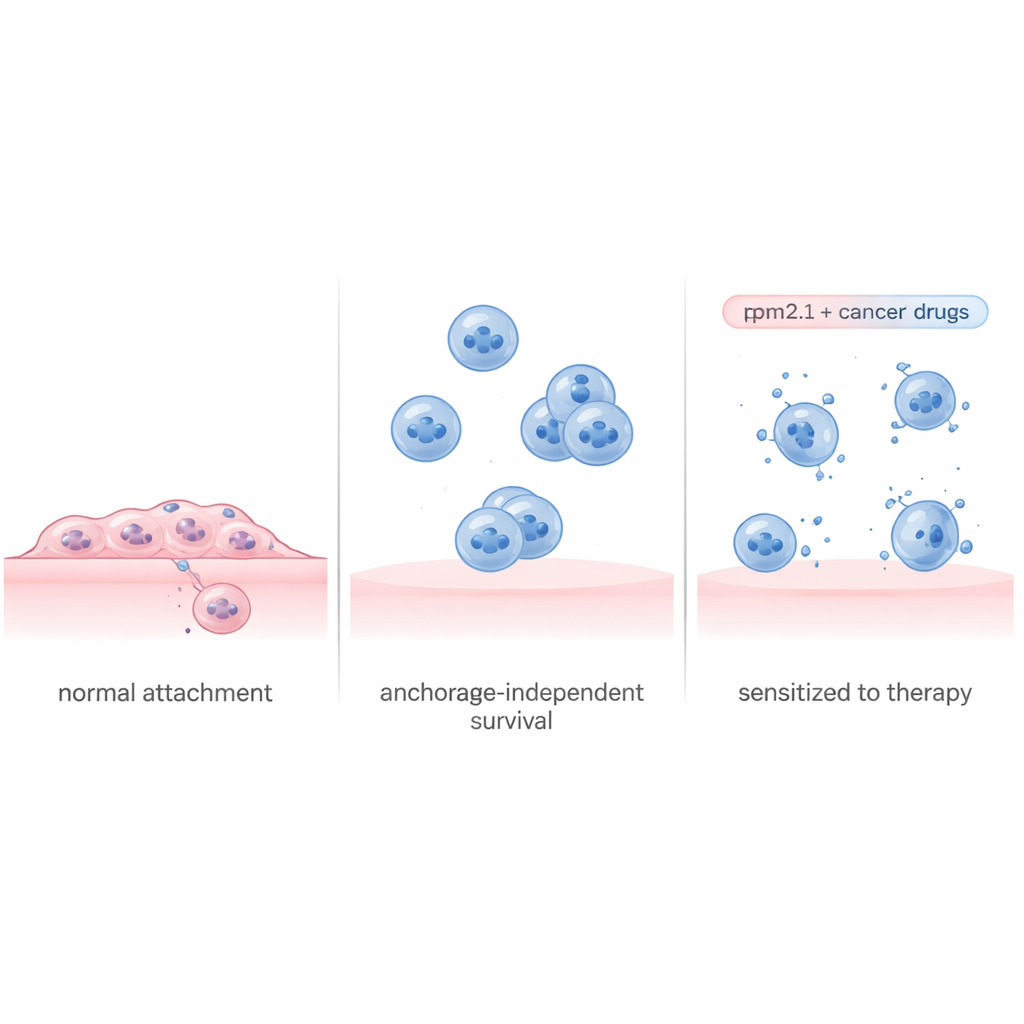
Чтение пособия по выживанию раковых клеток
Чтобы понять, почему одни клетки гибнут, а другие выживают, команда разделила плавающие клетки, экспрессирующие Tpm2.1, на две группы: те, которые показывали ранние признаки гибели, и те, которые выглядели здоровыми. Затем они измеряли, какие гены включены или выключены в каждой группе в течение четырех дней. У гибнущих клеток наблюдалось широкое подавление программ, связанных с делением клеток, репарацией ДНК и прикреплением, а также стрессовые сигналы, указывающие на необратимый путь к самоуничтожению. Напротив, выжившие клетки активировали скоординированный план выживания. Рано после отделения они включали воспалительные и иммунные пути, а позже усиливали крупные сигнальные каскады роста и выживания, включая хорошо известный путь, центром которого является белок Akt. Одновременно они сильно усиливали экспрессию генов, способствующих сцеплению клеток друг с другом, что позволило им образовывать защитные кластеры даже без опоры на внеклеточный матрикс.
Сила в числе: как клеточные кластеры сопротивляются гибели
Поскольку данные экспрессии генов указывали на повышенную клеточно‑клеточную адгезию, исследователи проверили, может ли простая скученность помогать клеткам выживать в суспензии. Когда клетки, экспрессирующие Tpm2.1, выращивали в высокой плотности, что облегчало образование кластеров, гораздо меньше клеток погибало по сравнению с редкой посевкой. Один из молекул адгезии, ICAM1, выделился как особенно повышенный в выживших клетках — известно, что он помогает образованию кластеров циркулирующих опухолевых клеток и их оседанию в отдаленных тканях. Блокирование ICAM1 с помощью маломолекулярного ингибитора увеличивало гибель клеток, экспрессирующих Tpm2.1, в суспензии, тогда как в стандартных прикрепленных кульутрах эффект был незначителен. Эти результаты поддерживают идею о том, что, даже частично восстановив внутреннюю механику, раковые клетки все еще могут избежать гибели, буквально удерживаясь друг за друга, а не за окружение.
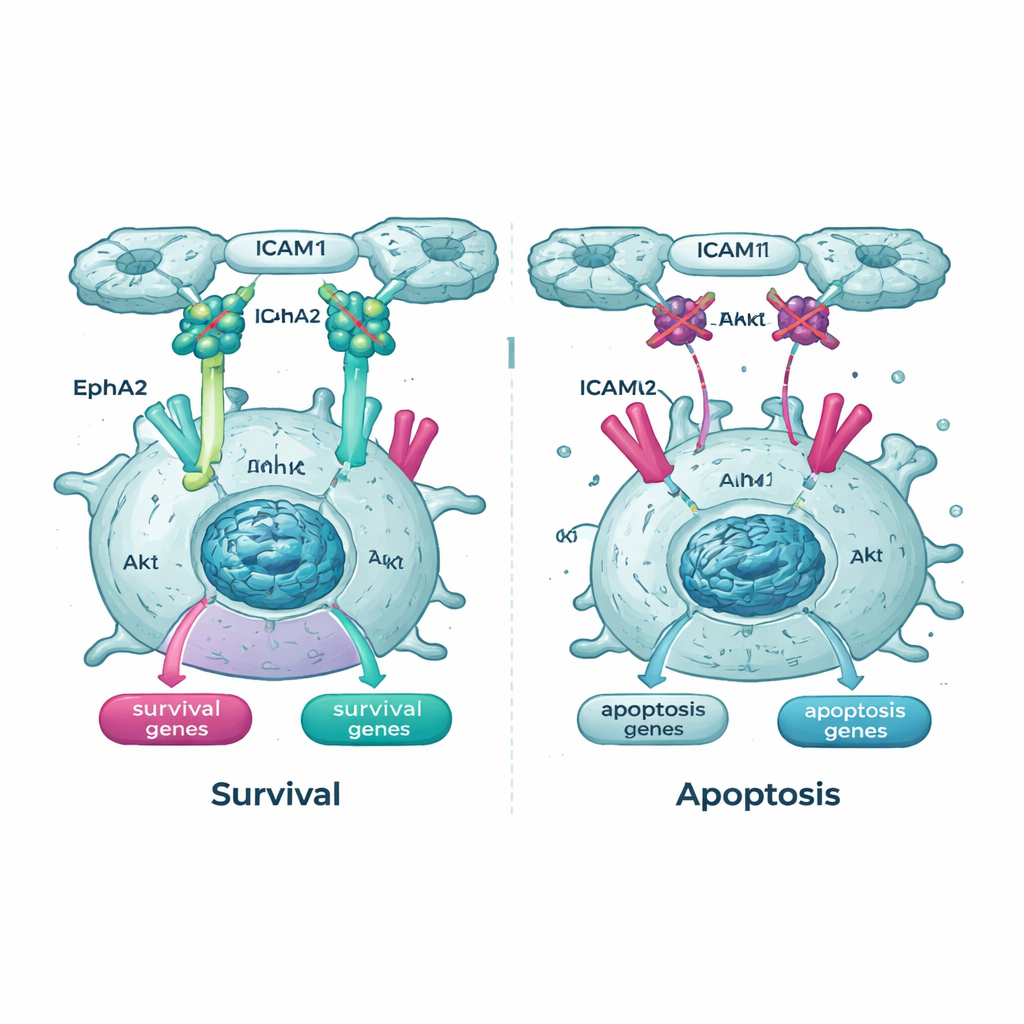
Перекрывая ключевые жизнеобеспечивающие цепи внутри клетки
Генетические исследования также выделили путь Akt и одного из его партнеров, рецептор EphA2, как важные линии жизнеобеспечения для клеток в суспензии. В клетках, экспрессирующих Tpm2.1, активная, фосфорилированная форма Akt была ниже в суспензии по сравнению с контрольными клетками, а уровни и активность EphA2 также были снижены. Когда команда обрабатывала клетки препаратами, блокирующими Akt или EphA2, как обычные, так и экспрессирующие Tpm2.1 раковые клетки становились значительно более склонными к гибели в суспензии. Примечательно, что клетки с восстановленным механизмом оценки жесткости были особенно чувствительны к этим препаратам со временем, что подразумевает: частичное повторное включение механических контрольных точек делает их более зависимыми от оставшихся сигналов выживания.
Преобразование подготовленного состояния в леткую слабость
Для неспециалиста ключевое послание таково: восстановление одного сломанного предохранителя в раковых клетках — их способности ощущать и реагировать на потерю контакта — необходимо, но недостаточно, чтобы заставить их саморазрушиться. Клетки, которые выживают, делают это, собираясь в кластеры и перенаправляя внутренние сигнальные пути через альтернативные пути роста и выживания. Эта работа показывает, что восстановление оценки жесткости с помощью Tpm2.1 переводит метастатические клетки рака молочной железы в «подготовленное» состояние, в котором они ближе к смерти, но еще не обречены. Последующее блокирование пути Akt–EphA2 и нарушение клеточно‑клеточной адгезии через ICAM1 позволяет исследователям подтолкнуть эти подготовленные клетки через грань и значительно увеличить гибель, вызванную отделением. В практическом плане исследование представляет стратегию для будущих комбинированных терапий, направленных на уничтожение свободно плавающих опухолевых клеток до того, как они смогут посеять новые метастазы.
Цитирование: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
Ключевые слова: метастазирование рака молочной железы, клеточная адгезия, анойкис, сигнализация Akt, оценка жесткости