Clear Sky Science · ru
Влияние определённой микробиоты Oligo-MM12 на кишечную колонизацию и распространение Listeria monocytogenes
Почему микробы в вашем кишечнике имеют значение
Многие знают Listeria monocytogenes как опасный пищевой патоген, связанный с заражёнными продуктами готовыми к употреблению и тяжёлыми заболеваниями у уязвимых людей. Менее очевидно то, что способность этой бактерии закрепиться в организме зависит не только от нашей иммунной системы, но и от бурлящего сообщества микробов, уже обитающих в кишечнике. В этом исследовании используются специально разработанные модели на мышах и миниатюрный «искусственный толстый кишечник», чтобы ответить на простой, но важный вопрос: как сложность микробиоты кишечника влияет на способность Listeria колонизовать кишечник и распространяться по организму?
История двух микробных «районов»
Для решения этого вопроса исследователи сравнили два типа мышей. Одна группа, называемая SPF-мышами, несла богатую, естественную смесь кишечных бактерий, аналогичную той, что встречается у многих лабораторных животных. Другая группа, мыши Oligo-MM12, была населена куда более простой общиной, состоящей всего из 12 хорошо охарактеризованных бактериальных штаммов. Поскольку каждый член этой коллекции известен и стабилен из поколения в поколение, мыши Oligo-MM12 представляют собой мощный инструмент для выяснения, какие микробы помогают блокировать захватчиков, а какие могут оставлять пробелы в нашей защите. Сравнивая эти мыши, команда могла проверить, чем плотная, разнообразная экосистема кишечника отличается от упрощённой, минималистичной при ответе на инфекционное испытание.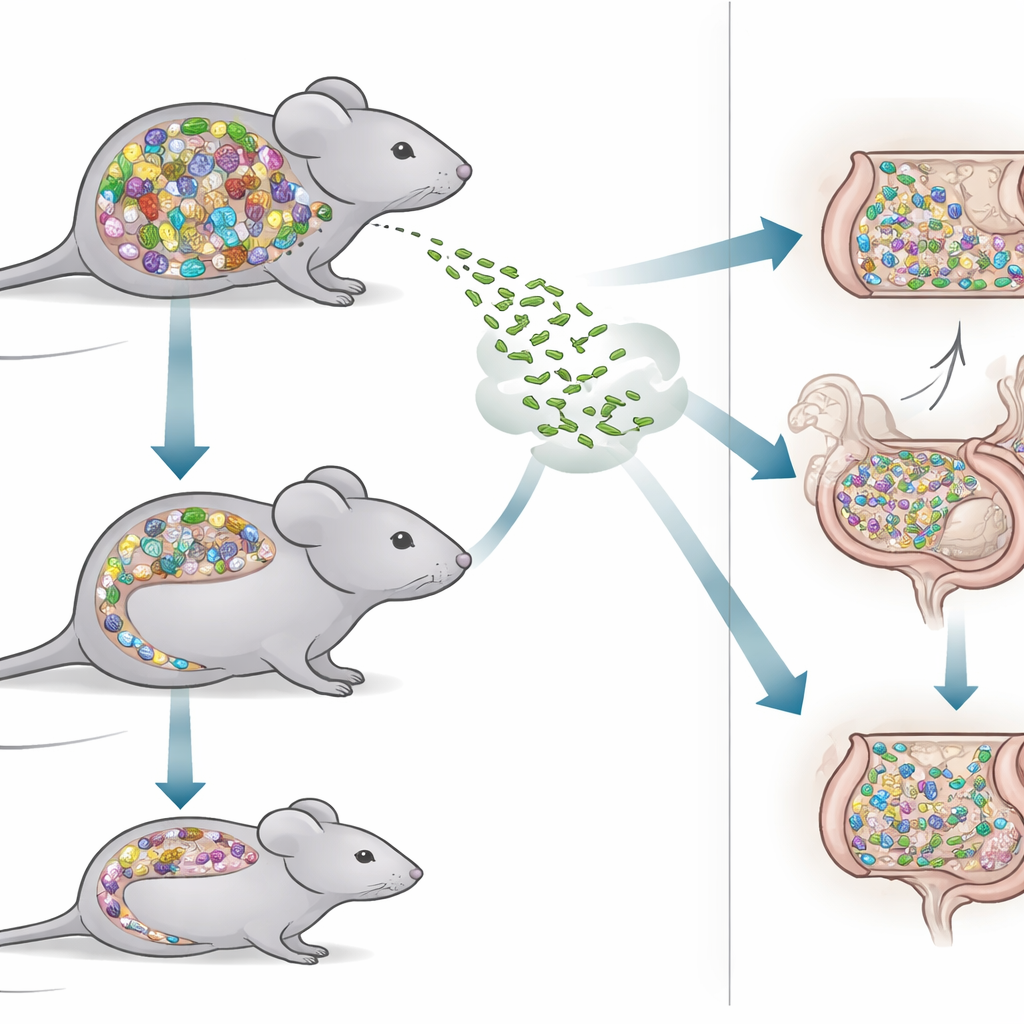
Прослеживание Listeria через кишечник и дальше
Учёные инфицировали оба типа мышей одинаковой пероральной дозой Listeria и вели подсчёт бактерий в фекалиях и внутренних органах в течение трёх дней. Любопытно, что более простая община Oligo-MM12 поначалу казалась лучше сдерживающей Listeria: в первый день после инфекции эти мыши выделяли меньше клеток Listeria в стуле, чем SPF-мыши. Однако это раннее преимущество исчезло. На третий день мыши Oligo-MM12 выделяли больше Listeria, тогда как у SPF-мышей количество бактерий стабильно снижалось. Несмотря на явные различия в кишечнике, количества Listeria во внутренних органах, таких как печень, селезёнка и лимфатические узлы, были похожи между двумя моделями мышей, что указывает на то, что когда Listeria достигает глубинных тканей, сложность микробиоты играет меньшую роль.
Моделирование толстого кишечника в контролируемой коробке
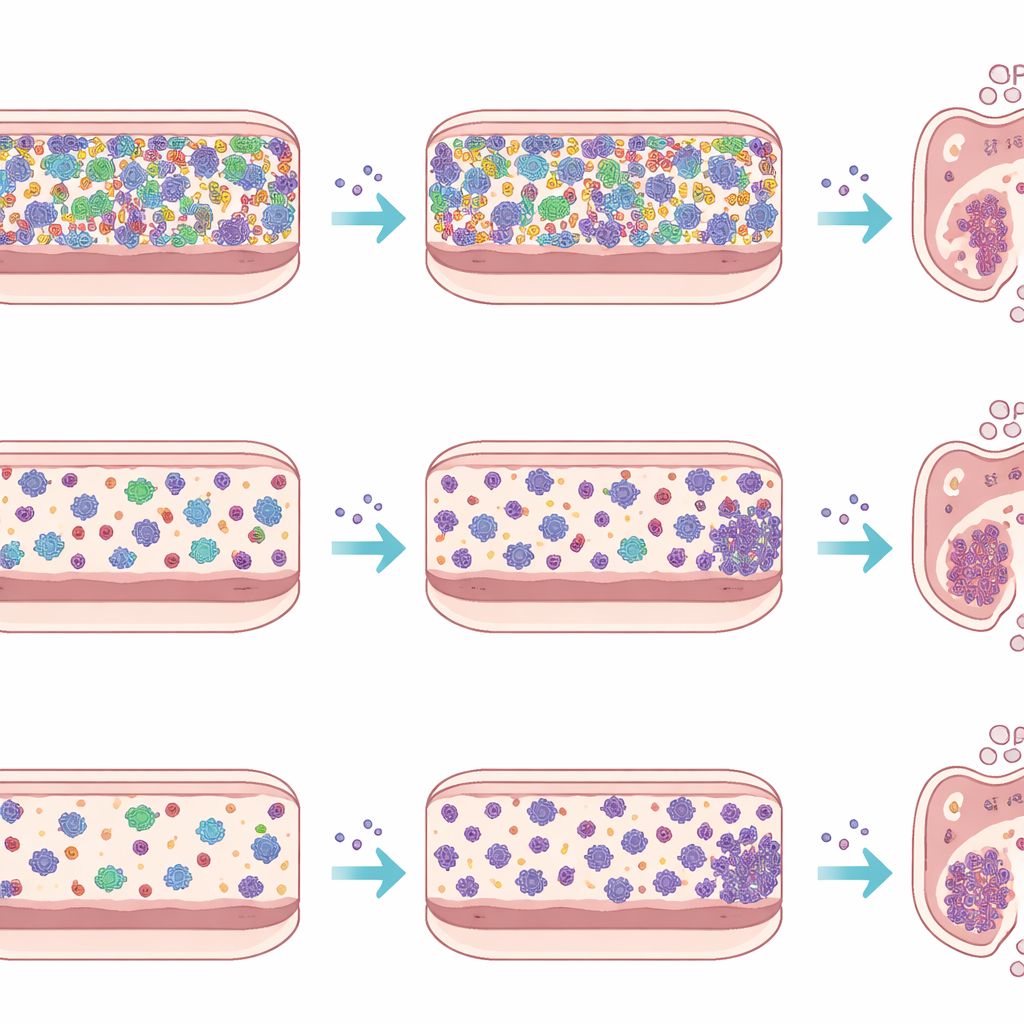
Чтобы отделить влияние тканей хозяина и иммунитета от поведения самих микробов, команда также провела ex vivo эксперимент с использованием устройства micro-Matrix биореактора. Они приготовили фекальные суспензии от каждого типа мышей, добавили их в питательную среду в герметичных бескислородных лунках и внесли Listeria в некоторые из этих миниатюрных культур, оставив другие в качестве контроля. В течение пяти дней измеряли количество Listeria и секвенировали бактериальную ДНК, чтобы проследить, как сообщества эволюционируют. В этом искусственном толстом кишечнике Listeria выросла до схожих уровней независимо от того, сталкивалась ли она со сложной микробиотой SPF или с более простой общиной Oligo-MM12, и её присутствие вызвало лишь скромные сдвиги в общей композиции сообществ. Это отличие от экспериментов на живых животных подчёркивает, насколько сильно иммунная система, слизистая кишечника, желчные и слизевые потоки формируют динамику инфекции в реальном кишечнике.
Ключевые микробные победители, проигравшие и наблюдатели
Рассматривая, какие бактериальные группы возрастали или уменьшались во время инфекции, исследование выделяет кандидатов, способных влиять на успех Listeria. У мышей Oligo-MM12 уровни Akkermansia, бактерии, связанной со слизью и часто ассоциируемой со здоровьем кишечника, упали на второй день, а затем сильно восстановились к третьему дню. У SPF-мышей несколько родов, известных производством полезных метаболитов или поддержкой барьерной целостности, таких как Blautia и Bacteroides, снижались в ходе инфекции, в то время как некоторые бактерии, похожие на Prevotella, демонстрировали сложные подъёмы и падения, которые могут отражать прямое воздействие антимикробных соединений самой Listeria. Ex vivo эти закономерности в основном были приглушены, что усиливает идею о том, что многие наблюдаемые сдвиги возникают из трёхсторонних взаимодействий между патогеном, резидентными микробами и средой хозяина, а не только из простой конкуренции микроорганизмов между собой.
Что это означает для защиты людей
Для неспециалистов главный вывод состоит в том, что не все внешне «здоровые» микробиомы защищают от инфекции одинаково, и что «большее разнообразие» не всегда лучше в каждый момент. Упрощённая община Oligo-MM12 обеспечивала сильную раннюю резистентность к Listeria в кишечнике, но с течением времени более сложная микробиота SPF лучше справлялась с удалением захватчика. Работа показывает, что тщательно сконструированные модели микробиоты низкой сложности в сочетании с управляемыми ex vivo системами могут выявлять, какие бактериальные группы и экологические факторы критичны для блокирования опасных пищевых патогенов. В конечном счёте такие знания могут помочь в создании таргетных пробиотиков или терапий, основанных на микробиоме, которые укрепляют правильных микробных союзников в нужное время для предотвращения тяжёлых инфекций Listeria у групп риска.
Цитирование: Cazzaniga, M., Bra, K.K., Herzog, M.K.M. et al. Impact of the defined Oligo-MM12 microbiota on intestinal colonisation and dissemination of Listeria monocytogenes. Sci Rep 16, 8434 (2026). https://doi.org/10.1038/s41598-026-37294-4
Ключевые слова: Инфекция Listeria, микробиом кишечника, резистентность к колонизации, модель на мышах, пробиотики