Clear Sky Science · ru
Комплексный анализ глобальных регуляторов и генов эффлюкса, связанных с отменой устойчивости к антибиотикам у множественной лекарственно‑устойчивой Klebsiella pneumoniae
Почему эти внутрибольничные микрообы настолько трудно уничтожить
В больницах по всему миру некоторые штаммы бактерии Klebsiella pneumoniae стали печально известны своей плохо поддающейся терапии. Они отталкивают несколько антибиотиков, которые раньше работали надежно, превращая рутинные инфекции в опасные для жизни состояния. Это исследование заглядывает под микробный капот, чтобы понять один важный прием, который используют эти бактерии: микроскопические насосы, выплевывающие антибиотики наружу из клетки, и генетические переключатели, которые, по‑видимому, регулируют активность этих насосов.
Супермикробы и их молекулярные пожарные люки
Множественная лекарственная устойчивость Klebsiella pneumoniae теперь встречается во многих больницах, включая и иракский медицинский центр, где проводилось это исследование. Эти бактерии могут выдерживать несколько крупных семейств антибиотиков одновременно, таких как фторхинолоны, аминогликозиды и цефалоспорины третьего поколения. Один из способов достижения этого — установка мощных «насосов выведения» в оболочку клетки. Среди наиболее значимых — система AcrAB‑TolC, которая проходит через бактериальные мембраны и работает как крошечный дренажный насос, захватывая молекулы антибиотика внутри клетки и выталкивая их наружу до того, как препараты смогут причинить серьёзный вред. Когда эти насосы очень активны, концентрация антибиотика внутри бактерии никогда не достигает летального уровня.
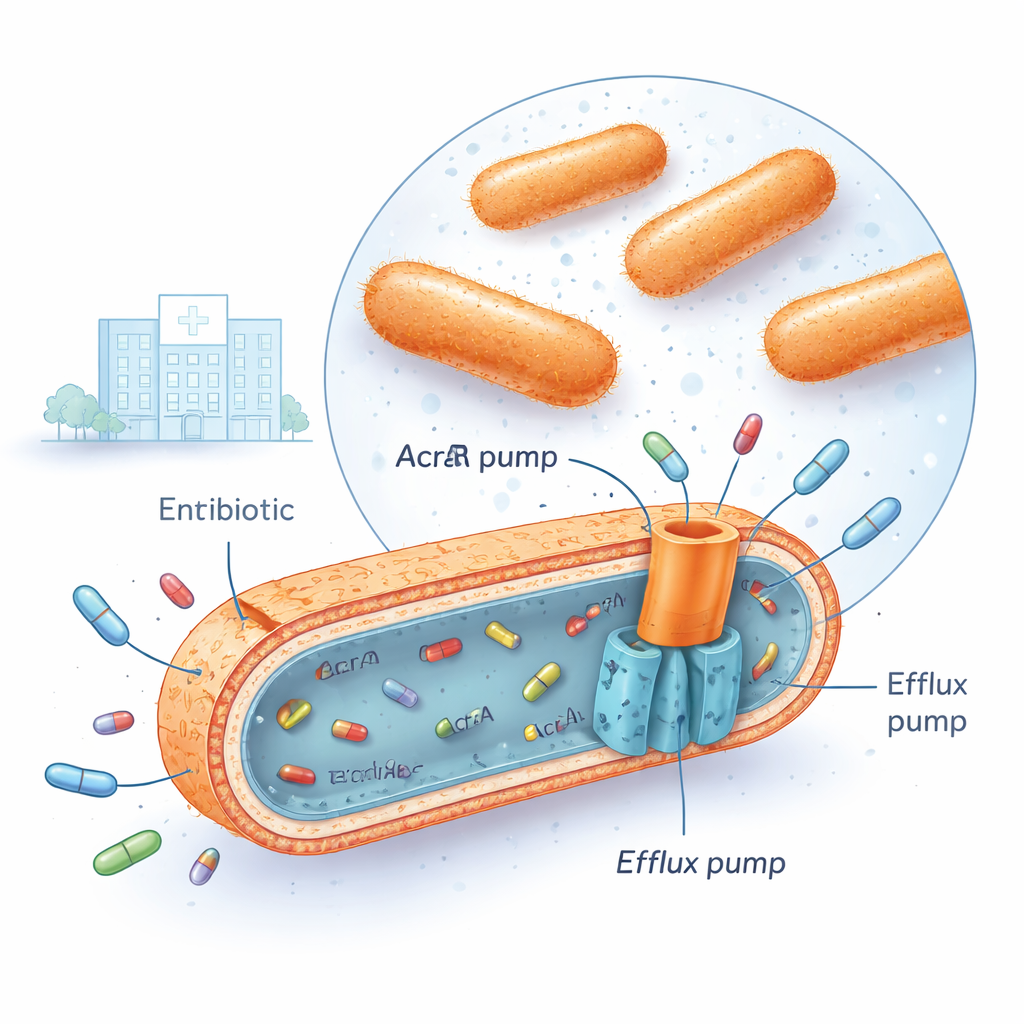
Генетические переключатели, сопутствующие перегрузке насосов
Исследователи собрали 30 клинических изолятов Klebsiella pneumoniae с множественной лекарственной устойчивостью и сравнили их с 10 чувствительными к антибиотикам изолятами и стандартным референтным штаммом. С помощью метода количественной ПЦР в реальном времени они измеряли, насколько активно включены определённые гены. В центре внимания были три «глобальных регулятора» — гены marA, soxS и rob — а также три компонента насоса AcrAB‑TolC (acrA, acrB и tolC). В устойчивых штаммах два регулятора, marA и soxS, как правило, были повышены примерно в четыре‑пять раз по сравнению с чувствительными бактериями, тогда как acrB, центральный компонент насоса, был усилен почти в восемь раз. Статистический анализ показал, что при высоких уровнях marA и soxS уровни acrB обычно тоже были высоки, и такие штаммы выдерживали значительно большие дозы фторхинолонов, например ципрофлоксацина. Третий регулятор, rob, менялся мало и не коррелировал с активностью насоса, что указывает на его меньшую роль в изученных условиях.
Выключение насосов для ослабления устойчивости
Нахождение одновременной активности генов насосов и регуляторов является наводящим на мысль, но недостаточно, чтобы доказать их причинную роль в устойчивости. Чтобы проверить функциональное значение насосов, команда использовала химическое средство PAβN. Это соединение не применяется как лекарство у пациентов, но в лабораторных условиях оно может заглушать насосы, подобные AcrAB‑TolC, и препятствовать их способности выталкивать антибиотики. Учёные выбрали десять устойчивых изолятов с особенно высокими уровнями гена acrB и измерили, какая концентрация ципрофлоксацина требуется для прекращения их роста с PAβN и без него. У восьми из этих десяти штаммов блокирование насоса снижало требуемую дозу ципрофлоксацина как минимум в четыре раза, а иногда до шестнадцати раз. Это падение демонстрирует, что во многих из этих супермикробов активные насосы выведения действительно являются основной причиной их способности переносить высокие дозы антибиотиков.
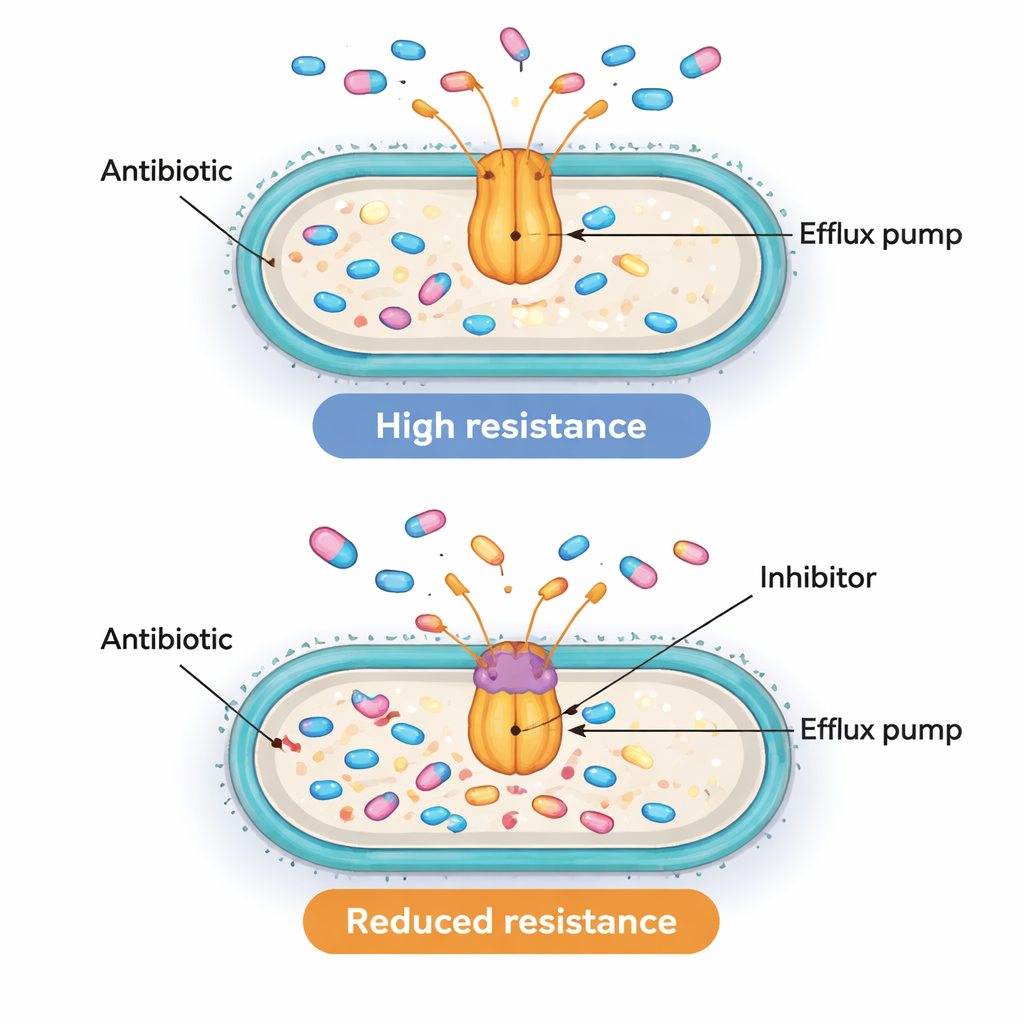
Сложная головоломка устойчивости с перспективными целями
Не все штаммы вели себя одинаково. Некоторые бактерии с сильно экспрессируемыми генами насосов лишь частично восстанавливали чувствительность при блокировании насосов, что подразумевает, что иные пути устойчивости — такие как изменения в мишени антибиотика внутри клетки, выработка разрушающих лекарство ферментов или альтернативные насосы — также вносят вклад. Например, гентамицин, аминогликозидный антибиотик, в значительной мере оставался не затронутым закономерностями, наблюдаемыми для генов marA/soxS и AcrAB‑TolC, подчёркивая, что множественная лекарственная устойчивость обычно складывается из нескольких перекрывающихся механизмов, а не одного единственного.
Что это значит для будущего лечения
Для неспециалистов ключевой вывод таков: некоторые внутрибольничные бактерии могут выживать при воздействии антибиотиков не только путём блокировки или разрушения препаратов, но и активным их выбрасыванием. В этом исследовании повышенная активность двух генетических «переключателей», MarA и SoxS, связана с более активными насосами выведения и более сильной устойчивостью к широко используемому классу антибиотиков. Когда насосы экспериментально блокируются, многие из этих бактерий становятся по крайней мере частично чувствительными снова. Хотя работа ещё не доказывает точно, как эти переключатели контролируют насосы, она выделяет как регуляторы, так и сами насосы как привлекательные мишени. В долгосрочной перспективе сочетание традиционных антибиотиков с безопасными блокаторами насосов — или препаратами, снижающими активность этих глобальных регуляторов — может помочь восстановить эффективность существующих методов лечения против иначе грозных инфекций с множественной лекарственной устойчивостью.
Цитирование: Obaid, A.J., Alkawaz, A.J. & Naser, M.S. Integrated analysis of global regulators and efflux genes associated with antimicrobial resistance reversal in multidrug resistant Klebsiella pneumoniae. Sci Rep 16, 7435 (2026). https://doi.org/10.1038/s41598-026-37272-w
Ключевые слова: устойчивость к антибиотикам, насосы выведения (эффлюкса), Klebsiella pneumoniae, фторхинолоны, обратимость устойчивости