Clear Sky Science · ru
Снижение активности деубиквитинирующего фермента USP10 коррелирует с апоптозом нейронов при миелопатии, связанной с HTLV-1
Почему это важно для людей с вирусными заболеваниями нервной системы
Некоторые вирусы вызывают не только кратковременные инфекции, но и на протяжении многих лет тихо повреждают нервную систему. Вирус Т‑клеточного лейкоза человека типа 1 (HTLV‑1) — один из таких вирусов; он может привести к хроническому заболеванию спинного мозга, называемому миелопатией, связанной с HTLV‑1 (HAM). У людей с HAM постепенно снижается сила и контроль в ногах, возникают проблемы с мочевым пузырём и нарушается чувствительность. Это исследование задаёт простой, но важный вопрос: почему нервные клетки спинного мозга погибают при этом состоянии, и может ли один защитный белок объяснить, кто переносит болезнь легче, а кто — хуже?
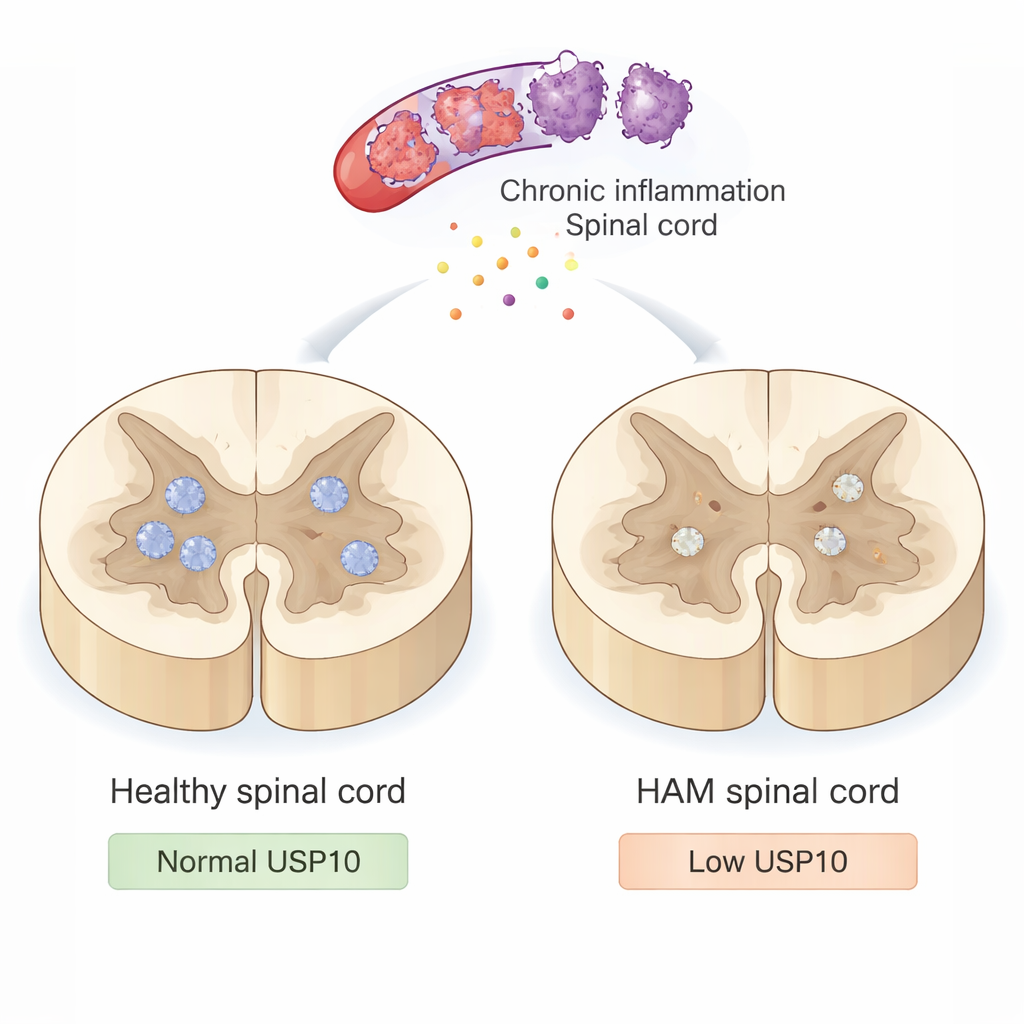
Медленная атака на спинной мозг
HAM возникает не из‑за прямой инфекции нервных клеток вирусом. HTLV‑1 инфицирует иммунные клетки, которые проникают в спинной мозг и вызывают длительное воспаление. Эти чрезмерно активные иммунные клетки выделяют токсичные вещества и провоспалительные сигналы, которые, пытаясь контролировать инфекцию, также повреждают соседние нейроны и их миелин. Со временем это тлеющее повреждение приводит к жёсткости и слабости ног и затруднениям при ходьбе. Тем не менее врачи до сих пор полностью не понимают, почему одни нейроны уступают воспалительной среде, а другие выживают десятилетиями.
Под подозрением — фермент «уборки» в клетке
Исследователи сосредоточились на белке USP10 — ферменте, который участвует в системе контроля качества белков в клетке и известен тем, что ограничивает клеточный стресс и программируемую гибель клеток (апоптоз). USP10 активен во многих тканях, включая мозг и спинной мозг, и предшествующие работы при болезни Паркинсона, инсульте и других состояниях указывают, что он помогает нейронам противостоять окислительному и воспалительному повреждению. Используя образцы спинного мозга от восьми людей, умерших с HAM, и двух неврологически здоровых контрольных образцов, команда применяла методы окрашивания, чтобы увидеть, где присутствует USP10 и насколько сильно он экспрессируется в нейронах.
Меньше USP10 — больше погибающих нейронов
В здоровом спинном мозге USP10 хорошо был заметен во многих нейронах. Однако в большинстве случаев HAM окрашивание на USP10 в нейронах было явно снижено, а у одного пациента оно почти отсутствовало. Затем учёные искали признаки апоптоза двумя методами: тестом TUNEL для обнаружения фрагментированной ДНК и окрашиванием на активный каспаз‑3 — белок, участвующий на ранних стадиях гибели клетки. В контрольных образцах практически не было нейронов с этими сигналами гибели. Напротив, у пациентов с HAM значительная доля нейронов оказалась TUNEL‑положительной, и многие проявляли активный каспаз‑3. Важно, что образцы с более низкой экспрессией USP10, как правило, содержали больше апоптотических нейронов и меньше выживших нейронов, помеченных NeuN — стандартным маркером нейронов. Один примечательный пациент с HAM, который спустя 22 года ещё мог передвигаться с тростью, имел высокую экспрессию USP10 и относительно сохранённое число нейронов, что намекает на то, что более высокий уровень USP10 может защищать от тяжёлой инвалидности.
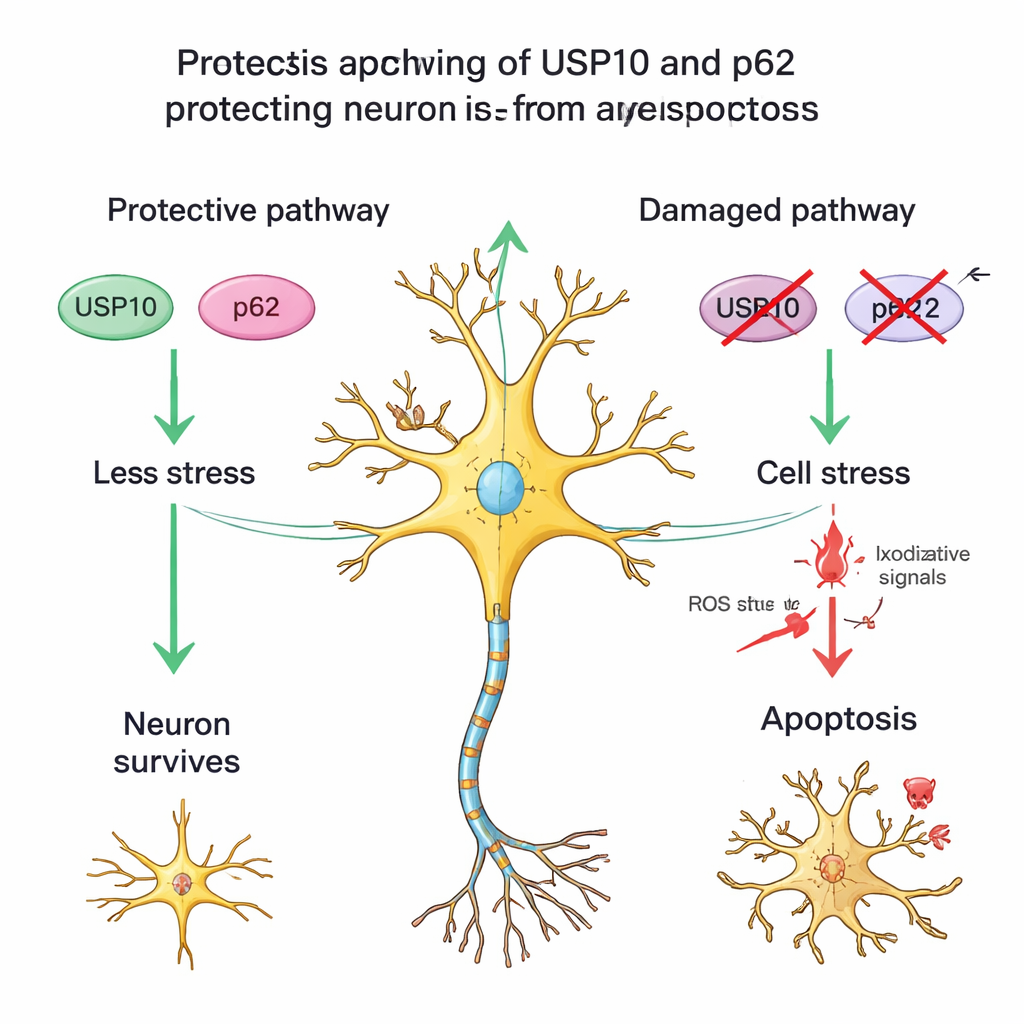
Сопутствующий белок и клетки под стрессом, но выжившие
Команда также изучала другой белок, p62, который работает с USP10 в обработке повреждённых белков и регулировании путей стресса и выживания. В здоровом спинном мозге окрашивание p62 было умеренным; среди пациентов с HAM те, у кого был низкий уровень USP10, часто также имели слабее выраженное p62 и меньше выживших нейронов. Этот паттерн поддерживает идею партнёрства USP10–p62, помогающего нейронам противостоять хроническому воспалению. Исследователи дополнительно заметили множество нейронов в тканях HAM, которые сохраняли типичную форму нервной клетки, но утратили окрашивание NeuN — признак, встречающийся при других повреждениях мозга, когда нейроны находятся под серьёзным стрессом, но ещё не полностью мертвы. Это указывает на то, что при HAM некоторые нейроны не только теряются полностью, но и другие остаются в повреждённом, уязвимом состоянии, возможно из‑за ослабления защит, связанных с USP10.
Что это может означать для будущей диагностики и лечения
Это исследование не доказывает, что потеря USP10 непосредственно вызывает гибель нейронов, поскольку оно основано на небольшом числе посмертных образцов и не позволяет проследить изменения во времени. Тем не менее последовательные связи между низким уровнем USP10, уменьшением p62, большим количеством признаков апоптоза и меньшим числом выживших нейронов указывают на общую цепь событий, которая может связывать хроническое воспаление и медленную нейрональную дегенерацию при HAM. Для пациентов это открывает обнадёживающую перспективу: измерение или усиление путей, связанных с USP10 в спинном мозге — или, возможно, в более доступных образцах, таких как спинномозговая жидкость — однажды может помочь выявлять тех, кто подвержен быстрому прогрессированию, направлять наблюдение или вдохновлять новые методы лечения, направленные на укрепление собственных систем защиты клетки при вирусных нейровоспалительных заболеваниях.
Цитирование: Arishima, S., Takahashi, M., Dozono, M. et al. Downregulation of the deubiquitinating enzyme USP10 correlates with neuronal apoptosis in HTLV-1-associated myelopathy. Sci Rep 16, 6062 (2026). https://doi.org/10.1038/s41598-026-37271-x
Ключевые слова: Миелопатия, связанная с HTLV-1, нейровоспаление, апоптоз нейронов, USP10, дегенерация спинного мозга