Clear Sky Science · ru
Визуализация внеклеточных биомолекул с помощью флуоресцентных белковых индикаторов с липид–PEG анкерами
Наблюдение за общением клеток в реальном времени
Наш мозг и тело зависят от постоянного химического диалога между клетками. Ионы и нейромедиаторы пересылают сообщения через крошечные промежутки, но эти быстрые и кратковременные сигналы трудно увидеть, не нарушив их. В этом исследовании предлагается простой способ «окрасить» живые клетки светящимися сенсорами, которые прикрепляются к их внешней поверхности, позволяя учёным наблюдать эти сообщения — особенно ионы калия и нейромедиатор глутамат — в реальном времени и с высокой детализацией. 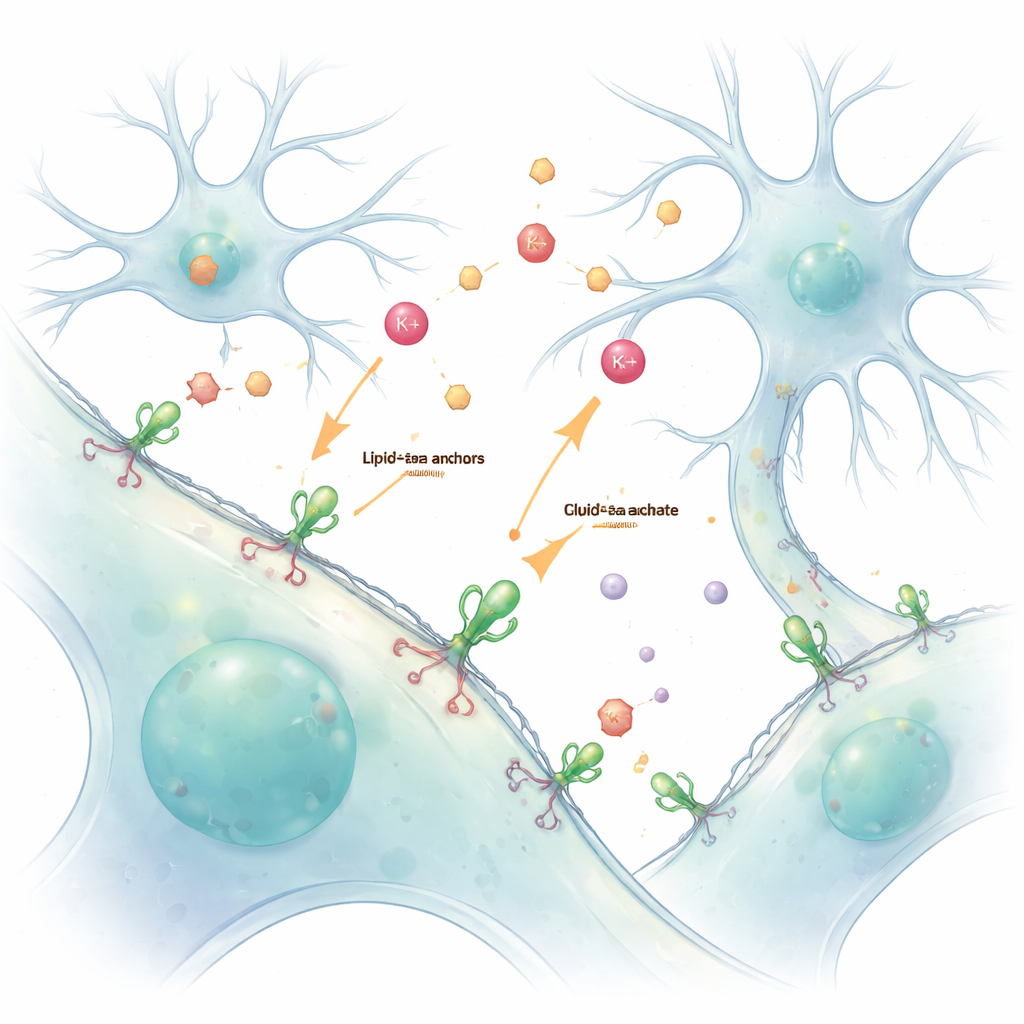
Новый способ пометить поверхность клетки
Традиционно исследователи заставляют клетки синтезировать флуоресцентные белковые сенсоры из собственной ДНК. Хотя этот генетический подход мощный, он часто приводит к тому, что сенсоры оказываются внутри клетки, и тогда трудно отделить происходящее внутри от событий снаружи. Авторы решили эту проблему, используя химическую «ручку» — липид–PEG анкер. Один конец этой молекулы внедряется в наружную мембрану, а другой химически связан с флуоресцентным белковым сенсором. Когда такие подготовленные сенсоры просто добавляют к живым клеткам, они самопроизвольно покрывают внешнюю поверхность, образуя стабильный светящийся слой, который сообщает о том, что происходит в окружающей жидкости.
Преобразование калия и глутамата в свет
Команда адаптировала два существующих флуоресцентных индикатора: GINKO2, реагирующий на ионы калия, и R-iGluSnFR1, реагирующий на глутамат. Белки очистили из бактерий и затем прикрепили к ним липид–PEG анкеры. В культивируемых клетках человека анкерный калиевый сенсор образовывал ровный контур по поверхности клетки и становился ярче при повышении внеклеточного калия, затем снова тускнел при падении уровней. Важно, что его световые характеристики и чувствительность в значительной степени совпадали с исходным, немодифицированным сенсором в пробирочных экспериментах, что показывает — анкеровка не снизила его эффективность. То же самое наблюдалось для глутаматного сенсора: после анкеровки он оставался чувствительным и чётко выделял глутамат в пространстве непосредственно у наружной поверхности клеток.
Прослушивание нейронов в культурах и срезах
Затем исследователи перешли к нервным клеткам из гиппокампа мыши — области мозга, важной для обучения и памяти. Они покрыли эти нейроны липид–PEG–анкерами глутаматного сенсора и загрузили внутренности тех же клеток отдельным красителем кальция, который сообщает об электрической активности. С помощью микроскопии полного внутреннего отражения они могли наблюдать красные вспышки глутамата на поверхности клетки, в то время как зелёные сигналы внутри клеток сообщали о спайках. Этот двухцветный режим показал, что анкерные сенсоры способны отслеживать спонтанный выброс нейромедиатора без какой‑либо генетической модификации самих нейронов.
Картирование химических волн по ткани мозга
Далее команда протестировала метод на острых срезах мозга, которые сохраняют естественную проводящую сеть гиппокампа. Они применили анкерный калиевый сенсор к срезам и электрически стимулировали нервные волокна. Анкерный сенсор давал чёткие, повторяемые увеличения флуоресценции после каждого стимула, тогда как неанкерные сенсоры быстро диффундировали и давали слабые, нестабильные сигналы. Купая срезы в растворах с известными концентрациями калия и корректируя данные с учётом собственной слабой флуоресценции ткани, авторы построили калибровочную кривую и оценили фактические внеклеточные концентрации калия. Базовый уровень составлял примерно 2,5 миллимоляр, а при умеренной стимуляции повышался до примерно 3,4 миллимоляр — в соответствии с классическими электродными измерениями. Анкерные сенсоры для калия и глутамата показали различную пространственную распространённость сигналов: изменения глутамата оставались близко к активным синапсам, тогда как повышения калия распространялись на сотни микрометров, указывая на более широкое влияние на возбудимость сети. 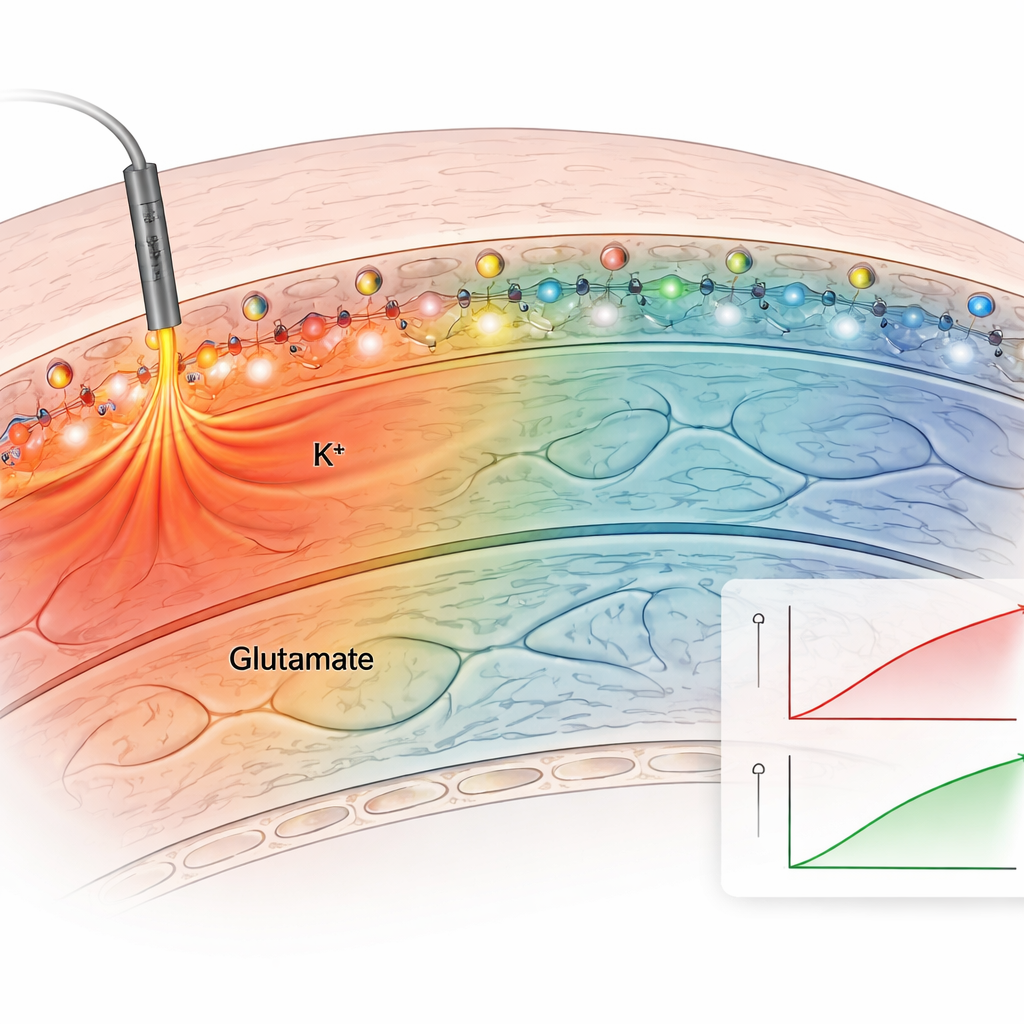
Изучение того, как мозг очищает и генерирует сигналы
Поскольку сенсоры закреплены на поверхности клетки, авторы могли разложить на составляющие процессы, формирующие эти внеклеточные волны. Блокирование транспортеров глутамата, которые обычно улавливают глутамат, вызывало у анкерного глутаматного сенсора более крупные и длительные сигналы, подтверждая, что локальный захват ограничивает распространение глутамата. Блокирование AMPA‑типных глутаматных рецепторов уменьшало как электрические ответы, так и калиевые сигналы, указывая на то, что большая часть подъёма калия происходит из постсинаптических нейронов, активированных синаптическим входом. Блокирование натриевых каналов тетродотоксином почти полностью устраняло калиевые изменения, связывая их непосредственно с потенциалами действия. Вместе эти эксперименты демонстрируют, как анкерные сенсоры могут превратить сложную распределённую химию в наглядные фильмы и карты.
Почему это важно для будущих исследований мозга
Для неспециалистов главное послание в том, что эта работа предлагает быстрый, негетерологичный (негенетический) способ покрыть живые клетки и ткани высокочувствительными молекулярными репортерами. Вместо того чтобы перенастраивать каждую клеточную линию генетически, учёные могут добавлять заранее приготовленные белковые сенсоры снаружи и немедленно визуализировать, как ионы и нейромедиаторы меняются в реальном времени на поверхности клетки. Такой подход улучшает контроль, воспроизводимость и пространственную точность, избегая сложностей доставки генов, особенно в деликатных препаратах вроде острых срезов мозга. По мере появления всё большего числа флуоресцентных индикаторов для разных химических веществ та же стратегия липид–PEG анкеровки может стать широко используемым набором инструментов для наблюдения химического языка клеток по всему организму.
Цитирование: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
Ключевые слова: внеклеточная сигнализация, флуоресцентные биосенсоры, визуализация глутамата, динамика калия, гиппокампальные нейроны