Clear Sky Science · ru
Структурная характеристика связывания металлов в человеческой тиозил-протеин сульфотрансферазе 2, TPST2
Почему мелкие ионы металлов важны для клеточной сигнализации
Внутри наших клеток бесчисленные молекулярные механизмы тихо настраивают рост тканей, действие гормонов и общение иммунных клеток. Один из таких механизмов — фермент TPST2 — добавляет небольшой сульфатный ярлык к определённым белкам по мере их прохождения через «почтовый центр» клетки, аппарат Гольджи. Это исследование показывает, как простые ионы металлов, такие как натрий и марганец, повышают эффективность TPST2, слегка уплотняя отдельные участки его структуры — открытие, которое может связывать минеральный баланс в клетках с раком и гормональными нарушениями. 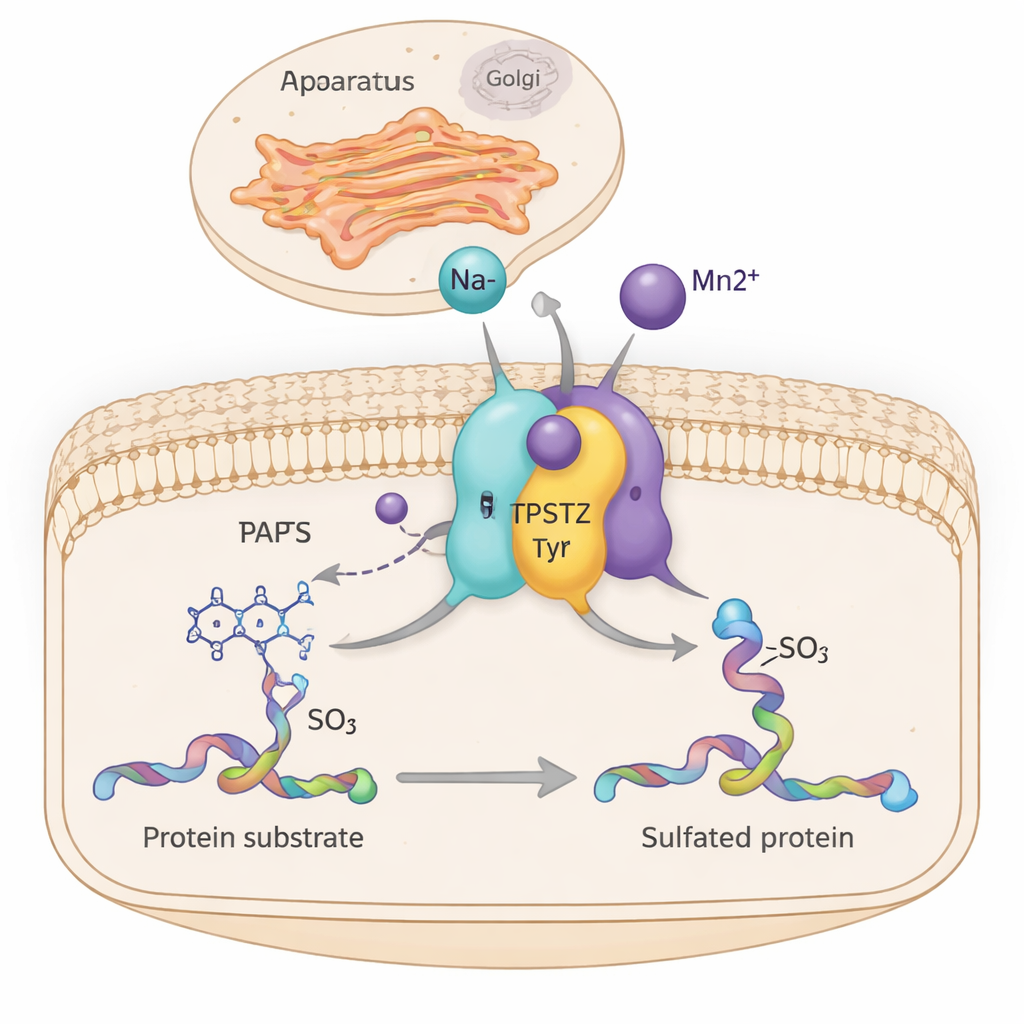
Белок, который украшает другие белки
TPST2 относится к семейству ферментов, выполняющих «сульфирование тирозина» — химическую модификацию, вносимую в определённые остатки тирозина в белках. Эти сульфированные белки играют ключевые роли за пределами клетки, влияя на свертывание крови, движение лейкоцитов, связывание гормонов с рецепторами и даже проникновение вирусов в клетки. У человека есть два основных сульфирующих фермента, TPST1 и TPST2, которые находятся в мембране аппарата Гольджи и модифицируют белки по мере их подготовки к выводу из клетки. Исследования на мышах показывают, что потеря TPST2 нарушает выработку тиреоидных гормонов, замедляет рост и вызывает мужское бесплодие, что подчёркивает его важность для нормальной физиологии.
Связь с раком и ускользанием от иммунитета
Недавние исследования прямо связывают TPST2 с заболеваниями. При меланоме TPST2 модифицирует компонент рецептора интерферона так, что ослабляет иммунную сигнализацию, и блокировка TPST2 усиливает эффект иммунных терапий, нацеленных на PD-1. При раке поджелудочной железы путь, зависящий от TPST2, помогает стабилизировать белок (integrin β4), который способствует росту и метастазированию опухоли. Ингибирование TPST2 в таких моделях замедляет деление и инвазию раковых клеток. Поскольку TPST2 действует на белки на поверхности клетки, он фактически перенастраивает то, как клетки воспринимают и реагируют на окружение, делая его привлекательной мишенью для новых терапий.
Нахождение металлических «включателей»
Биохимикам давно известно, что TPST2 становится значительно активнее в присутствии двовалентных металлов, таких как марганец (Mn²⁺), но структурный механизм этого феномена был неизвестен. В работе авторы получили каталитическое ядро человеческого TPST2 и кристаллизовали его вместе с побочным продуктом реакции и либо с натрием (Na⁺), либо с марганцем. С помощью рентгеновской кристаллографии высокой разрешающей способности они обнаружили два небольших металловых кармана внутри фермента, каждый с аккуратной шестиугольной (октаэдрической) организацией окружающих атомов. Подбирая длину волны рентгеновского излучения под уникальные сигнатуры разных металлов, исследователи подтвердили, что Mn²⁺ избирательно занимает эти сайты, тогда как такие металлы, как цинк и медь, либо слабо связываются в других местах, либо вовсе не связываются.
Уплотнение ключевых подвижных участков вместо глобальной перестройки
Удивительно, но TPST2 с натрием и TPST2 с марганцем в целом выглядели почти одинаково; не наблюдалось драматического открывания или закрывания белка. Вместо этого металлы в основном влияли на два гибких региона у входа в активный центр: спираль, называемую α3, и соседнюю петлю, известную как петля α12–α13. В безметалльном или слабо связанном состоянии эти сегменты колышутся и частично неупорядочены. При связывании Na⁺ они становятся более упорядоченными; Mn²⁺ дополнительно их фиксирует, что демонстрируется снижением теплового движения в рентгеновских данных и анализами гибкости на компьютере. Эта дополнительная жёсткость умеренно повышает температуру плавления фермента и, как полагают, снижает «энтропийные» затраты на организацию активного сайта — облегчая и ускоряя процесс наведения субстратов TPST2 в правильное положение для сульфирования. 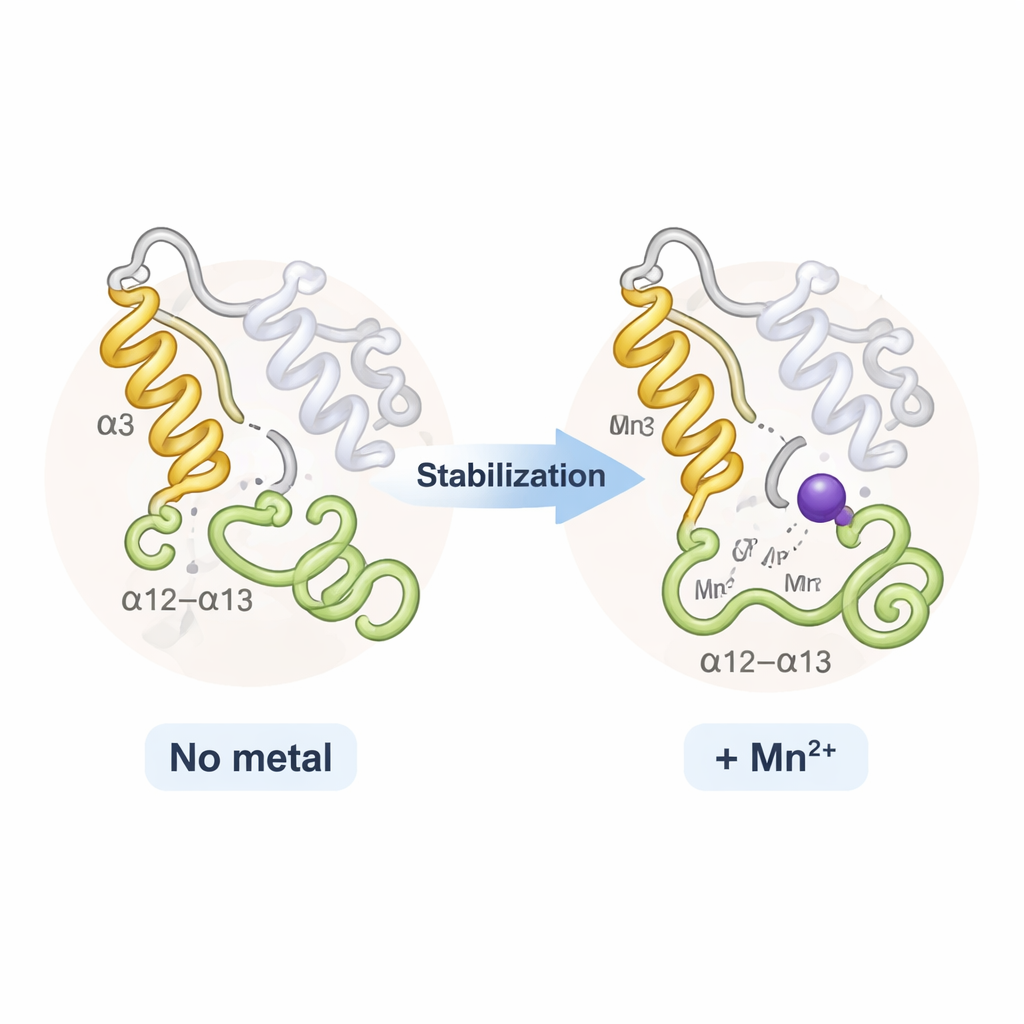
От клеточных минералов к контролю сигнализации
Авторы предлагают модель «активации через упорядочение». При отсутствии связанного металла TPST2 остаётся подвижным у входа в активный сайт и работает неэффективно. Натрий, который в изобилии присутствует в клетках, может связываться в тех же сайтах и создавать частично упорядоченное, умеренно активное состояние. Марганец, находящийся в строго регулируемых микромолярных концентрациях в аппарате Гольджи, связывается сильнее и фиксирует ключевые регионы в оптимально организованное состояние, максимизируя каталитическую эффективность. Это позволяет предположить, что тонкие изменения уровня марганца в Гольджи могут регулировать, насколько активно TPST2 модифицирует свои мишени. Поскольку TPST2 влияет на выработку гормонов и сигналы, связанные с раком, работа подчёркивает возможную связь между балансом ионов металлов, «украшениями» белков и заболеваниями — и предоставляет структурную основу для разработки препаратов, которые модулируют активность TPST2, имитируя или нарушая связывание металлов.
Цитирование: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
Ключевые слова: сульфирование тирозина, TPST2, марганец, аппарат Гольджи, модификация белков