Clear Sky Science · ru
Интегративное машинное обучение и молекулярный докинг выявляют, что нарирутин нацелен на ABCC1/ABCG2 для ремоделирования иммунной микроокружения при колоректальном раке
Соединение из фруктов с большими надеждами против рака
Колоректальный рак — один из самых смертоносных видов рака в мире, и многие пациенты по‑прежнему сталкиваются с тяжёлыми методами лечения и лекарственной резистентностью. В этом исследовании изучают нарирутин, природное вещество, встречающееся в цитрусовых, чтобы выяснить, может ли оно помочь организму мягче бороться с опухолями толстой кишки — за счёт изменения того, как раковые клетки обращаются с лекарствами, и как себя ведут иммунные клетки вокруг опухоли.
От цитрусового фрукта к мишени в раке
Исследователи начали с простого вопроса: если бы нарирутин был лекарством, к каким частям наших клеток он бы «прилипал»? Используя крупные публичные онкологические базы данных и инструменты компьютерного предсказания, они просканировали тысячи генов из опухолей толстой кишки и нормальной ткани. Затем эти гены, связанные с раком, сопоставили с теми, на которые нарирутин наиболее вероятно воздействует. Из более чем 3000 изменённых генов при колоректальном раке нарирутин был предсказан как взаимодействующий значимо всего с девятью, и особенно с пятью «узловыми» генами, которые занимают ключевые контрольные позиции внутри опухолевых клеток.
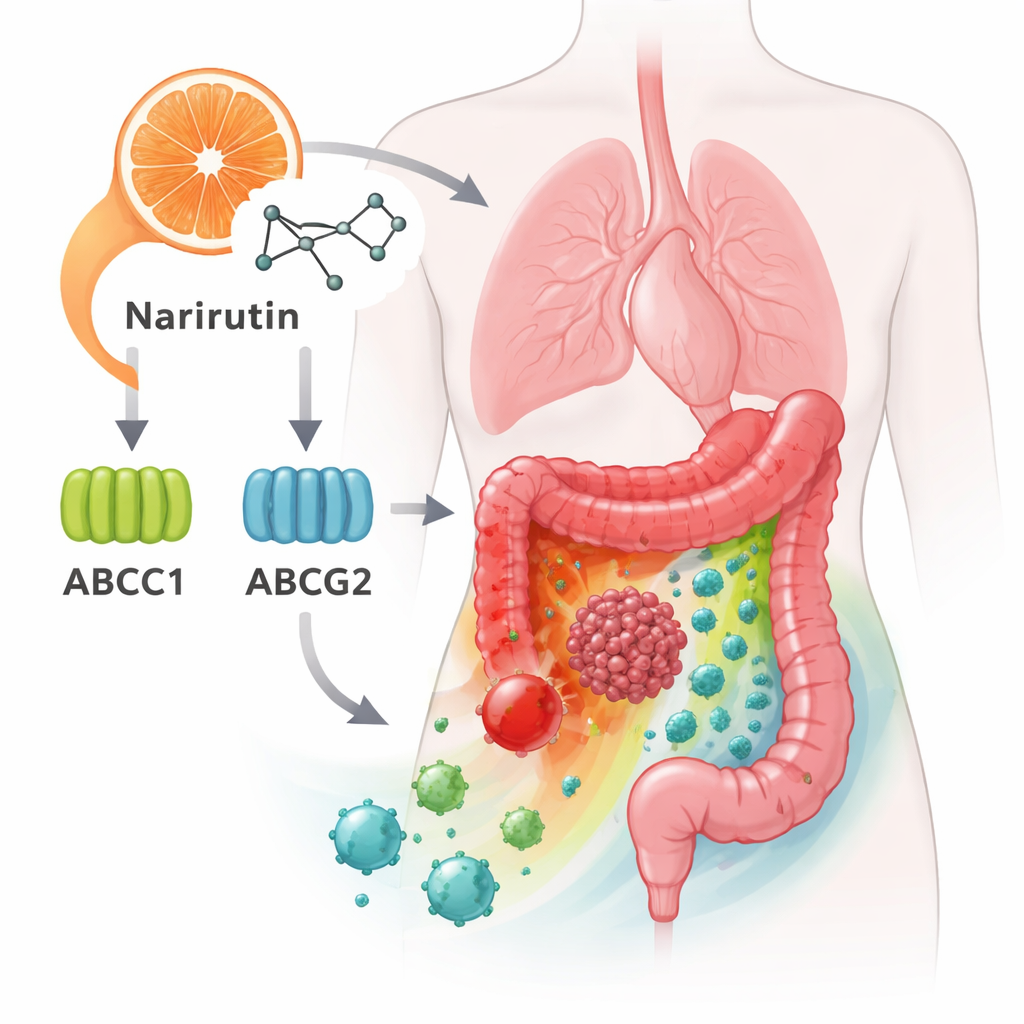
Ключевые «шлюзы» на поверхности раковых клеток
Среди этих узловых генов выделились два: ABCC1 и ABCG2. Они кодируют насосоподобные белки, расположенные в наружной мембране клеток, которые выталкивают лекарства наружу — одна из причин, по которой некоторые раки становятся устойчивыми к химиотерапии. Новая аналитика предполагает, что нарирутин может связываться с этими насосами и, возможно, влиять на их работу. Другие узловые гены, включая CA12, EPHX2 и PTGS1, участвуют в регуляции кислотности, метаболизма липидов и воспалительных сигналов. В совокупности эти гены помогают определять, будет ли опухоль расти бесконтрольно, как она откликается на лекарства и как взаимодействует с окружающей нормальной тканью.
Моделируемое связывание и реальные клинические данные
Чтобы проверить, действительно ли нарирутин может прочно прикрепляться к этим целевым белкам, команда использовала молекулярный докинг — высокоточные компьютерные модели, предсказывающие, как малая молекула помещается в большой белок. Эти симуляции показали, что нарирутин плотно «упаковывается» в карманы целевых белков и формирует стабильные контакты, что делает связывание физически правдоподобным. При анализе данных пациентов исследователи обнаружили, что узловые гены чётко различают опухолевую ткань и нормальную и связаны с выживаемостью пациентов. Например, более высокие уровни ABCC1 и PTGS1 часто ассоциировались с худшими исходами, что указывает на то, что подавление этих генов — потенциально с помощью соединений вроде нарирутина — могло бы быть полезным.
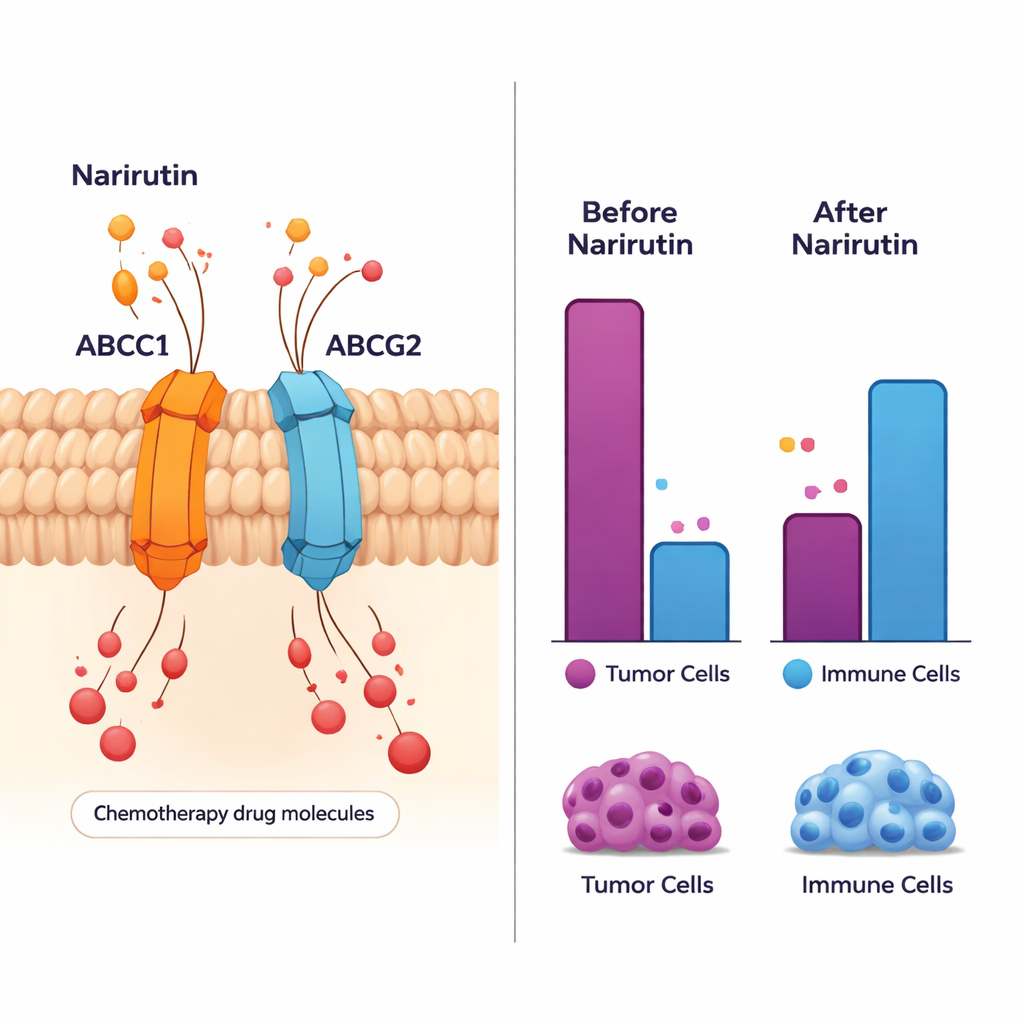
Переформатирование иммунного «района» опухоли
Рак не растёт в изоляции; он существует в оживлённом «районе» из иммунных клеток, кровеносных сосудов и вспомогательной ткани. В исследовании проанализировали 28 различных типов иммунных клеток вокруг опухолей толстой кишки и обнаружили широкие сдвиги по сравнению с нормальной тканью. Некоторые полезные иммунные клетки, такие как активированные B‑клетки и определённые T‑клетки, были более многочисленными или вели себя иначе в опухолях. Основные мишени нарирутина, особенно ABCC1, ABCG2 и PTGS1, показали сильные связи с этими иммунными изменениями. Это даёт основание полагать, что, действуя на эти гены, нарирутин может влиять не только непосредственно на раковые клетки, но и настраивать локальный иммунный ответ — возможно делая среду менее благоприятной для роста опухоли.
Обещает многое, но предстоит ещё работа
Проще говоря, это исследование предлагает, что природный флавоноид из цитрусовых может «заблокировать насосы», которые используют раковые клетки, чтобы уйти от химиотерапии, и помочь перестроить иммунный ландшафт вокруг опухолей толстой кишки. Работа основана на мощных компьютерных анализах и больших генетических наборах данных, а не на лабораторных или клинических испытаниях, поэтому она представляет собой ранний, но важный шаг. Если будущие эксперименты в клетках, животных и пациентах подтвердят эти предсказания, нарирутин — или препараты, созданные по его образцу — однажды могут войти в состав комбинированных терапий, которые сделают стандартное лечение колоректального рака более эффективным и менее уязвимым к резистентности.
Цитирование: Bian, R., Wang, H., Zhang, H. et al. Integrative machine learning and molecular docking reveal Narirutin targets ABCC1/ABCG2 for immune microenvironment remodeling in colorectal cancer. Sci Rep 16, 7649 (2026). https://doi.org/10.1038/s41598-026-37181-y
Ключевые слова: колоректальный рак, нарирутин, лекарственная резистентность, опухолевое микроокружение, модуляция иммунитета