Clear Sky Science · ru
Геномные скрининги выявляют ключевые регуляторы экспрессии прионов на поверхности клеток
Почему это важно для здоровья мозга
Прионные болезни, такие как болезнь Крейтцфельдта–Якоба у людей и «коровье бешенство» у крупного рогатого скота, редки, но всегда смертельны. Центральная причина — обычный мозговой белок, называемый прионным белком, который может неправильно сворачиваться и распространять повреждение от клетки к клетке. Чем больше этого белка находится на поверхности нервных клеток, тем легче болезни прижиться. В этом исследовании поставлена цель просканировать весь геном, чтобы выяснить, какие гены контролируют количество прионного белка на внешней стороне клеток, похожих на нейроны. Такая карта может помочь учёным разработать способы снижения этого белка и потенциально замедлить развитие различных нейродегенеративных заболеваний.
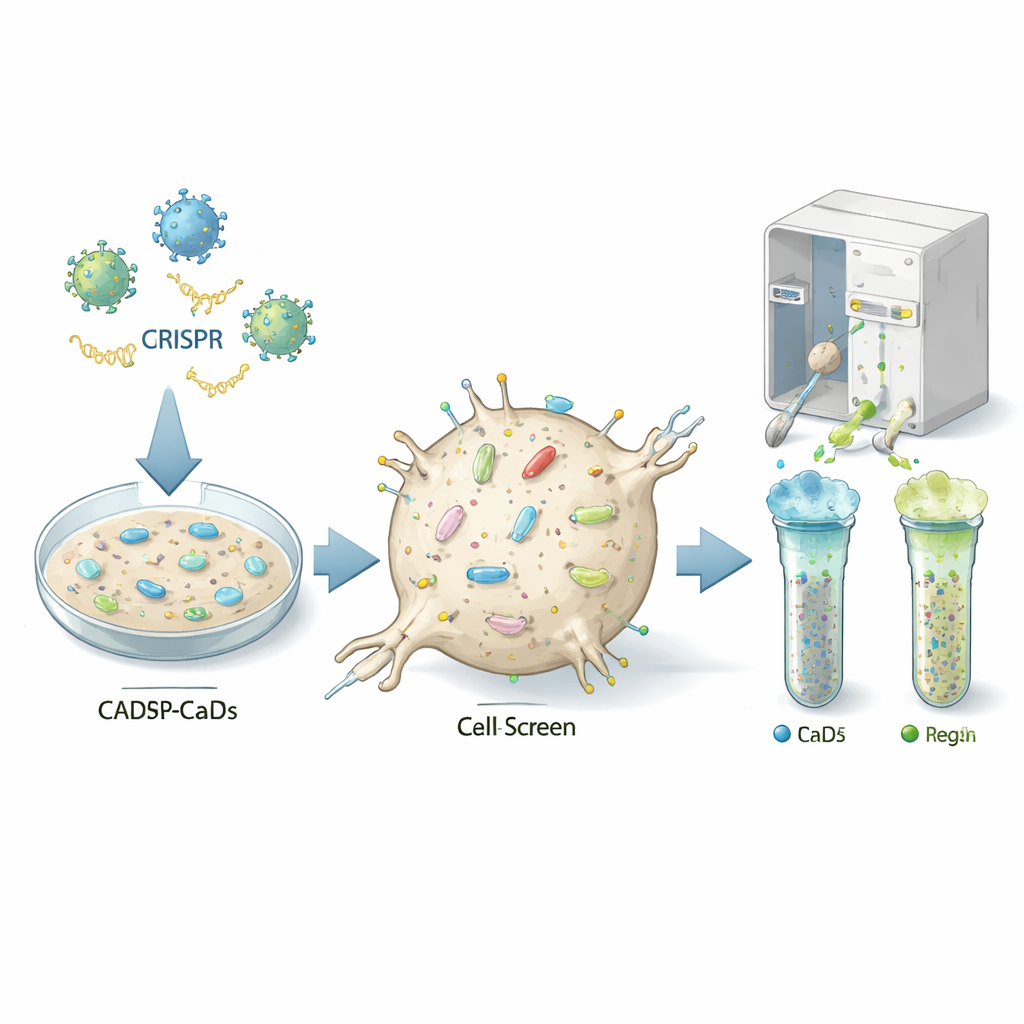
Поиск «ручек управления» клетки
Авторы использовали мощный метод редактирования генома, называемый CRISPR, чтобы поочерёдно выключить практически каждый ген в мышиной клеточной линии, напоминающей нейроны, которая восприимчива к прионам (CAD5-клетки). Каждая клетка получала «удар» по разному гену, поэтому итоговая популяция содержала миллионы вариантов, в каждом из которых отсутствовал определённый ген. Команда затем окрашивала клетки флуоресцентными антителами, распознающими нормальный прионный белок на поверхности, и с помощью сортировщика разделяла клетки с необычно низким или высоким уровнем этого белка. Секвенирование гидирующих РНК, обогащённых в группах с низким или высоким уровнем, позволило определить, какие выбитые гены обычно действуют как включатели или выключатели для прионного белка на поверхности клетки.
Два состояния клетки — пересекающиеся ответы
Нейроны не одинаковы по внешнему виду и поведению на разных стадиях жизни, поэтому исследователи проверили, управляют ли те же гены прионным белком в различных состояниях клетки. CAD5-клетки можно поддерживать в быстроделящемся, менее специализированном состоянии или, убрав сыворотку из среды, перевести в более зрелую, нейроно-подобную форму. Команда провела одинаковый геномный CRISPR-скрининг в обеих условиях. В недифференцированных (менее зрелых) клетках они подтвердили 46 генов, повышающих, и 21 ген — снижающих уровень прионного белка на поверхности при их наличии. В дифференцированных (более нейроноподобных) клетках выявили 41 положительный и 13 отрицательных регуляторов. Двадцать три гена — в основном те, которые участвуют в прикреплении липидного «якоря» к белку — оказались общими для обоих состояний, что подчёркивает существование базового регуляторного механизма, действующего независимо от зрелости.
Ключевые «сборочные линии», которые имеют наибольшее значение
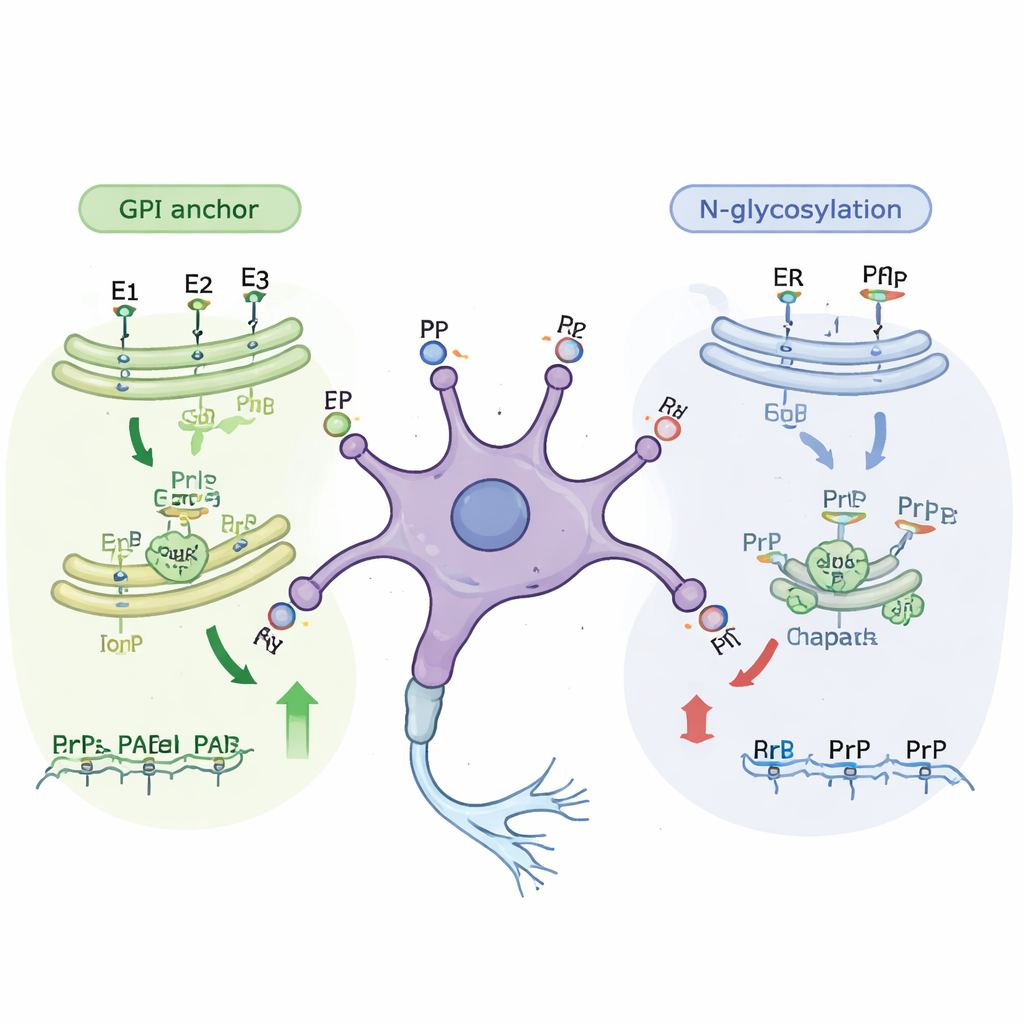
Дальнейший анализ показал, что многие вновь идентифицированные гены принадлежат к известным внутриклеточным «сборочным линиям», модифицирующим белки по пути к поверхности клетки. Одна важная цепочка строит GPI-анкоры — небольшие богатые липидами структуры, прикрепляющие прионный белок к внешней поверхности клеточной мембраны. Нарушение почти любого шага в этом пути сокращало количество прионного белка на поверхности как в незрелых, так и в зрелых клетках. Вторая ветвь связана с N-связанным гликозилированием, когда к белкам по мере прохождения через внутренние мембраны клетки добавляются сложные сахарные цепочки. Гены этого пути в основном проявляли себя как важные в менее зрелых клетках. Когда исследователи обрабатывали клетки малыми молекулами, блокирующими конкретные этапы гликозилирования, уровень прионного белка на поверхности падал примерно на треть без гибели клеток, что подтвердило генетические находки.
Помогающие белки и ответ на стресс
Скрининги также выделили молекулярные шапероны — белки, помогающие другим белкам сворачиваться правильно — как важные регуляторы прионного белка. В частности, Hspa5 (также называемый BiP), ключевой шаперон в компартменте сворачивания белков клетки, проявился как положительный регулятор в более нейроноподобных клетках. При использовании препарата, ингибирующего Hspa5, уровни прионного белка на поверхности падали в обоих состояниях клеток, опять же без очевидного вреда для клеток. Среди других попаданий были гены, участвующие в транспортировке белков по клетке, в контроле включения генов, а также несколько белков, связанных с функцией синапсов и другими заболеваниями мозга, такими как болезнь Альцгеймера и БАС. В совокупности эти результаты показывают, что уровни прионного белка на поверхности формируются сетью путей, охватывающих синтез белка, его модификацию, транспорт и контроль качества.
Что это значит для будущих терапий
Эта работа представляет собой первый всесторонний каталог генов, контролирующих количество прионного белка на поверхности нейроно-подобных клеток, восприимчивых к прионной инфекции. Некоторые из этих генов, особенно те, что участвуют в путях GPI-анкеров и N-гликозилирования, а также система шаперонов Hspa5, выглядят многообещающими точками для разработки лекарств: снижение их активности должно уменьшить количество прионного белка, доступного для неправильного сворачивания, и предыдущие исследования показывают, что даже частичное снижение может существенно отложить развитие болезни в экспериментах на животных. В то же время явные различия между незрелыми и зрелыми клетками подчёркивают, что состояние клеток мозга имеет значение при выборе мишеней. Хотя требуется дополнительная работа, чтобы проверить, как манипуляции этими генами влияют на реальную прионную инфекцию и другие нейродегенеративные состояния в живом мозге, это исследование даёт дорожную карту клеточных рычагов, которые учёные могут исследовать для замедления или предотвращения этих разрушительных заболеваний.
Цитирование: Beauchemin, K.S., Supattapone, S. Genome-wide screens identify core regulators of cell surface prion protein expression. Sci Rep 16, 5895 (2026). https://doi.org/10.1038/s41598-026-37137-2
Ключевые слова: прионный белок, CRISPR-скрининг, нейродегенерация, гликозилирование белков, GPI-якорь