Clear Sky Science · ru
Повышенное давление на двух твердых поверхностях и сверхбыстрое охлаждение улучшают восстановление печеночных клеток и точечно вырезанных срезов печени после оттаивания
Почему важно замораживание печеночной ткани
Сохранение клеток и тканей живыми вне организма — одна из тихих опор современной медицины. Замороженные печеночные клетки помогают исследователям тестировать новые лекарства, моделировать заболевания и, возможно, в будущем восстанавливать отказавшие органы. Но замораживание живых материалов — сложная задача: если внутри или между клетками образуются кристаллы льда, они разрывают нежные структуры. В этом исследовании изучается новый способ столь стремительного и контролируемого замораживания печеночных клеток и тонких срезов печени, что вредоносным кристаллам льда практически не остается времени на формирование.
Проблема льда и химических защитников
Традиционная криоконсервация опирается на два несовершенных инструмента: холод и химикаты. По мере охлаждения вода склонна превращаться в лед, который может проколоть мембраны и нарушить структуру ткани. Чтобы этому противодействовать, ученые добавляют криопротекторы, такие как диметилсульфоксид (ДМСО), которые помогают воде перейти в стеклообразное состояние вместо кристаллического льда. Однако при типично высоких концентрациях эти вещества сами по себе могут быть токсичны для клеток или вызывать вредное набухание и усыхание по мере их проникновения в ткань и выхода из нее. Цель авторов состояла в том, чтобы сократить количество требуемого ДМСО, при этом по‑прежнему предотвращая образование вредного льда, делая хранение печеночных клеток и тканей более безопасным и практичным.
Новый способ одновременного сжатия и охлаждения
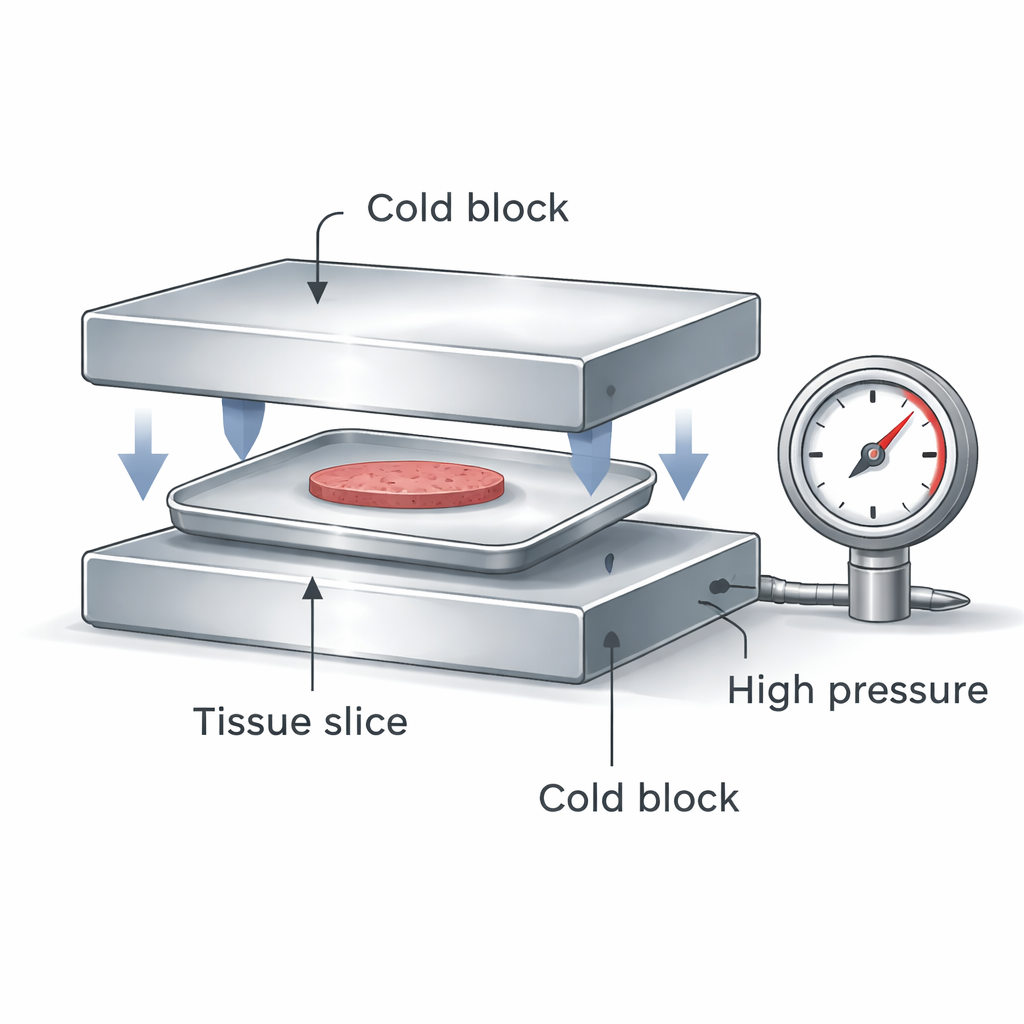
Команда разработала компактное устройство, которое размещает герметичный плоский алюминиевый контейнер с печеночными клетками или точечно вырезанными срезами печени между двумя чрезвычайно холодными металлическими блоками. Когда блоки сжимаются, они выполняют одновременно две важные функции: создают высокое давление внутри герметичного контейнера и отводят тепло из образца с обеих сторон. Высокое давление изменяет поведение воды так, что лед образуется при более низких температурах, и раствор легче переходит в стеклообразное состояние. Контакт с двух сторон обеспечивает гораздо более быстрое и равномерное охлаждение, чем простое погружение пластиковой ампулы в жидкий азот, а герметичный контейнер изолирует образец от загрязнений.
Поиск оптимума между безопасностью и выживаемостью
Чтобы проверить, достаточно ли мягок этот метод для живого материала, исследователи сначала убедились, что сам алюминиевый контейнер не вредит полученным из печени клеткам HepG2 в течение короткого времени обработки. Выживаемость клеток оставалась фактически неизменной. Затем эти клетки подвергали воздействию разных уровней ДМСО перед замораживанием и подтвердили хорошо знакомую компромиссную ситуацию: большее количество ДМСО лучше подавляет образование льда, но при 30% становится явно токсичным, тогда как 20% остается в большой степени переносимым. Для мышиных срезов печени они проверяли, какое давление ткань выдерживает без замораживания. Короткие всплески до 150 мегапаскалей мало влияли на жизнеспособность, но 200 мегапаскалей вызывали примерно 30% падение, обозначив верхний предел для безопасной работы.
Лучше сохранившиеся печеночные срезы после оттаивания
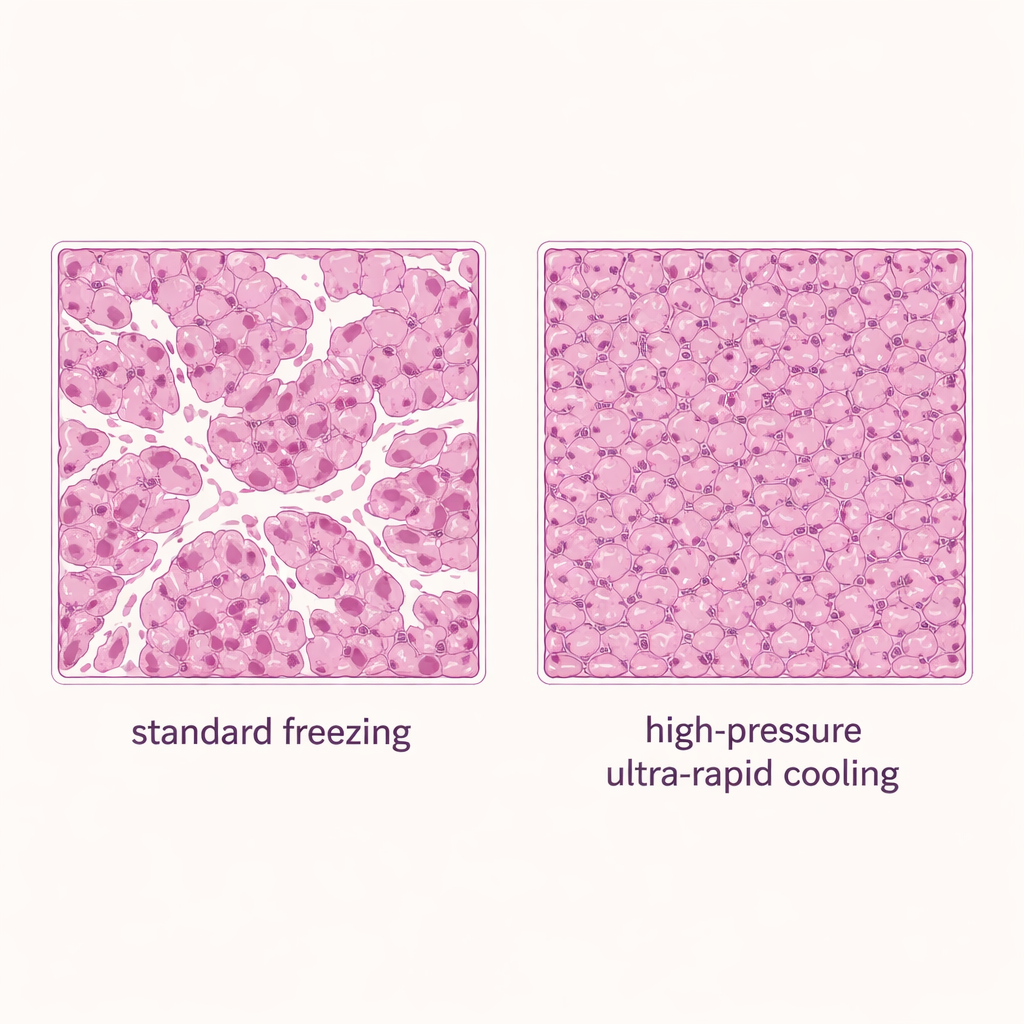
Установив безопасные диапазоны, авторы сравнили три метода замораживания срезов печени: стандартное погружение герметичного контейнера в жидкий азот (конвекционный, то есть жидкостный подход), охлаждение на твердой поверхности без увеличенного давления и охлаждение на твердой поверхности с высоким давлением 150 мегапаскалей. Во всех группах использовали 20% ДМСО. Метод с поддержкой давления дал лучшие результаты: примерно 80% исходной жизнеспособности ткани сохранялось, что превосходило как стандартное замораживание, так и охлаждение на твердой поверхности без давления. Микроскопия окрашенных срезов поддержала эти выводы. Образцы, замороженные при обычном погружении, показывали множество открытых белых пространств — признаки повреждения льдом — тогда как при усиленном давлением охлаждении на твердой поверхности ткань была плотнее и более целостной с гораздо меньшим числом пустот.
Что это значит для будущего хранения тканей
В целом исследование показывает, что сжатие герметичного алюминиевого среза печени между двумя сверххолодными блоками под тщательно контролируемым высоким давлением может значительно улучшить выживаемость ткани после оттаивания. Комбинируя более быстрое и равномерное охлаждение с изменением поведения воды под давлением, метод ограничивает рост вредного льда, при этом сохраняя умеренную, клинически знакомую концентрацию ДМСО. Для неспециалиста вывод прост: более продуманная инженерия — то, как мы упаковываем и охлаждаем ткань — может быть не менее важна, чем химические добавки. Этот двусторонний метод с высоким давлением может стать шагом на пути к более безопасному и надежному хранению печеночной ткани и, в перспективе, других органов для исследований и терапии.
Цитирование: Amini, M., Benson, J.D. Pressure enhanced dual-solid-surface ultra-rapid cooling improves post-thaw recovery in hepatocytes and precision cut liver slices. Sci Rep 16, 5994 (2026). https://doi.org/10.1038/s41598-026-37136-3
Ключевые слова: криоконсервация, печеночная ткань, витрификация, высокое давление при охлаждении, замораживание без образования льда