Clear Sky Science · ru
DANEELpath — открытые цифровые инструменты анализа для гистопатологических исследований в моделях нейробластомы
Почему крошечные опухоли в геле важны
Рак — это не просто масса бунтующих клеток; это целый микрорайон, где клетки общаются друг с другом и со своей опорной структурой. В детских онкологиях, таких как нейробластома, эта окружающая «поддержка» может способствовать росту опухолей и их устойчивости к лечению. В этом исследовании представлен DANEELpath — бесплатный, с открытым исходным кодом набор цифровых инструментов, который превращает микроскопические изображения выращенных в лаборатории мини-опухолей в подробные количественные карты. Тем самым он помогает учёным понять, как клетки опухоли располагаются, как они реагируют на экспериментальные препараты и как эти наблюдения могут привести к лучшим терапиям для детей.
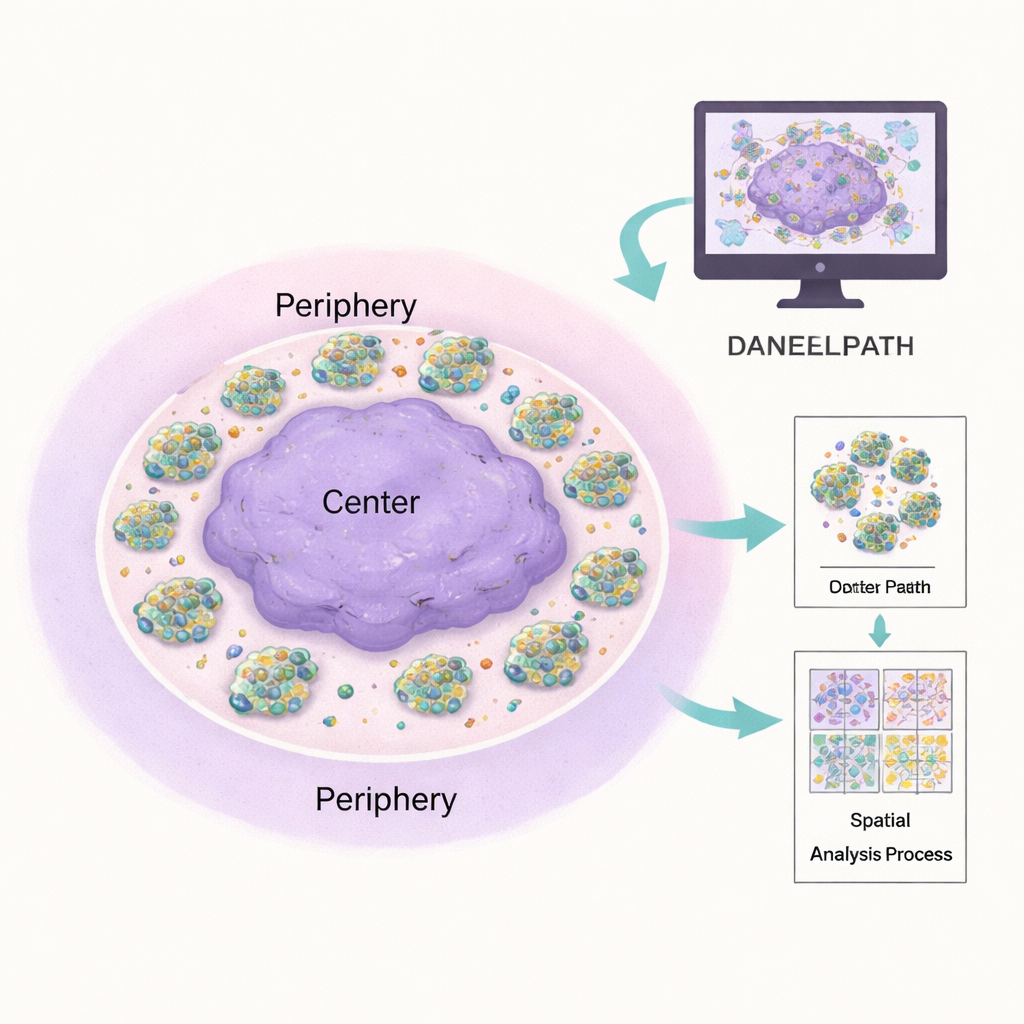
Создание маленьких опухолевых миров в лаборатории
Чтобы имитировать сложную среду настоящей опухоли, исследователи выращивают клетки нейробластомы внутри мягких 3D-гидрогелей из желатина и шёлка. В таких условиях клетки естественным образом формируют округлые кластеры, похожие на крошечные опухоли. Важную роль здесь играет витронектин — «клейкий» белок внеклеточного матрикса, который помогает клеткам прикрепляться и может способствовать более агрессивному течению болезни. Команда подготовила гидрогели с добавочным витронектином и без него, а некоторые образцы обработали целенгитидом — экспериментальным препаратом, блокирующим рецепторы, связанные с витронектином. Через несколько недель гели были разрезаны, окрашены и отсканированы в виде высокоразрешающих полнотканевых изображений, создавая цифровую версию каждого мини-опухолевого мира.
Преобразование сложных изображений в измеримые закономерности
Традиционная патология опирается на опыт глаз специалиста под микроскопом — это мощно, но трудно стандартизировать и масштабировать. DANEELpath интегрируется с популярной платформой с открытым исходным кодом QuPath и автоматизирует большую часть этой работы. С помощью моделей глубокого обучения типа U-Net набор инструментов точно выделяет контуры каждого клеточного кластера на обычных окрасках, даже когда размеры кластеров варьируются от нескольких клеток до сотен. Затем применяются математические методы, которые разбивают каждый неправильно сформованный гидрогель на сбалансированные «центр» и «периферию», что обеспечивает справедливое сравнение внутренней и внешней зон независимо от формы геля. Это позволило авторам подтвердить, что кластеры нейробластомы обычно более плотны у края гидрогеля, и что этот рисунок меняется в зависимости от содержания витронектину и лечения препаратом.
Измерение расстояний между клетками и соседями кластеров
Помимо простого подсчёта кластеров, DANEELpath исследует пространственную организацию клеток и кластеров. Внутри каждого кластера другой модуль находит отдельные ядра клеток и измеряет расстояние до ближайшего соседа, суммируя, насколько плотно упакованы клетки. Между кластерами набор предлагает три способа определения «соседей», включая метод на основе диаграмм Вороного, который рисует зоны влияния вокруг каждого кластера. Сравнивая эти показатели в разных условиях, исследователи показали, что целенгитид изменяет число соседних кластеров у большого кластера и их распределение — но эти изменения зависят от того, был ли в геле добавлен витронектин. Это подчёркивает, как внеклеточный матрикс и механотерапевтические препараты совместно формируют организацию опухоли.
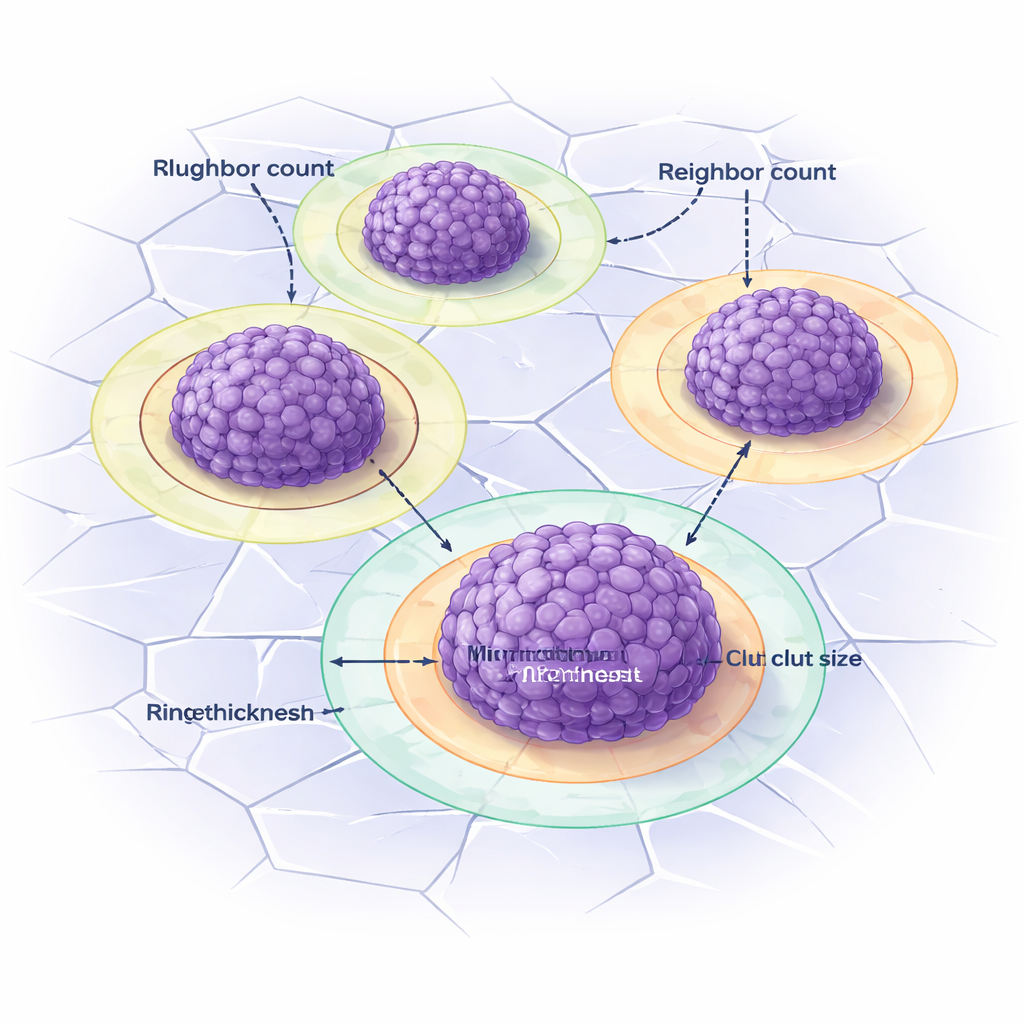
Наблюдение «ореола» вокруг опухолевых кластеров
Витронектин в этих моделях часто образует заметные кольца вокруг кластеров: яркую «корону», когда присутствует только витронектин, вырабатываемый клетками, и бледный ореол, когда дополнительный витронектин встроен в гель. Визуально отделить эти кольца от ядра кластера сложно. DANEELpath решает эту задачу, сначала строя на основе Вороного зоны влияния вокруг каждого кластера, затем расширяя их наружу ровно настолько, чтобы захватить кольцо без наложения на соседей. Простейшие правила по контрасту изображения используются для обнаружения корон и ореолов, а инструмент автоматически измеряет их толщину. Подобные стратегии также применяли к образцам пациентов: например, для картирования иммунных клеток на границе опухолевых областей или для определения зон вокруг кровеносных сосудов, чтобы изучать расположение витронектина и других маркеров в тканях человека с нейробластомой.
Что это означает для будущих исследований рака
По сути, эта работа превращает статичные патоморфологические изображения в детальные, воспроизводимые измерения организации опухолевых клеток и их окружения. Для неспециалистов это означает, что исследователи теперь могут проще проверять, как новые препараты, материалы для матрикса или генетические изменения влияют не только на то, растут ли опухоли, но и на то, как они растут в пространстве. Поскольку DANEELpath с открытым исходным кодом, имеет графический интерфейс и работает на обычных компьютерах, он снижает порог доступа для лабораторий по всему миру к продвинутому анализу изображений. Со временем такие инструменты могут помочь связать закономерности, наблюдаемые в 3D-моделях и тканях пациентов, с клиническими исходами, направляя создание более целевых и эффективных методов лечения детей с высоко рискованной нейробластомой.
Цитирование: Vieco-Martí, I., López-Carrasco, A., Navarro, S. et al. DANEELpath open source digital analysis tools for histopathological research in neuroblastoma models. Sci Rep 16, 6162 (2026). https://doi.org/10.1038/s41598-026-37134-5
Ключевые слова: нейробластома, цифровая патология, 3D гидрогели, внеклеточный матрикс, глубокое обучение