Clear Sky Science · ru
Связанные с сенесценцией лнкРНК TRMP и TRMP-S способствуют развитию рака желудка через активацию IGFL4
Почему это исследование важно
Рак желудка по-прежнему остается одним из самых смертельных видов рака в мире, в основном потому, что его часто обнаруживают на поздних стадиях, и лечение может быть сложным. В этом исследовании раскрыто, как два малоизученных генетических молекулы — TRMP и его короткий изоформ TRMP-S — помогают опухолям желудка расти и распространяться. Выявив цепочку событий, которые они запускают в раковых клетках и в иммунной среде опухоли, работа указывает на новые подходы, которые в будущем могут помочь врачам диагностировать пациентов раньше и разрабатывать более эффективные таргетные терапии.
Скрытые послания в нашей ДНК
Большинство людей представляют гены как чертежи для белков, но наша ДНК также синтезирует длинные некодирующие РНК (lncRNA), которые не кодируют белки, но сильно влияют на поведение клеток. TRMP и его короткий сплайсинг-вариант TRMP-S — два таких lncRNA. Ранее их связывали со старением и контролем клеточного цикла в легочных и кишечных клетках, но их роль в раке желудка была неизвестна. Поскольку lncRNA могут служить маркерами для диагностики и мишенями для терапии, авторы решили выяснить, способствуют ли TRMP и TRMP-S превращению желудочных клеток в раковые и как они могут взаимодействовать с другими молекулами, чтобы этого добиться.
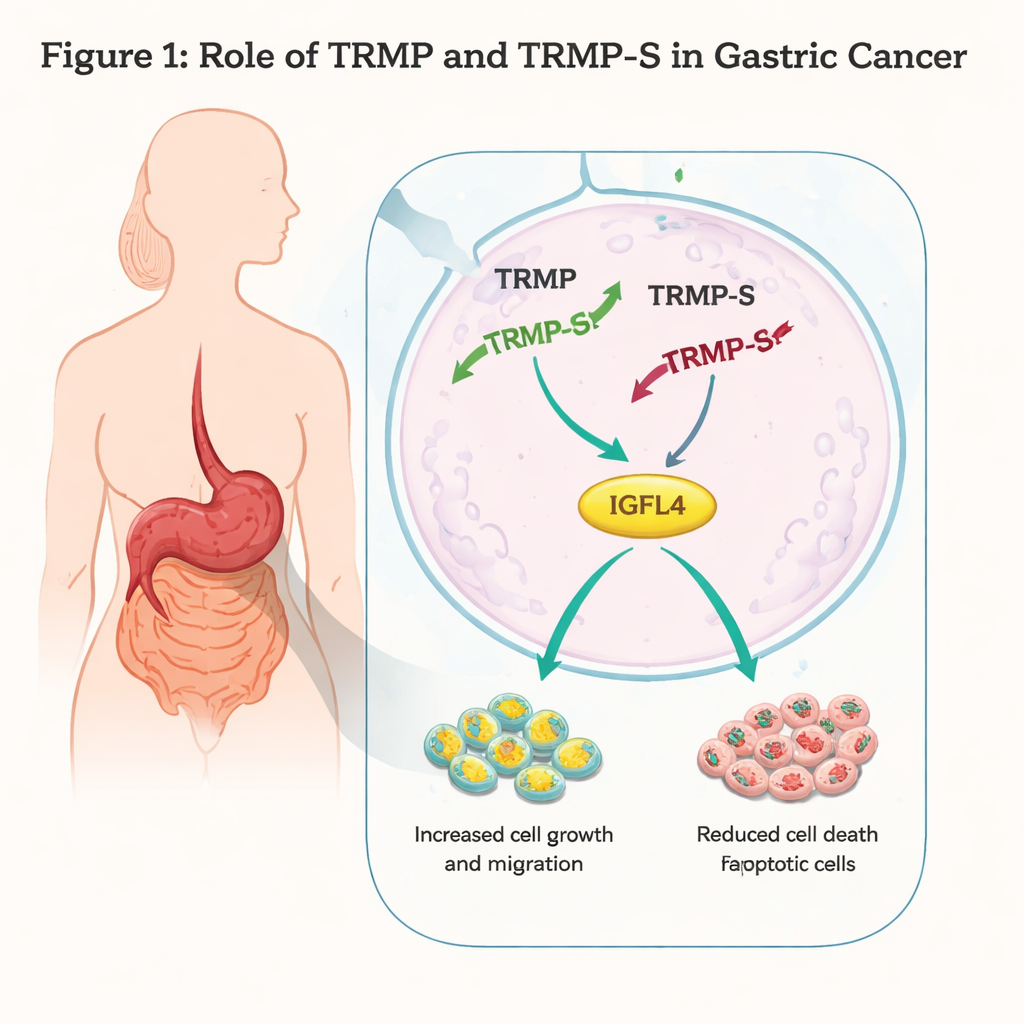
Выключение «ускорителя» рака
Исследователи работали с двумя линиями человеческих клеток рака желудка, AGS и MKN45, и использовали генетические инструменты для снижения уровней TRMP-S и TRMP. При подавлении TRMP-S клетки росли медленнее, образовывали меньше колоний и хуже перемещались через искусственные барьеры или закрывали раны в культуре. Проточная цитометрия и анализ белков показали, что больше клеток проходит программируемую гибель (апоптоз), а клеточный цикл останавливается на фазе G1 — ключевой «контрольной точке» перед репликацией ДНК. Уровни p73, члена семейства супрессоров опухолей p53, повышались при отсутствии TRMP-S, что согласуется с усилением контроля клеточного цикла и увеличением гибели клеток. В совокупности эти результаты указывают на то, что TRMP-S обычно действует как «педаль акселератора» для клеток рака желудка.
Ключевой партнёр: сигнал IGFL4
Чтобы понять, как TRMP и TRMP-S реализуют свои эффекты, команда проанализировала крупные пациентские наборы данных из The Cancer Genome Atlas и корейской когорты рака желудка. Они искали гены, которые были одновременно аномально повышены в опухолях и положительно коррелировали с уровнями TRMP, после чего построили шестигенный «риск-модель», предсказывающую выживаемость пациентов — более высокие баллы коррелировали с худшим прогнозом. Среди этих генов выделялся IGFL4, член семейства, родственного инсулиноподобным факторам роста, которые известны тем, что стимулируют рост и выживание во многих видах рака. В клетках рака желудка снижение уровня TRMP-S резко понижало уровни РНК и белка IGFL4, а РНК-иммунопрепципитация показала, что и TRMP, и TRMP-S физически связываются с белком IGFL4. Прямое подавление TRMP давало тот же ослабляющий эффект на IGFL4, что говорит о том, что эти lncRNA помогают стабилизировать или поддерживать производство этого роста стимулирующего сигнала.
Замедление распространения и перестройка иммунной среды
Когда исследователи использовали малые интерферирующие РНК для подавления собственно IGFL4, клетки рака желудка замедляли рост, меньше мигрировали и демонстрировали более слабую способность инвазировать через мембраны и закрывать раны. Анализ данных опухолей пациентов показал, что уровни IGFL4 значительно выше в опухолях желудка по сравнению с нормальной тканью желудка и повышены во многих других типах рака. Важно, что опухоли с высоким экспрессией IGFL4 демонстрировали характерные паттерны инфильтрации иммунных клеток: больше недифференцированных макрофагов (M0) и меньше плазматических клеток, моноцитов, эозинофилов и нейтрофилов. Вычислительные оценки иммунного статуса предполагали, что опухоли с высоким уровнем IGFL4 могут лучше отвечать на современные иммунотерапии, блокирующие контрольные точки иммунитета, что указывает на то, что IGFL4 может помочь в отборе пациентов, подходящих для этих методов лечения.
Маленькая РНК, которая тормозит развитие
Исследование также выявило противовес этой промотирующей раку цепочке. Сопоставляя экспрессию микроРНК и генов в данных пациентов, авторы выделили miR-129-5p как мелкую РНК, негативно коррелирующую и с TRMP, и с IGFL4. В клетках рака желудка введение miR-129-5p снижало уровни IGFL4 и замедляло рост, тогда как блокада miR-129-5p увеличивала IGFL4 и ускоряла пролиферацию. Другая кандидатная микроРНК, miR-4739, существенного влияния на IGFL4 не оказала и была исключена. Эти результаты поддерживают регуляторную цепочку, в которой TRMP и TRMP-S, miR-129-5p и IGFL4 образуют сеть, тонко настраивающую агрессивность роста раковых клеток желудка и их взаимодействие с окружающей средой.
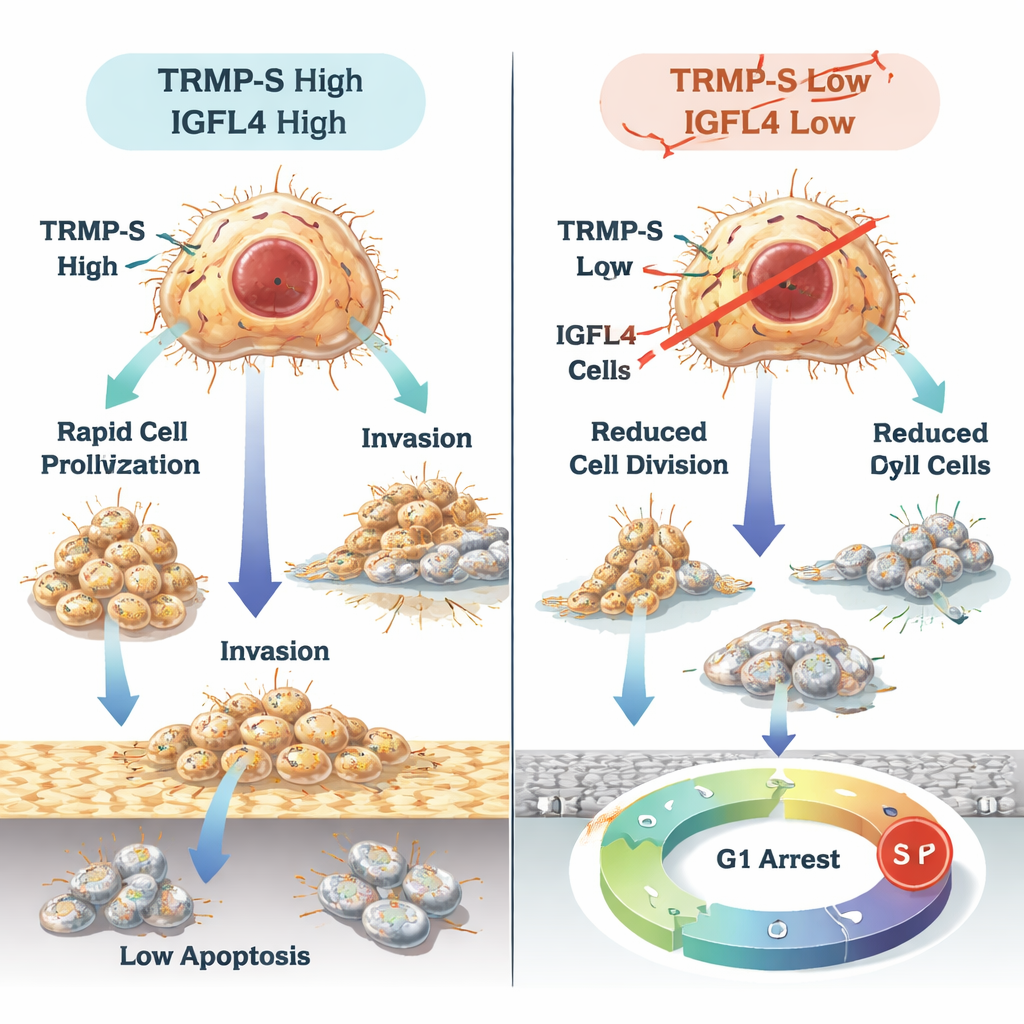
Что это может означать для пациентов
Проще говоря, работа показывает, что TRMP и TRMP-S выступают как закулисные режиссёры, включающие IGFL4 и помогая клеткам рака желудка расти, распространяться и обходить природные механизмы торможения. В то же время малая РНК miR-129-5p действует как тормоз для IGFL4, а сам IGFL4 влияет на то, как иммунные клетки собираются вокруг опухолей и насколько эффективны терапии, активирующие иммунную систему. Несмотря на то, что необходимы дополнительные исследования и клинические испытания, TRMP, TRMP-S, IGFL4 и miR-129-5p в совокупности представляют многообещающую группу маркеров для прогноза и потенциальных новых мишеней для препаратов, направленных на замедление или остановку рака желудка.
Цитирование: Zhang, M., Mi, Y., Li, F. et al. Senescence-associated LncRNAs TRMP and TRMP-S promote gastric cancer by activating IGFL4. Sci Rep 16, 6740 (2026). https://doi.org/10.1038/s41598-026-37106-9
Ключевые слова: рак желудка, длинные некодирующие РНК, TRMP, IGFL4, опухолевый микросреда