Clear Sky Science · ru
Идентификация RBX1 как регулятора транскрипции LIPT1 и его роль в медленной, вызванной медью гибели клеток в клетках ГБМ
Почему важны медь и опухоли головного мозга
Глиобластома многоформенная — одна из самых смертоносных форм рака головного мозга: несмотря на агрессивные операции, лучевую терапию и химиотерапию, большинство пациентов живут лишь небольшой срок после постановки диагноза. В этом исследовании рассматривается неожиданный союзник в борьбе с этими опухолями — металл медь. Ученые изучают недавно описанную форму гибели клеток, вызванную медью, и выявляют молекулярный путь, который может помочь врачам использовать этот процесс для ослабления опухолей и потенциального усиления противоопухолевой реакции иммунной системы.
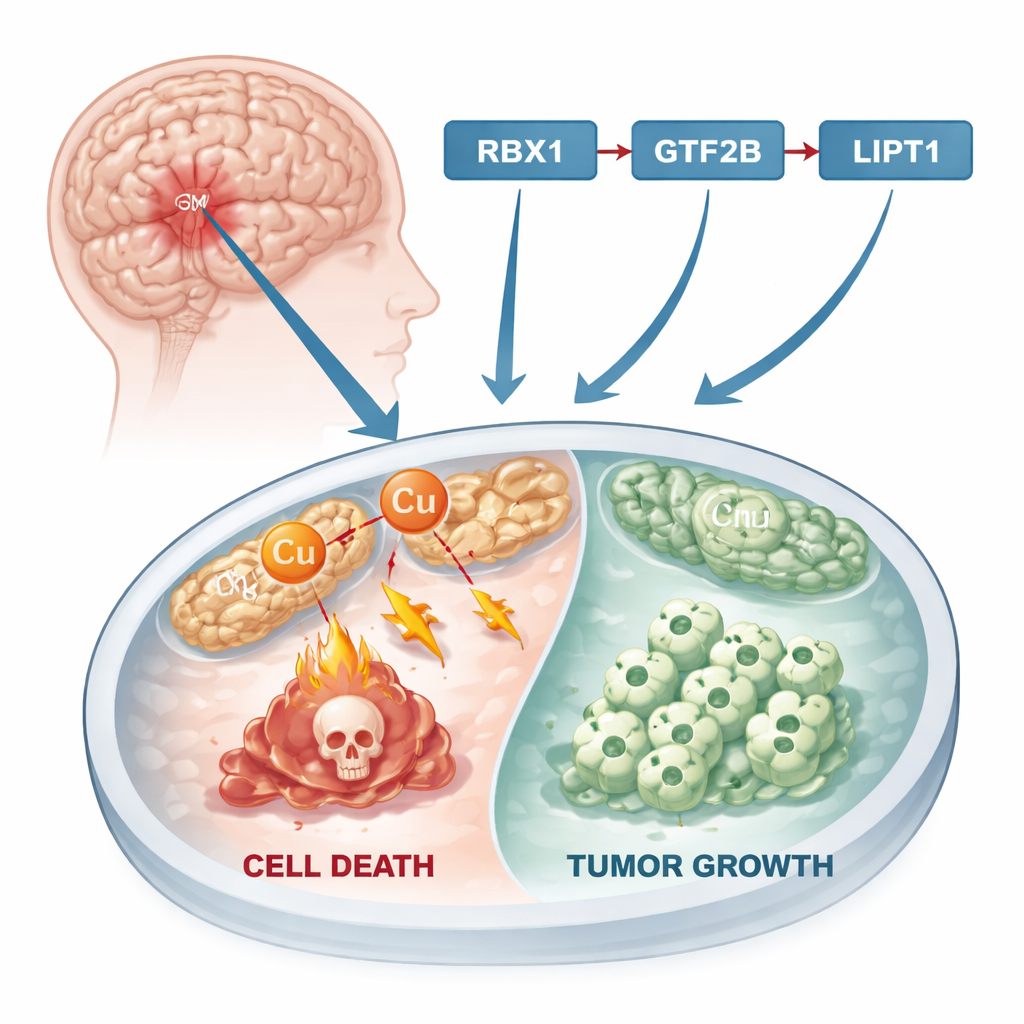
Новый путь гибели клеток
На протяжении десятилетий исследования рака сосредотачивались на знакомых формах гибели клеток, таких как апоптоз, при котором поврежденные клетки «тихо» прекращают свою работу. В последнее время ученые обнаружили иной путь — гибель клеток, индуцируемую медью, или «купроптоз». При этом процессе избыток меди накапливается в энергетических «фабриках» клетки — митохондриях. Там она нарушает работу ключевых белков, вызывая образование токсичных агрегатов и в конечном счете приводя к гибели клетки. Поскольку во многих опухолях метаболизм металлов изменен и уровень меди выше, чем в нормальных тканях, купроптоз представляет собой потенциальную точку приложения: если исследователи сумеют направить опухолевые клетки к этой меди-опосредованной гибели, это может замедлить или остановить рост рака.
Выделение ключевого гена при глиобластоме
Авторы начали с анализа группы генов, уже известных участием в купроптозе, и изучили их поведение в образцах глиобластомы по сравнению с нормальной мозговой тканью. Один ген особенно выделялся — LIPT1. Он был более активен в тканях глиобластомы и в нескольких клеточных линиях глиобластомы по сравнению с нормальными мозговыми клетками. Что важно, у пациентов, чьи опухоли имели более высокую активность LIPT1, наблюдалась более длительная безрецидивная выживаемость после лечения. Высокие уровни LIPT1 также коррелировали с большим количеством CD8 Т‑клеток — ключевых иммунных эффекторов против рака, — что предполагает, что этот ген может способствовать созданию в опухолевой среде условий, более уязвимых для иммунной атаки.
Что происходит, когда выключается «медный» выключатель смерти
Чтобы проверить, действительно ли LIPT1 влияет на медь-индуцированную гибель клеток, команда подвергла клетки глиобластомы воздействию лекарственной комбинации, доставляющей медь и надежно вызывающей купроптоз. Затем они использовали генетические инструменты для снижения уровня LIPT1. При подавлении LIPT1 опухолевые клетки стали более устойчивыми к меди-индуцированной гибели, лучше выживали и проявляли повышенные миграционные и инвазивные свойства — поведение, связанное с более агрессивным раком. В смешанных культурах опухолевых клеток и человеческих CD8 Т‑клеток снижение LIPT1 также уменьшало выброс иммунных сигнальных молекул и затрудняло Т‑клеткам уничтожение раковых клеток. В совокупности эти эксперименты указывают на то, что LIPT1 повышает чувствительность к меди-индуцированной гибели и поддерживает антиопухолевую иммунную активность.
Прослеживание командной цепочки до RBX1
Следующей задачей было понять, почему LIPT1 активирован при глиобластоме. Объединив несколько крупных генетических и протеомных баз данных, исследователи выявили фактор транскрипции — своего рода главный переключатель активности генов — GTF2B, который связывается вблизи гена LIPT1 и, вероятно, усиливает его экспрессию. Затем они спросили, что регулирует сам GTF2B. Второй белок, RBX1, проявил себя как сильный кандидат. RBX1 — часть клеточной системы пометки и утилизации белков, которая отмечает другие белки для разрушения. В клетках глиобластомы уровни RBX1 были ниже, чем в нормальных мозговых клетках, тогда как GTF2B и LIPT1 были повышены. Лабораторные тесты показали, что RBX1 может присоединять небольшие «метки — уничтожьте меня» к GTF2B, приводя к его деградации; при увеличении RBX1 уровни GTF2B и активность LIPT1 снижались, а блокада клеточного протеасомного пути обращала этот эффект.
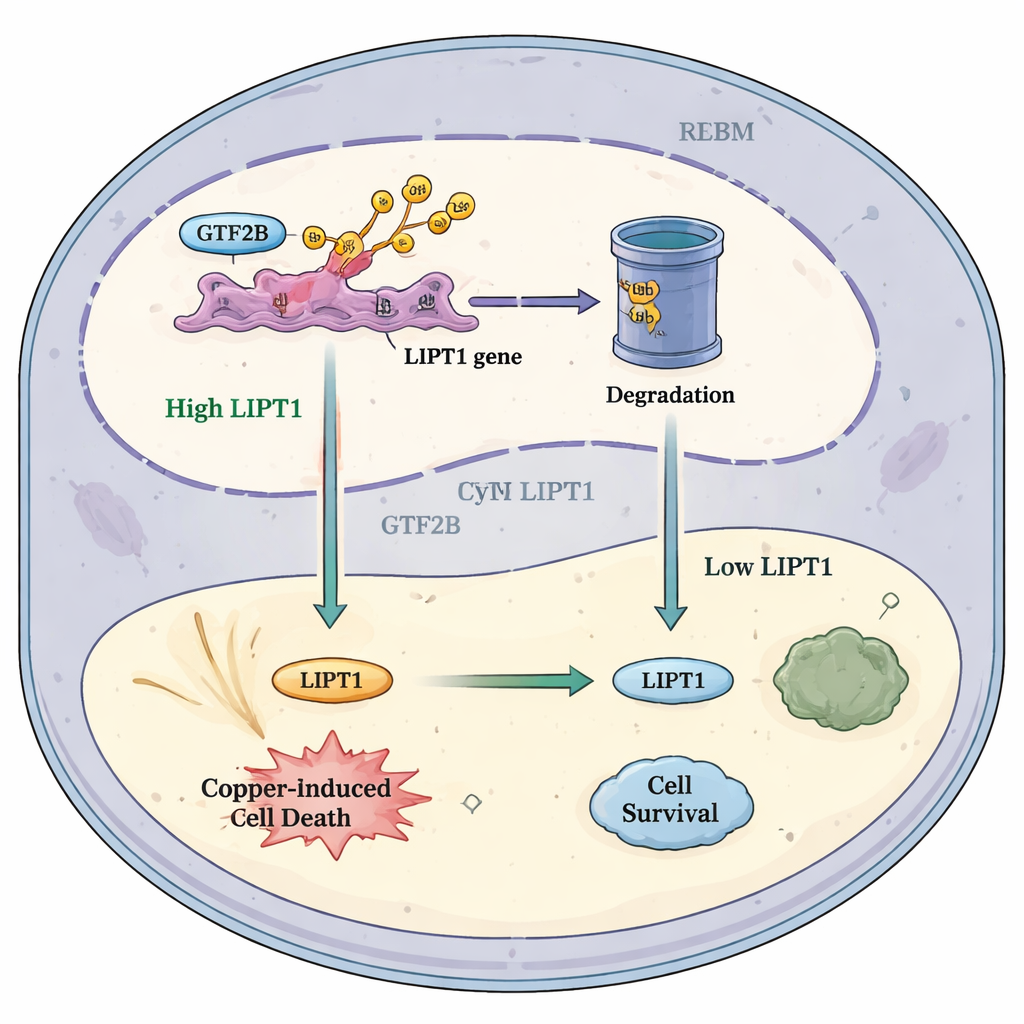
Как этот путь может помочь будущему лечению
Собрав эти данные воедино, авторы предлагают простую модель: в нормальных условиях RBX1 сдерживает GTF2B, ограничивая силу его активации гена LIPT1. При глиобластоме пониженный RBX1 означает меньшую деградацию GTF2B. Избыточный GTF2B усиливает LIPT1, повышая чувствительность опухолевых клеток к меди-индуцированной гибели и привлекая больше иммунных клеток, борющихся с раком. Эта модель предполагает, что аккуратная модуляция пути RBX1–GTF2B–LIPT1, возможно в сочетании с препаратами, нацеленными на медь, и иммунотерапией, может склонить равновесие внутри опухолей мозга в сторону самоуничтожения. Хотя до применения этой идеи у пациентов еще далеко, исследование подчеркивает перспективное пересечение металлобиологии, регуляции генов и онкоиммунологии, которое может открыть новые терапевтические пути для одного из самых устойчивых видов рака.
Цитирование: Zeng, J., Liu, J., Hua, S. et al. Identification of RBX1 as a regulator of LIPT1 transcription and its role in copper-induced cell death in GBM cells. Sci Rep 16, 6837 (2026). https://doi.org/10.1038/s41598-026-37105-w
Ключевые слова: глиобластома, медь-индуцированная гибель клеток, LIPT1, онкоиммунология, путь RBX1