Clear Sky Science · ru
Интеграция машинного обучения и физических моделей для предиктивного проектирования нанокомпозитов с гемцитабином
Более умные противораковые лекарства по замыслу
Препараты против рака, такие как гемцитабин, могут спасти жизни, но часто ведут себя скорее как грубые инструменты, чем как точные приборы: они быстро распадаются, промахиваются мимо мишеней и вызывают сильные побочные эффекты. В этом исследовании рассматривается, как компьютеры могут помочь ученым «предварительно испытывать» новые крошечные носители лекарств на экране, а не только в лаборатории, чтобы сделать лечения с гемцитабином более эффективными, долговечными и потенциально безопаснее для пациентов.
Почему важны крошечные носители
Традиционная химиотерапия заливает организм молекулами лекарства, которые циркулируют повсюду, а не только в опухоли. Нанокомпозиты — сконструированные частицы в тысячи раз меньше зерна песка — предлагают способ упаковать гемцитабин так, чтобы он был защищен в кровотоке и доставлялся более направленно к раковым клеткам. Два показателя в значительной степени определяют полезность конструкции. Эффективность загрузки показывает, сколько препарата оказывается внутри каждой частицы, а эффективность инкапсуляции измеряет, какую долю исходного лекарства удалось захватить, а не потерять. Высокие значения обоих показателей означают меньше инъекций, меньше материала-носителя и большую вероятность нанести сильный удар по опухоли, не перегружая остальную часть тела.
От метода проб и ошибок к основанному на данных проектированию
Проектировать эти нанонесители вручную — все равно что настраивать радио со множеством ручек: размер частиц, заряд поверхности, материалы, покрытия и методы приготовления взаимодействуют сложным образом. До сих пор исследователи в основном меняли по одной–две настройки и измеряли результат — медленный и дорогой цикл, который показывает лишь небольшой фрагмент общей картины. В этой работе авторы собрали 59 тщательно отобранных рецептов нанонесителей с гемцитабином из научной литературы и дополнительно обогатили их примерами, сгенерированными на компьютере с опорой на физику. Этот объединенный набор данных позволил им опробовать несколько подходов машинного обучения — компьютерных программ, которые извлекают закономерности из данных — чтобы предсказывать эффективность загрузки и инкапсуляции, исходя только из выбранных параметров конструкции.
Когда физика направляет алгоритмы
Большинство систем машинного обучения — мощные инструменты подбора кривой: они улавливают закономерности, но не понимают, когда ответ противоречит законам природы. Чтобы избежать нереалистичных прогнозов, исследователи построили гибридный метод, который сочетает данные с базовыми физическими законами о том, как молекулы лекарства перемещаются, связываются и устанавливают равновесие в замкнутой системе. В их рамке любая предсказанная величина, которая, например, предполагала бы создание лекарства в объеме, превышающем исходно внесенное, или игнорировала бы диффузию молекул через материал, мягко наказывалась во время обучения. Такой «информированный физикой» подход подталкивает модель к ответам, которые имеют химический и физический смысл, особенно в областях проектного пространства, где реальные измерения скудны.
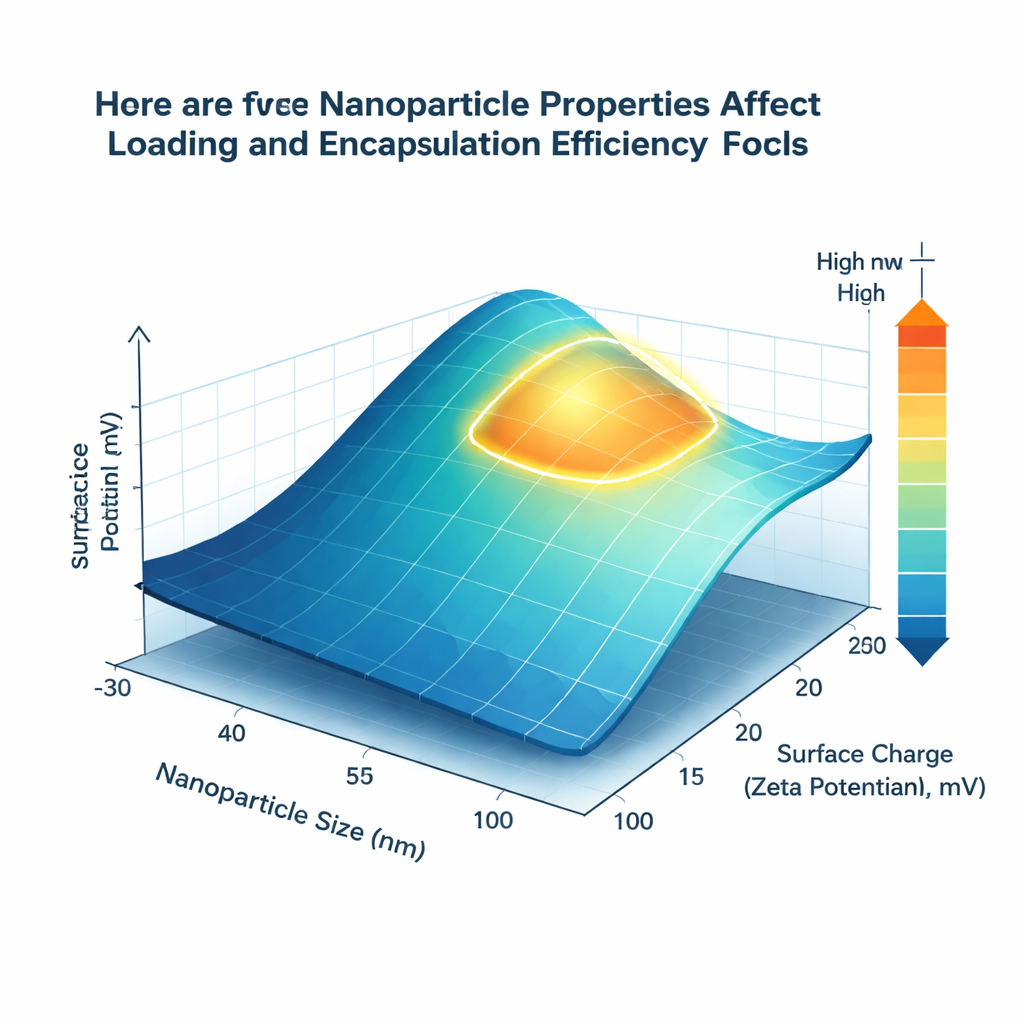
Что обнаружили модели
Среди протестированных методов наиболее точные прогнозы давал продвинутый ансамблевый алгоритм XGBoost, который близко соответствовал опубликованным экспериментальным результатам для обоих ключевых показателей. Но помимо точности команда искала понятные правила проектирования. С помощью метода SHAP, который ранжирует, насколько сильно каждый фактор подталкивает прогноз вверх или вниз, они обнаружили, что размер частиц и заряд поверхности стабильно доминируют в определении эффективности. Нанонесители диаметром примерно от 80 до 150 нанометров обеспечивали лучший баланс между площадью поверхности и внутренним объемом, повышая как загрузку, так и инкапсуляцию. Слабоположительный заряд поверхности, в диапазоне примерно +15 до +25 милливольт, был связан с лучшим захватом гемцитабина, вероятно потому, что положительно заряженные поверхности носителя благоприятно взаимодействуют с отрицательно заряженными группами лекарства.
Цифровая карта для будущих противораковых терапий
Итог — не готовое лекарство, а мощный инструмент планирования. Исследование предоставляет своего рода «карту проектирования», которая указывает исследователям рецептуры нанонесителей, с наибольшей вероятностью хорошо удерживающих и защищающих гемцитабин, одновременно отсекая миллионы безнадежных комбинаций. Авторы подчеркивают, что их прогнозы по-прежнему нужно подтверждать в новых лабораторных и животных исследованиях, а их набор данных — хотя и тщательно собранный — невелик по объему. Тем не менее эта физически ориентированная рамка машинного обучения демонстрирует, как компьютеры могут помочь сузить поиск лучших носителей противораковых препаратов, сократив расходы и ускорив путь от идей к более точным и удобным для пациентов терапиям.
Цитирование: Rahdar, A., Fathi-karkan, S. & Shirzad, M. Integrating machine learning and physics-based modeling for predictive design of gemcitabine-loaded nanocomposites. Sci Rep 16, 6268 (2026). https://doi.org/10.1038/s41598-026-37098-6
Ключевые слова: наномедицина, гемцитабин, доставка лекарств, машинное обучение, наночастицы