Clear Sky Science · ru
Автоматизированная количественная оценка лимфоцитов, инфильтрирующих опухоль, с помощью машинного обучения выявляет прогностические и иммуногеномные характеристики при раке легкого
Почему важно считать крошечные иммунные клетки в опухолях легкого
Рак легкого по‑прежнему остается одним из самых смертоносных видов рака, но не все опухоли ведут себя одинаково. Некоторые интенсивно патрулируются иммунными клетками, которые проникают внутрь опухоли, в то время как другие остаются почти нетронутыми. Эти лимфоциты, инфильтрирующие опухоль (TIL), могут подсказать, как будет развиваться заболевание и выиграет ли пациент от современных препаратов иммунотерапии. Проблема в том, что сейчас TIL обычно подсчитывают визуально под микроскопом — это медленно и субъективно. В этом исследовании задают актуальный вопрос: можно ли с помощью машинного обучения автоматически измерять эти клетки на рутинных слайдах патологии и что это раскрывает о биологии рака легкого и выживаемости пациентов?
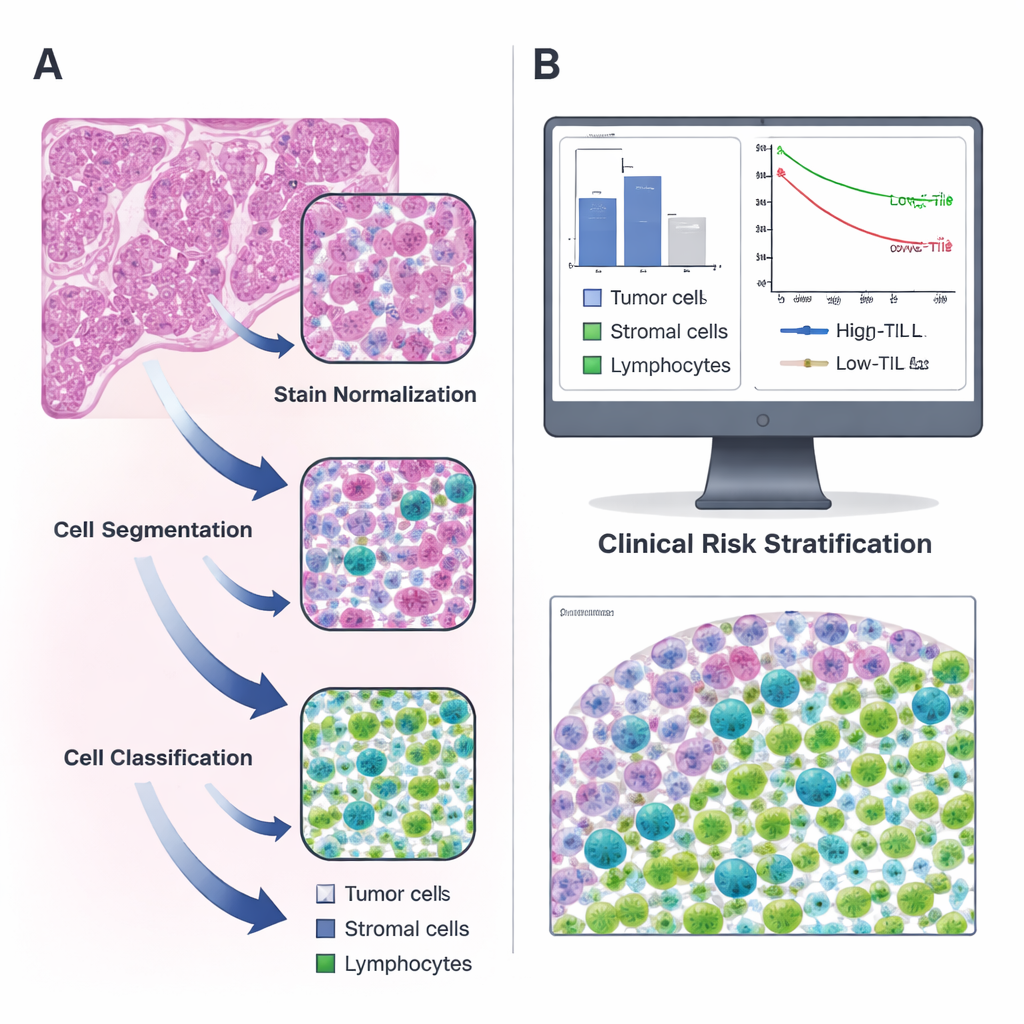
Преобразование обычных слайдов в цифровые карты
Исследователи сосредоточились на аденокарциноме легкого, распространенном типе рака легкого, используя открытые данные The Cancer Genome Atlas и независимую группу пациентов из собственной больницы. Для каждого пациента они анализировали стандартные гистологические слайды, окрашенные гематоксилином и эозином (H&E) — знакомые каждому патологоанатому розово‑фиолетовые изображения. С помощью открытого программного обеспечения QuPath они построили пошаговый конвейер: сначала корректировали цветовые различия между слайдами; затем использовали алгоритм «водораздела» для разделения перекрывающихся ядер клеток; наконец, обученный классификатор компьютера помечал каждую обнаруженную клетку как опухолевую, стромальную (вспомогательную ткань) или лимфоцит. Два эксперта‑патолога неоднократно проверяли и корректировали работу машины, пока она не научилась надежно распознавать разные типы клеток самостоятельно.
Связь числа иммунных клеток с исходами у пациентов
Когда система уверенно определяла клетки, команда подсчитала количество лимфоцитов на квадратный миллиметр опухолевой ткани у более чем 300 пациентов. Они обнаружили, что уровни TIL сильно варьируют и в среднем составляют лишь небольшую долю всех клеток. С помощью статистического подхода для выбора наиболе информативного порога исследователи установили значение 135 TIL на мм² как границу между опухолями с «высоким» и «низким» уровнем инфильтрации. Пациенты с опухолями, превышающими этот порог, жили дольше, чем те, у кого инфильтрация была скудной, и этот эффект сохранялся как в исходной, так и в валидационной когортах. Иными словами, простая числовая оценка, полученная автоматически, отражала значимые различия в выживаемости, подтверждая более ранние, более трудоемкие исследования с ручным подсчетом.
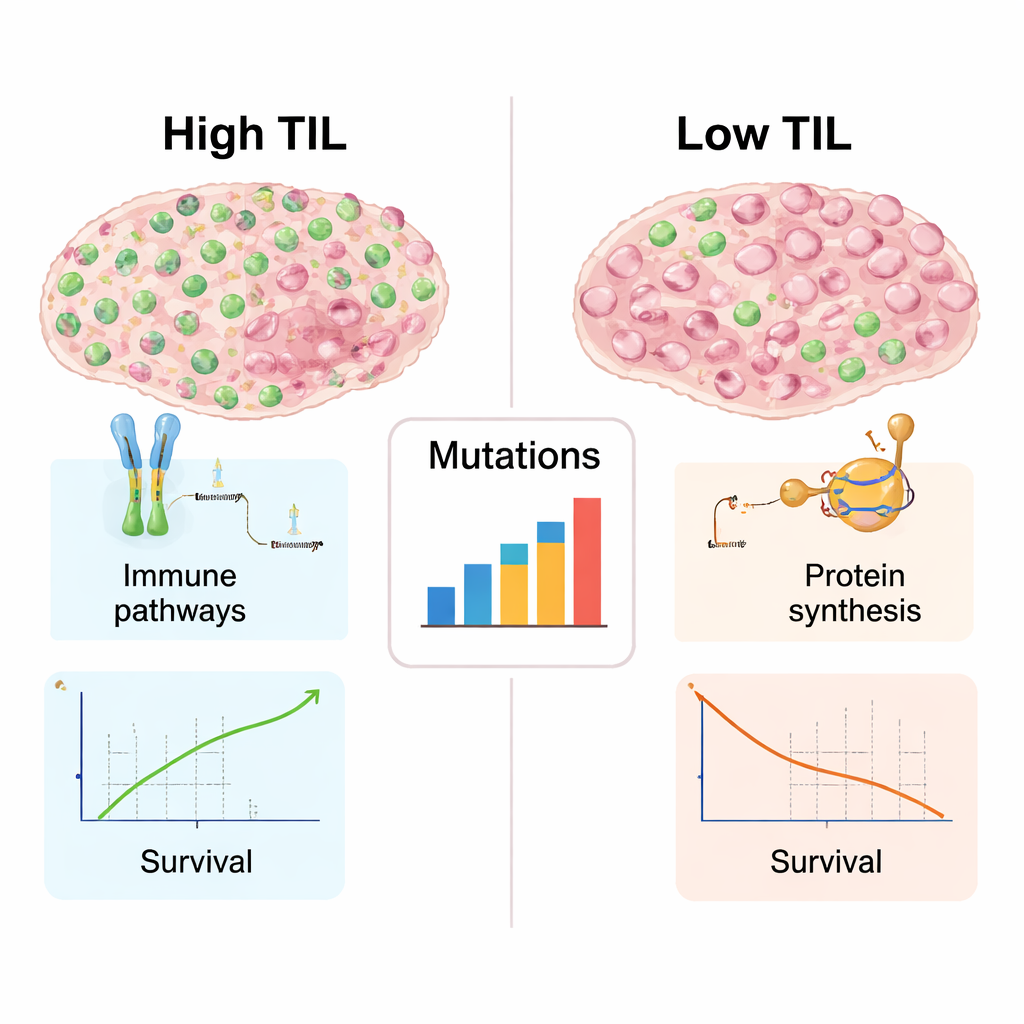
Как выглядят опухоли, богатые иммунными клетками, «под капотом»
Поскольку для многих опухолей были доступны генетические и молекулярные данные, авторы могли изучить, чем отличаются опухоли с высоким TIL от опухолей с низким TIL помимо простого подсчета клеток. Опухоли, в изобилии населенные лимфоцитами, демонстрировали более выраженные сигнатуры иммунной активности: более активно работали гены, вовлеченные в распознавание аномальных белков, презентацию антигенов Т‑клеткам и координацию иммунной атаки. Эти опухоли также имели более разнообразный набор ДНК‑мутаций, которые способны создавать новые мишени для иммунной системы. Напротив, опухоли с низким уровнем TIL преимущественно активировали гены, связанные со сборкой рибосом и синтезом белка — признак мощной клеточной машины роста при относительно тихом иммунном участии. Это разделение отражает теперь уже привычный контраст между «горячими» опухолями, богатыми иммунными клетками и более склонными к ответу на иммунотерапию, и «холодными» опухолями, которые иммунная система в основном игнорирует.
Обучение компьютера предсказывать иммунный статус
Команда пошла дальше и проверила, может ли компактный набор признаков изображения предсказать, относится ли опухоль к категории с высоким или низким TIL без явного подсчета каждого лимфоцита. Они суммировали тонкие текстурные паттерны на слайдах — то, как меняется интенсивность пикселей в небольших окрестностях — в так называемые признаки Харалика, и объединили их со клиническим стадированием опухоли в модели случайного леса. В кросс‑валидации этот классификатор с высокой точностью разделял опухоли на высоко‑ и низко‑TIL, а в независимой больничной когорте сохранял разумную работоспособность. Важно, что весь подход работает на стандартных компьютерах с бесплатным ПО, что предполагает возможность внедрения в многие лаборатории патологии без специализированного оборудования.
Что это значит для будущего лечения рака легкого
Для неспециалиста ключевой вывод таков: компьютер может научиться «читать» рутинные слайды рака легкого таким образом, чтобы отразить силу включения иммунной системы в борьбу с опухолью. Высокие уровни инфильтрирующих лимфоцитов сигнализируют об активной иммунной реакции, более богатом ландшафте мутаций и лучшей общей выживаемости. Хотя требуется дополнительная работа — особенно в группах пациентов, действительно лечившихся иммунотерапией — этот автоматизированный метод в перспективе может помочь врачам быстро и последовательно отнести опухоли к иммунным категориям «горячие» и «холодные». Это, в свою очередь, может направлять решения о том, кто с большей вероятностью получит пользу от иммунных методов лечения, и стимулировать новые стратегии по превращению холодных опухолей в горячие.
Цитирование: Li, A., Pang, Y., Zhang, H. et al. Automated quantification of tumor-infiltrating lymphocytes by machine learning reveals prognostic and immunogenomic features in lung cancer. Sci Rep 16, 7006 (2026). https://doi.org/10.1038/s41598-026-37076-y
Ключевые слова: аденокарцинома легкого, лимфоциты, инфильтрирующие опухоль, машинное обучение, цифровая патология, иммунная терапия рака