Clear Sky Science · ru
Прогнозирование выживаемости почечного трансплантата с помощью модели машинного обучения на основе транскриптомики биопсий по показаниям
Почему это важно для пациентов с трансплантатом
Для людей с почечной недостаточностью трансплантация может означать переход от жизни на диализе к возвращению к обычным делам. Тем не менее многие пересаженные почки все равно теряют функцию через годы после операции, часто из‑за того, что иммунная система организма постепенно атакует новый орган. В этом исследовании изучается, можно ли объединить паттерны активности генов из рутинных почечных биопсий с современными методами машинного обучения, чтобы выявлять трансплантаты, находящиеся в реальной опасности, задолго до того, как стандартные тесты фиксируют проблемы.
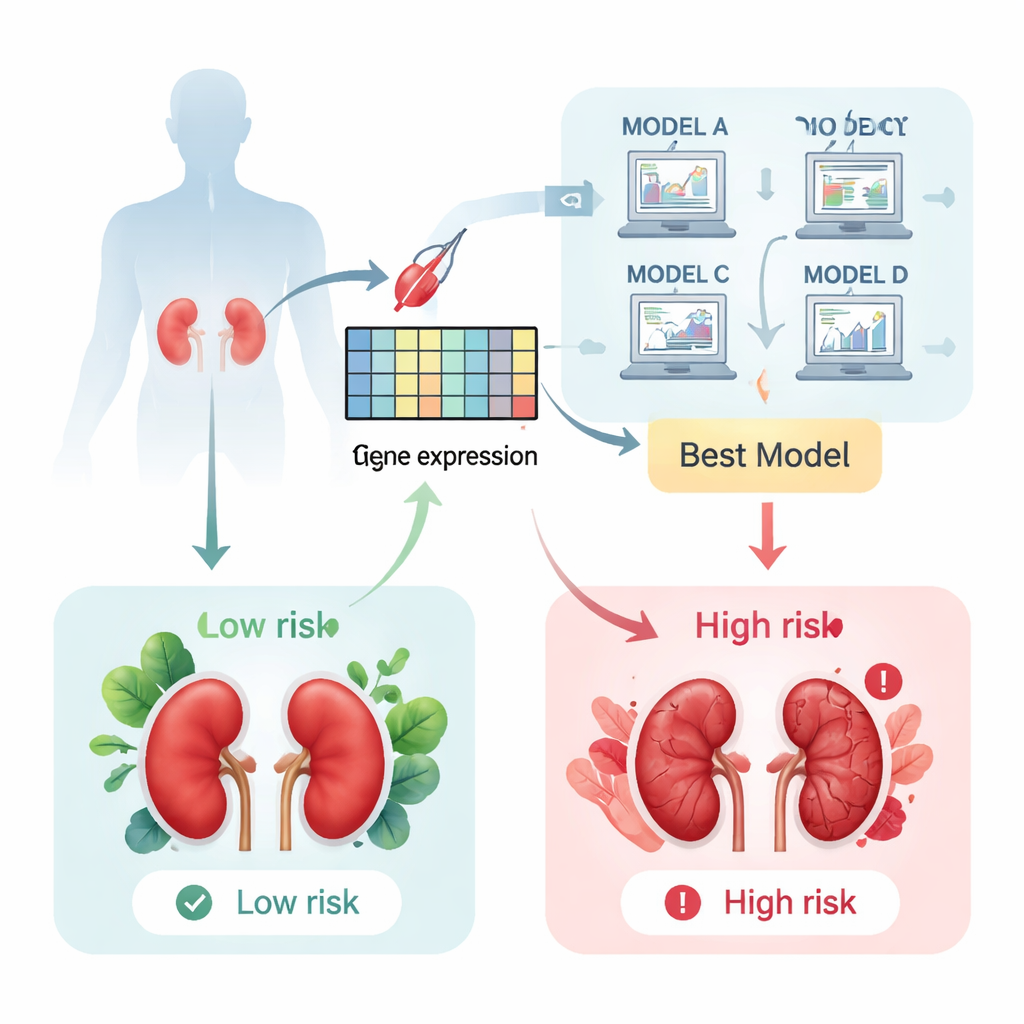
Заглядывая в трансплантат на молекулярном уровне
После трансплантации почки врачи иногда проводят биопсию «по показаниям», когда анализы крови или мочи указывают на возможный стресс органа. Традиционно патологи оценивают эти образцы под микроскопом, чтобы определить степень повреждения. Авторы работы задали иной вопрос: могут ли гены, активированные в этих биопсийных образцах, дать более ясный и ранний сигнал о будущем отторжении? Чтобы ответить на этот вопрос, они собрали данные активности генов более чем из 1 200 биопсий из шести международных исследовательских коллекций и сосредоточились на пациентах, у которых трансплантат либо сохранил функцию, либо впоследствии отказал.
Нахождение 11‑генного предупредительного сигнала
Исследователи сначала сравнили образцы биопсий пациентов, у которых в итоге произошла потеря трансплантата, с образцами тех, у кого функция сохранилась. Они проанализировали тысячи генов и выделили небольшую группу из 11, которые последовательно были более активны в неудавшихся трансплантатах. Эти гены тесно связаны с иммунной активацией и воспалением, включая сигналы, привлекающие лейкоциты в почку и способствующие их атаке на ткани. Иными словами, биопсии почек, которые позже ресорбировались, уже были «подсвечены» агрессивным иммунным профилем, даже когда традиционные показатели могли выглядеть удовлетворительными.
Обучение машин прогнозированию выживаемости трансплантата
Далее команда ввела уровни активности этих 11 генов в широкий набор подходов машинного обучения, предназначенных для предсказания того, как долго пересаженная почка будет функционировать. Они протестировали 117 различных конфигураций моделей и оценивали их по способности ранжировать пациентов от наименьшего к наибольшему риску потери трансплантата. Лучшей оказалась одна из разновидностей алгоритмов — градиентный бустинг (Gradient Boosting Machine), которая с высокой точностью упорядочивала пациентов по риску. Когда модель присваивала высокий риск, такие пациенты с гораздо большей вероятностью теряли трансплантат в течение следующих нескольких лет по сравнению с пациентами с низкими баллами, что подтверждалось резким расхождением кривых выживаемости во времени.
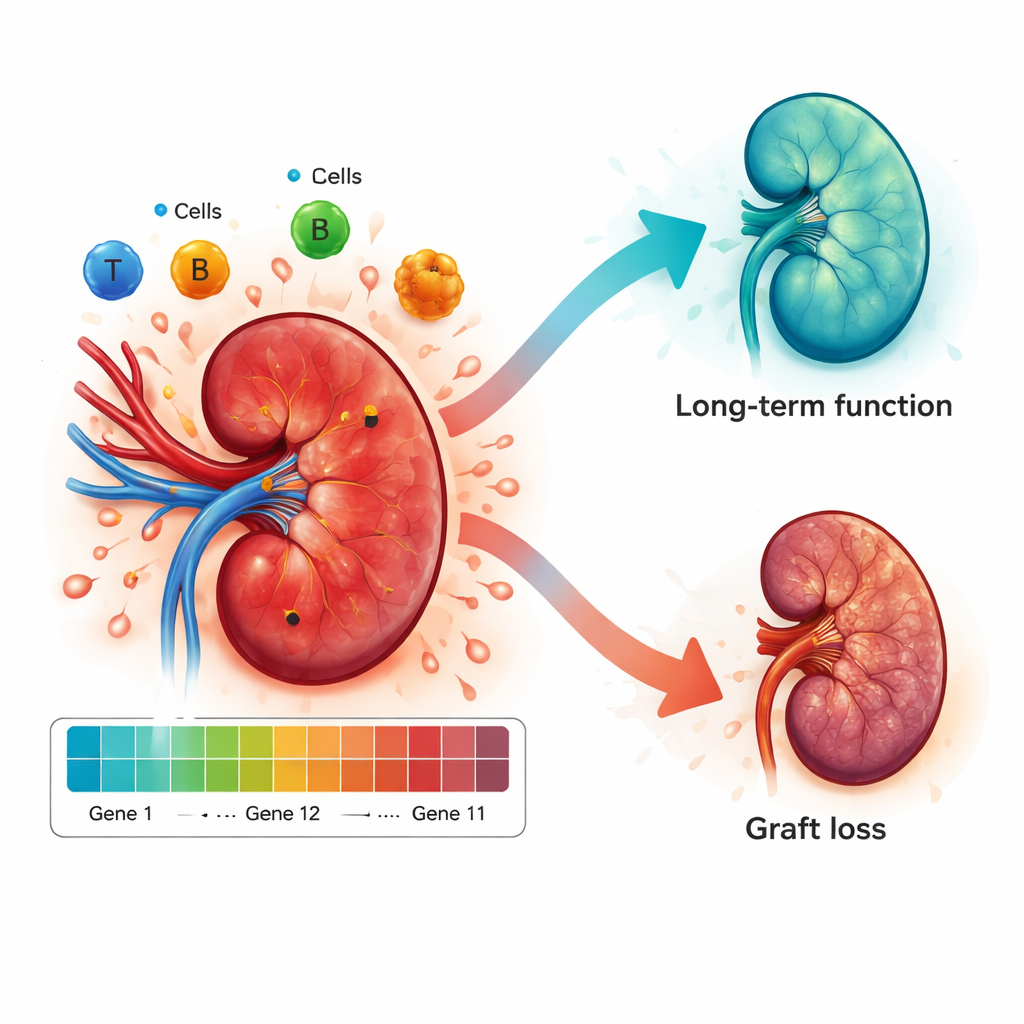
Проверка работы на новых когортах пациентов
Чтобы инструмент был полезен в клинике, он должен работать вне данных, на которых его создали. Авторы поэтому применили свою 11‑генную модель к четырем полностью независимым коллекциям биопсий из других центров. В этих группах подробные времена до события были не всегда доступны, но эксперты помечали каждую биопсию как проявляющую отторжение или нет. Тот же геномный скор хорошо различал отторжение и стабильные трансплантаты, с показателями точности, сопоставимыми со многими клиническими тестами. В отдельном исследовании, где пациентам планово брали биопсии в 0, 6 и 24 месяца после трансплантации, у тех, у кого позже развился хронический ущерб, уже за месяцы до микроскопически очевидных изменений были повышенные баллы риска.
Что модель сообщает о иммунном противостоянии
Помимо прогноза, исследователи использовали паттерны экспрессии генов, чтобы заглянуть в иммунный ландшафт внутри почки. Биопсии с высокими баллами риска демонстрировали больше агрессивных типов иммунных клеток, таких как определенные макрофаги и Т‑лимфоциты, а также более выраженные химические сигналы, привлекающие их в орган. Биопсии с низким риском, напротив, были богаче клетками, связанными с подавлением воспаления и восстановлением ткани. Это говорит о том, что модель не просто «черный ящик»: ее оценка риска отражает реальные биологические процессы, которые либо двигают почку к отторжению, либо поддерживают долгосрочный мир между органом и иммунной системой реципиента.
Как это может изменить уход за трансплантатами
В работе делается вывод, что 11‑генный скор, основанный на машинном обучении и рассчитанный по рутинным почечным биопсиям, способен надежно прогнозировать, какие трансплантаты с наибольшей вероятностью потеряют функцию, и выявлять проблемы раньше стандартных методов. Для пациентов и клиницистов такой инструмент в будущем мог бы направлять персонализированную тактику: пациентам с высоким риском — более частое наблюдение или адаптация медикаментозной терапии, а пациентам с низким риском — избегание ненужных вмешательств. Поскольку сигнатура включает лишь небольшой набор генов, ее можно перевести в практические лабораторные тесты с использованием существующих технологий. Хотя прежде чем это станет частью повседневной практики, потребуются дополнительные проспективные исследования, эта работа указывает на будущее, в котором молекулярные данные и искусственный интеллект помогают защищать пересаженные почки в долгосрочной перспективе.
Цитирование: Filho, V.O.C., Passos, P.R.C., de Andrade, L.G.M. et al. Predicting kidney graft survival with a machine learning model based on for-cause biopsy transcriptomics. Sci Rep 16, 6157 (2026). https://doi.org/10.1038/s41598-026-37038-4
Ключевые слова: трансплантация почки, выживаемость трансплантата, машинное обучение, экспрессия генов в биопсии, иммунное отторжение