Clear Sky Science · ru
Прогнозирование геморрагической трансформации после тромбэктомии с помощью количественной ДСА и машинного обучения
Почему это важно для пациентов с инсультом
Когда у человека случается крупный инсульт, врачи иногда могут извлечь сгусток из главной артерии мозга с помощью миниатюрного устройства в процедуре, называемой механической тромбэктомией. Это кардинально изменило лечение инсульта, но многие пациенты по‑прежнему получают неблагоприятный исход, потому что у некоторых развивается новое кровотечение в мозге. Исследование, лежащее в основе этой статьи, задаёт простой, но ключевой вопрос: можно ли на основе информации, которую врачи уже получают в операционной, и современных методов машинного обучения предсказать, у каких пациентов наиболее высок риск кровоизлияния и кому нужна дополнительная защита?
Смотреть дальше, чем «артерия открыта или закрыта»
Сегодня успех тромбэктомии обычно оценивают по тому, выглядит ли восстановленная артерия открытой на ангиографии — своего рода рентгеновском «фильме» сосудов в реальном времени. Но такая грубая оценка не показывает, что происходит в мелких дистальных сосудах мозга, где фактически возникают повреждение и кровотечение. Некоторые пациенты при идеально восстановленной магистральной проходимости всё же развивают тяжёлое мозговое кровоизлияние, называемое геморрагической трансформацией. Авторы предположили, что более детальные количественные измерения кровотока в этих малых сосудах, полученные из той же ангиограммы, могут содержать скрытые подсказки о риске.
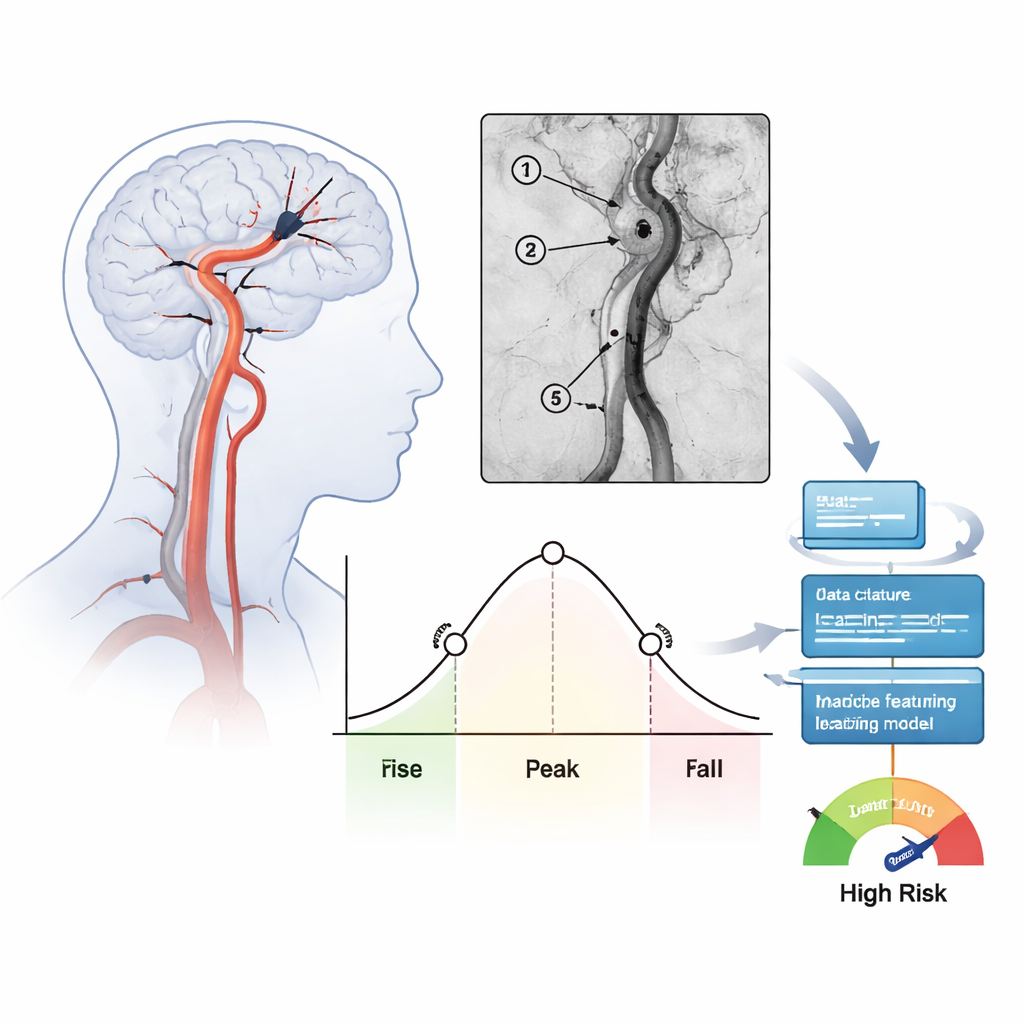
Преобразование «фильмов» ангиографии в числа
Команда изучила 171 человека, лечившегося от тяжёлых инсультов переднего мозга в течение года в одном центре. После удаления тромба и восстановления кровотока записывались стандартные ангиографические проекции, а затем анализировалось, как введённый контрастный препарат заполнял и опорожнялся в нескольких ключевых точках вдоль леченой артерии. Для каждой области рассчитывали временные показатели — например, среднее время транзита (how long blood needed to pass through) и ширину основного пика контраста на уровне половины максимума (full width at half maximum). Эти величины суммируют, движется ли кровь медленно и равномерно или проходит быстро и узким импульсом. В сумме для каждого пациента извлекли 39 таких характеристик кровотока и проверили их согласованность между независимыми рейтерами.
Обучая компьютер распознавать опасные шаблоны
Затем исследователи использовали набор распространённых методов машинного обучения, чтобы проверить, могут ли эти характеристики кровотока сами по себе или в сочетании с базовыми клиническими данными (например, возрастом и тяжестью инсульта) отличать пациентов, у которых позднее развилось мозговое кровотечение, от тех, у кого его не было. Чтобы избежать переобучения, они сначала применили пять различных методов отбора признаков для выбора наиболее информативных измерений и неоднократно делили данные на обучающую и тестовую выборки с перекрёстной проверкой. Среди множества протестированных комбинаций лучше всего показала себя относительно простая модель — логистическая регрессия, настроенная с фильтром признаков «Elastic Net». При использовании только ангиографически полученных показателей кровотока модель в среднем разделяла пациентов с кровотечением и без него с площадью под ROC‑кривой примерно 0,81. При добавлении клинических факторов производительность выросла до примерно 0,86, что говорит о потенциальной полезности модели как инструмента принятия решений.
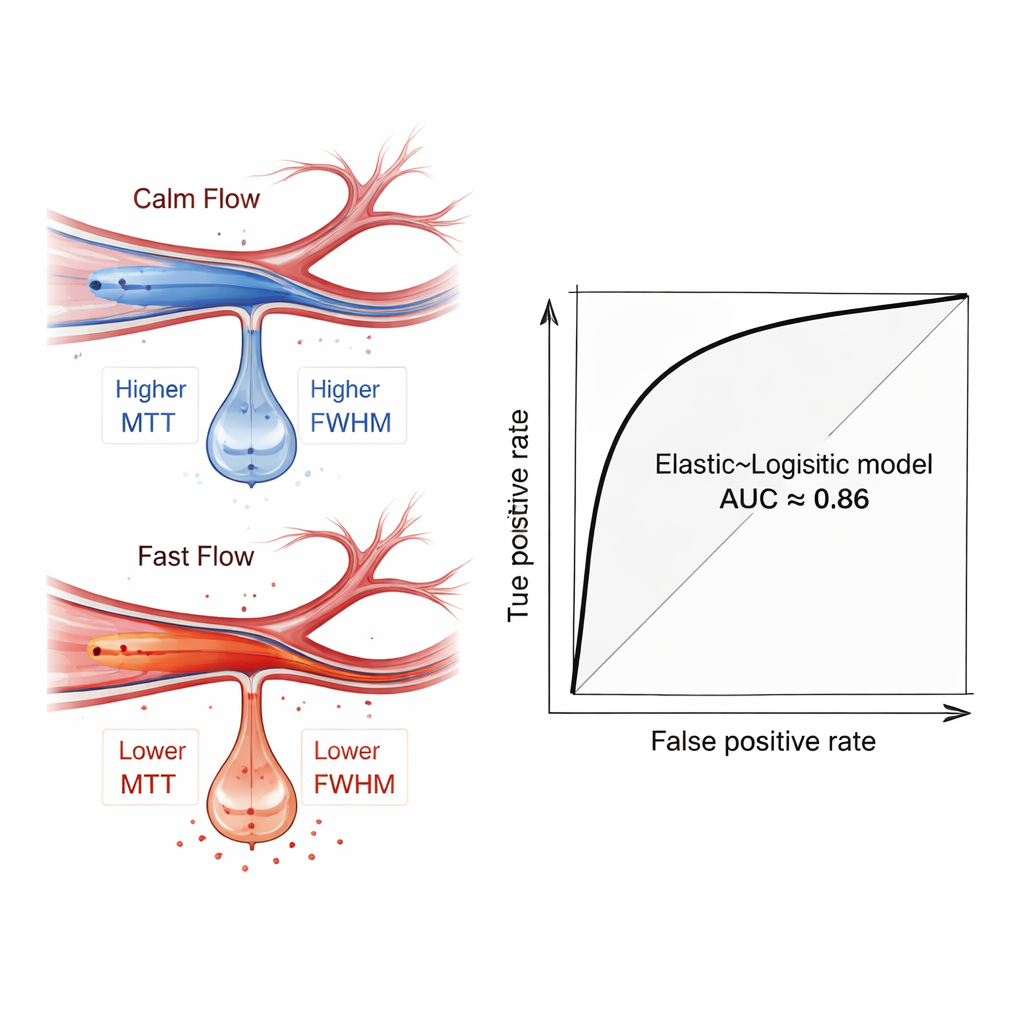
Что показали сигналы кровотока
Анализировав обученные модели, авторы применили метод интерпретируемости SHAP, чтобы выяснить, какие признаки имели наибольшее значение. Наибольшую роль играли показатели, отражающие длительность и растянутость пульса кровотока — особенно в более дистальной ветви средней мозговой артерии. Пациенты с последующим кровоизлиянием, как правило, демонстрировали более быстрый, более сфокусированный поток в этих дистальных сосудах — это проявлялось в меньших временах транзита и уже выраженных пиках. Такой паттерн можно рассматривать как гемодинамический «отпечаток» гиперперфузии, состояния, при котором ослабленная ткань мозга, внезапно подвергшаяся сильному притоку крови после ишемии, более склонна к протеканию и кровоточивости. Важно, что этот сигнал проявился даже тогда, когда простые групповые сравнения не выявляли сильных статистических различий, подчёркивая ценность многопризнакового анализа с помощью машин.
Как это может изменить уход у постели больного
Поскольку метод использует изображения, уже получаемые во время тромбэктомии, он не требует дополнительных сканирований, контраста или облучения. Как только задаются области интереса — шаг, который в настоящее время занимает несколько минут — компьютер автоматически вычисляет показатели кровотока и выдаёт персонализированную оценку риска кровотечения. В принципе это может помочь врачам устанавливать целевые значения артериального давления, решать, насколько агрессивно применять антикоагулянты, и планировать более ранние КТ‑сканирования для пациентов, помеченных как высокого риска. Авторы отмечают, что их исследование ретроспективно и выполнено в одном центре, поэтому прежде чем инструмент начнёт применяться в рутинной практике, нужны более крупные многоцентровые исследования. Тем не менее работа даёт ясное доказательство концепции: превращая ангиограммы при инсульте в богатые числовые данные и позволяя машинному обучению их анализировать, мы можем перейти от простого вопроса «Открыта ли артерия?» к вопросу «Безопасна ли микроциркуляция мозга?» — сдвигу, который в конечном счёте может уберечь больше пациентов от опасных послеоперационных кровотечений.
Цитирование: Li, H., Pang, C., Guo, X. et al. Machine learning-enabled prediction of hemorrhagic transformation post-thrombectomy using quantitative DSA. Sci Rep 16, 6008 (2026). https://doi.org/10.1038/s41598-026-37036-6
Ключевые слова: инсульт, механическая тромбэктомия, кровоизлияние в мозг, машинное обучение, ангиография