Clear Sky Science · ru
Влияние системных методов лечения, специфичных для нейроэндокринных новообразований, на экспрессию и функцию CXCR4 в клетках нейроэндокринных опухолей
Почему это важно для будущего онкологической помощи
Когда некоторые редкие опухоли кишечника и поджелудочной железы становятся более агрессивными, они часто перестают реагировать на стандартные таргетные препараты. Врачам и исследователям срочно нужны новые способы обнаружения и поражения таких резистентных опухолей. В этом исследовании поставлен практический вопрос с большими последствиями: изменяют ли химио‑ и таргетные препараты, которые пациенты уже получают, ключевой опухолевый маркер CXCR4, который разрабатывается и как диагностический «маяк», и как терапевтическая мишень?
Сдвиг мишени на агрессивных опухолевых клетках
Нейроэндокринные новообразования — это редкие раковые образования, возникающие из гормонопродуцирующих клеток, чаще всего в кишечнике и поджелудочной железе. В своей ранней, более упорядоченной форме эти опухоли обычно экспрессируют молекулу на поверхности — рецептор соматостатина 2, который врачи могут визуализировать и лечить специализированными радионуклидными препаратами. По мере перехода в более агрессивную стадию эти опухоли склонны терять этот маркер, что затрудняет их обнаружение и таргетирование. Одновременно многие из них включают другую поверхностную молекулу — рецептор CXCR4, связанный с более быстрым ростом, метастазированием и худшим прогнозом. Поскольку CXCR4 можно визуализировать с помощью ПЭТ‑трассера и потенциально поражать радиоактивными или антителозависимыми препаратами, он стал многообещающей «резервной» мишенью, когда стандартные опции исчерпаны.
Тестирование реальных препаратов в моделях опухолевых клеток
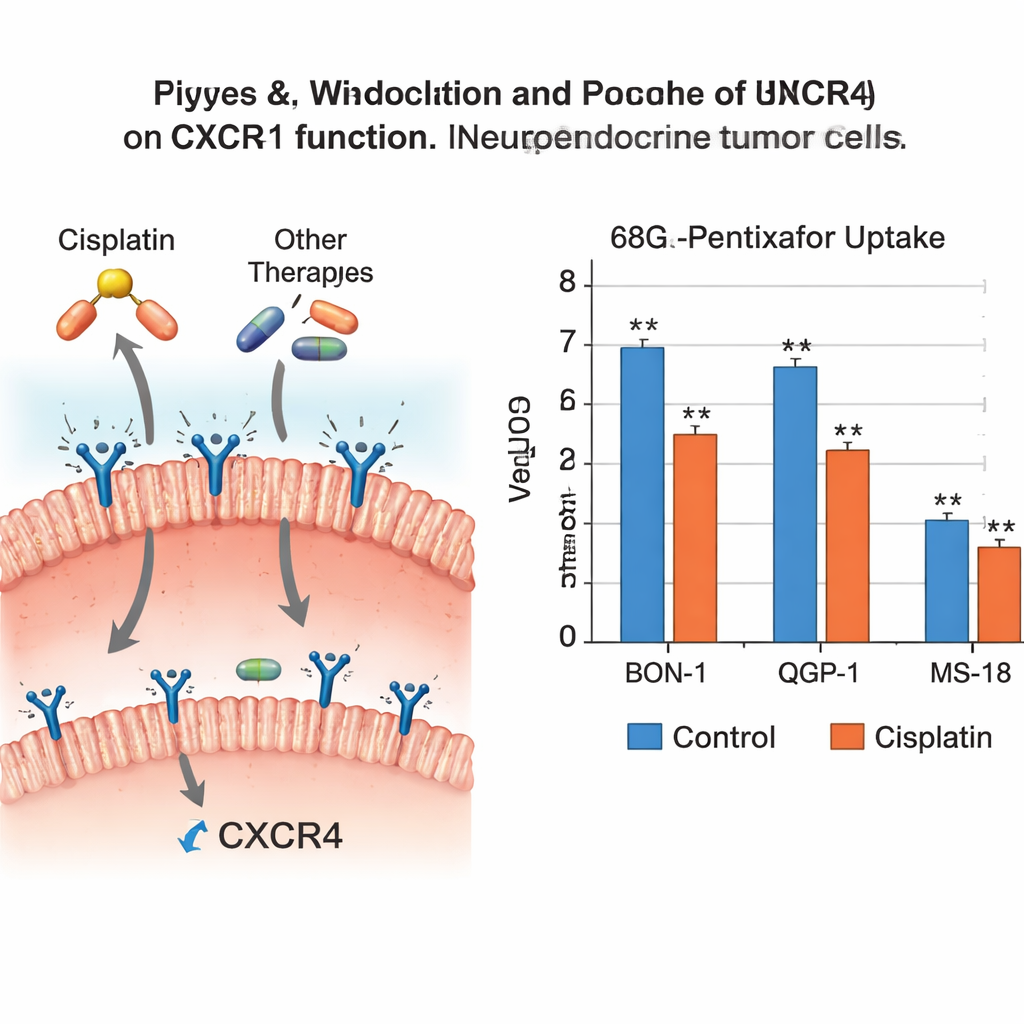
Исследователи хотели выяснить, как препараты, уже используемые для лечения высокодифференцированных нейроэндокринных опухолей, влияют непосредственно на CXCR4. Если эти лекарства случайно снижают CXCR4, они могут ослабить будущую визуализацию или терапию, нацеленную на CXCR4 — но в то же время это может способствовать сдерживанию агрессивности опухоли. Команда работала с тремя различными линиями человеческих опухолевых клеток, представляющими агрессивные формы заболевания, включая одну гибридную линию, которая близко имитирует особенно трудноизлечимые опухоли. Клетки подвергали воздействию шести распространённых препаратов: химиопрепаратов цисплатина, этопозида, стрептозотоцина, 5‑фторурацила, перорального темозоломида и таргетного ингибитора mTOR эверолимуса. После лечения измеряли CXCR4 на уровне генов и белка и тестировали, насколько хорошо клетки способны захватывать ПЭТ‑трассер, направленный на CXCR4.
Некоторые препараты снижают сигнал CXCR4
Результаты показали, что не все противораковые лекарства действуют одинаково в отношении этого рецептора. Цисплатин явно снижал генетическую активность CXCR4 в двух из трёх клеточных линий и значительно уменьшал захват трассера в двух линиях, что означает меньше работоспособных рецепторов для связывания трассера. Темозоломид и эверолимус также снижали уровни CXCR4 на генетическом и белковом уровнях в нескольких типах клеток, хотя это не всегда приводило к статистически значимому падению захвата трассера. В противоположность этому этопозид и стрептозотоцин мало влияли на CXCR4, а 5‑фторурацил вызывал умеренные изменения, которые существенно не меняли связывание трассера. В целом картина указывает, что цисплатин, темозоломид и эверолимус способны подавлять CXCR4 в этих агрессивных опухолевых клетках, тогда как другие препараты в основном оставляют его без изменений.
Что это значит для планирования сканирования и времени лечения
Эти наблюдения несут двойное послание для будущей помощи пациентам. С одной стороны, подавление CXCR4 может быть частью механизма, с помощью которого такие препараты, как цисплатин, темозоломид и эверолимус, замедляют распространение опухоли, поскольку высокая экспрессия CXCR4 связана с инвазивностью и метастазированием. С другой стороны, если CXCR4 опухоли подавлен текущим лечением, ПЭТ‑сканы, нацеленные на CXCR4, могут недооценивать объём заболевания, а радиотерапии, ориентированные на CXCR4, будут иметь меньше участков для «докинга». Исследование предполагает, что одновременное применение CXCR4‑таргетных терапий вместе с этими системными препаратами вряд ли усилит эффективность CXCR4‑фокусированных подходов и даже может ослабить их.
Новый фрагмент в головоломке персонализированной терапии
Для неспециалистов главный вывод таков: один опухолевый маркер может играть сразу две роли — быть предвестником агрессивного течения болезни и одновременно удобной точкой для визуализации и таргетной терапии. Это исследование показывает, что некоторые устоявшиеся противораковые препараты способны незаметно корректировать уровень такого маркера в ту или иную сторону. На практике это может влиять на выбор времени для проведения ПЭТ‑сканов и применения терапий, нацеленных на CXCR4 — предпочтительно тогда, когда рецептор наиболее выражен — и помогать объяснить, почему определённые терапии эффективны против быстрорастущих нейроэндокринных опухолей. Хотя эти результаты получены в клеточных моделях и требуют подтверждения у пациентов, они представляют важный шаг к более разумной последовательности лечения для людей с этими сложными опухолями.
Цитирование: Däubler, C., Böttcher, C., Landwehr, LS. et al. Impact of neuroendocrine neoplasm-specific systemic treatments on expression and function of CXCR4 in neuroendocrine tumor cells. Sci Rep 16, 4339 (2026). https://doi.org/10.1038/s41598-026-37026-8
Ключевые слова: нейроэндокринные опухоли, CXCR4, цисплатин, эверолимус, таргетная визуализация