Clear Sky Science · ru
Электрохимический биосенсор на основе M13-фага и rGO для быстрого обнаружения вирусного белка в сложных матрицах
Почему быстрые тесты на вирусы всё ещё важны
Пандемия COVID-19 показала, насколько важно быстро выявлять вирусы — не только у пациентов, но и в таких местах, как сточные воды или линии переработки пищевых продуктов. Современные лабораторные методы мощные, но могут быть медленными, дорогими и зависящими от хрупких биологических компонентов, которые трудно транспортировать и хранить. В настоящей работе представлен новый тип миниатюрного электронного сенсора, использующего модифицированные вирусы и пласт углеродного материала высокой технологии, который способен зафиксировать ключевой белок SARS‑CoV‑2 менее чем за секунду, даже в «грязных» реальных образцах, таких как сыворотка крови, молоко и сточные воды.
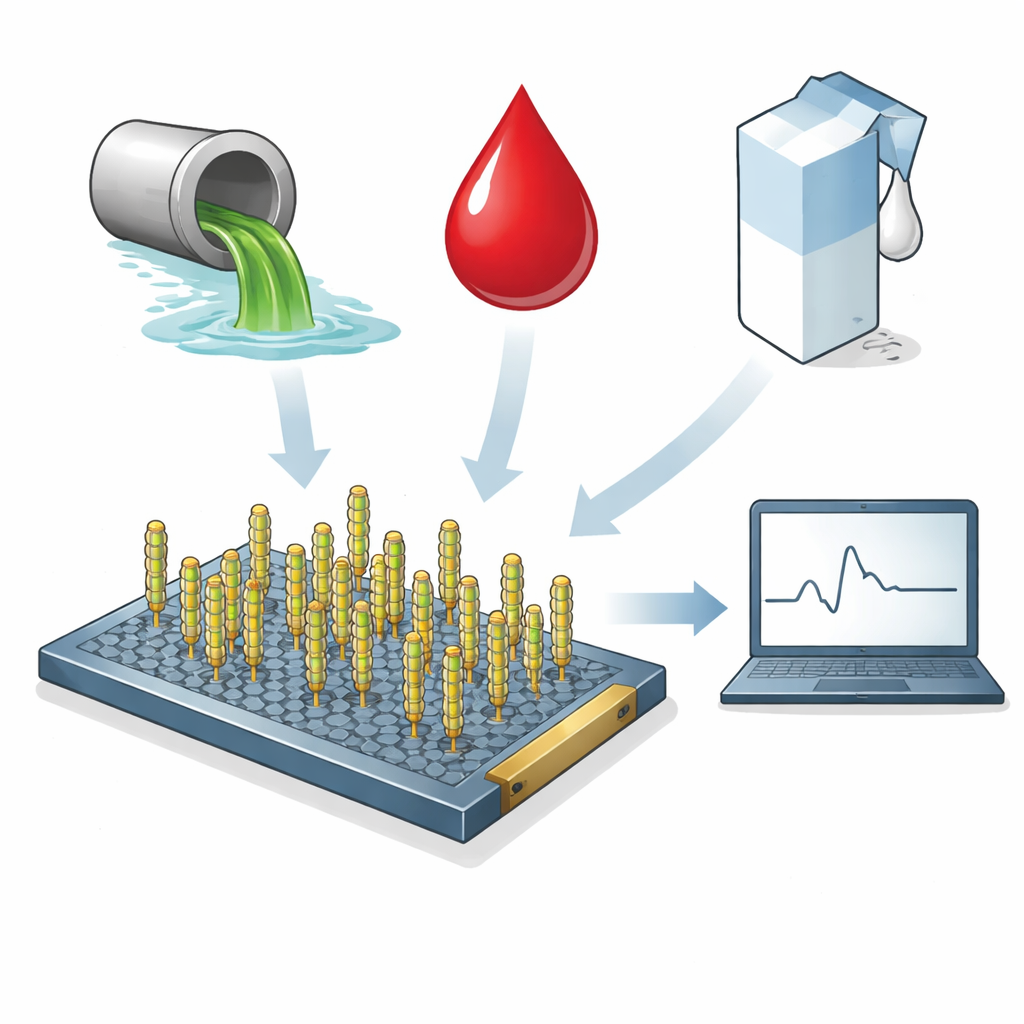
Преобразование безвредного вируса в «умный» детектор
В основе устройства — M13, безвредный фаг, который обычно инфицирует бактерии. Его длинное стержневидное тело покрыто множеством одинаковых оболочечных белков, которые учёные могут перепрограммировать генетически. Команда вставила короткий специально разработанный пептид в один из этих белков, чтобы частицы M13 распознавали и прикреплялись к фрагменту S1 шиповидного белка коронавируса. Вторая версия вируса с перемешанным (scrambled) пептидом использовалась как контроль, чтобы показать, что ответ обусловлен специфическим распознаванием, а не случайным прилипанием.
Опора на лист толщиной в атом
Чтобы превратить программируемый вирус в сенсор, исследователи прикрепили его к плоской плёнке восстановленного оксида графена (reduced graphene oxide, rGO) — высокопроводящей форме углерода, получаемой химической обработкой графита. После нанесения оксида графена на небольшие стеклянные чипы и термической обработки для его восстановления в rGO они добавили связывающую молекулу, которая прочно прикрепляется к углеродной поверхности и одновременно связывается с аминогруппами вируса. Это создало плотный слой частиц M13, закреплённых на проводящем слое. Сканирующая электронная микроскопия и атомно-силовая микроскопия подтвердили, что каждый этап изготовления изменял поверхность ожидаемым образом, а электрические измерения показали, что добавление связки и затем вируса последовательно увеличивало сопротивление — признак успешного покрытия поверхности.
Чтение связывания вируса как электрического импульса
В отличие от многих биосенсоров, которым требуются добавочные химикаты или подвижные элементы, эта платформа работает как простой резистор при малом постоянном напряжении. Когда белок S1 попадает на поверхность, покрытую вирусом, и связывается с отображаемым пептидом, он слегка меняет поведение переноса заряда через графеновый слой. Это проявляется как кратковременный всплеск электрического тока, появляющийся примерно через 300 миллисекунд после нанесения капли образца на чип, а затем исчезающий по мере установления равновесия. При настройке приложенного напряжения команда нашла «золотую точку» примерно при −0,8 милливольта, где сигнал от истинного связывания S1 был сильным, а фоновый шум и отклики на несвязанные белки, такие как бычий сывороточный альбумин, оставались низкими.
Работа в сложных реальных образцах
Затем исследователи испытали сенсор на типичных сложных смесях, которые часто выводят из строя чувствительные лабораторные реагенты. Они тестировали устройство в буфере, городских сточных водах, фетальной бычьей сыворотке (как модель крови) и пастеризованном молоке, с добавленным S1 и без него. Используя статистически определённый порог для положительного результата, сенсор обнаруживал чрезвычайно низкие уровни белка в простом буфере — до порядка 10⁻⁴ пикограмм на миллилитр — что сопоставимо с многочисленными системами на основе антител или превосходит их. В сточных водах устройство надёжно помечало более высокие уровни S1, тогда как в сыворотке и молоке оно последовательно фиксировало более низкие концентрации, причём всё это происходило за доли секунды. Важно, что контрольный сенсор с перемешанным фагом почти не реагировал на S1, подтверждая, что сигнал зависит от сконструированной последовательности связывания. Параллельный сенсор с обычным антителом на той же графеновой платформе показал сопоставимую работу, что указывает на то, что система на основе фага может соперничать с антителами по чувствительности при потенциально более низкой стоимости и простоте производства.

Что это может значить для повседневного тестирования
Антитела, являющиеся основой многих диагностических тестов, дороги в производстве, чувствительны к теплу и обычно требуют холодовой цепи от завода до клиники. Напротив, фаги M13 можно выращивать в бактериях как простую культуру, они более устойчивы к суровым условиям и их можно перепрограммировать, изменяя генетический код. Объединив эту устойчивость и гибкость с быстрым, энергоэффективным электронным считыванием на графене, работа прокладывает путь к портативным, недорогим приборам, которые можно адаптировать для обнаружения различных маркеров заболеваний или загрязнителей просто путём замены отображаемого пептида. Исследование пока находится на этапе доказательства концепции и ещё не тестировалось на клинических образцах человека, но оно указывает на будущее, в котором ручные сенсоры смогут в течение секунд скринировать вирусные белки и другие биомаркеры в клиниках, в канализационных системах или даже в пищевых продуктах без логистических сложностей традиционных тестов на антителах.
Цитирование: Alshehhi, H.Y., Tizani, L., Palanisamy, S. et al. An engineered M13 phage–rGO electrochemical biosensor for rapid detection of viral protein in complex matrices. Sci Rep 16, 9279 (2026). https://doi.org/10.1038/s41598-026-37008-w
Ключевые слова: биосенсор, графен, бактериофаг, SARS-CoV-2, электрохимическое обнаружение