Clear Sky Science · ru
Антимикробные наночастицы широкого спектра с низкой токсичностью для предотвращения образования биопленок на урологических устройствах
Почему медицинские импланты иногда оборачиваются против нас
Современная медицина опирается на пластиковые трубки и импланты для отведения мочи, поддержки блокированных почек и восстановления сексуальной функции. Но эти же устройства могут привлекать бактерии, которые формируют скользкие защитные сообщества — биопленки. Как только биопленка образуется, инфекцию трудно лечить, и часто врачам приходится удалять или заменять устройство. В этом исследовании изучается новый тип микроскопического покрытия из золота и серебра в углеродной оболочке, разработанный для того, чтобы предотвращать образование биопленок на раннем этапе.
Скрытая проблема липких микробов
Катетеры, уретеральные стенты и надувные пенильные протезы помогают сотням тысяч пациентов, но одновременно обеспечивают идеальную среду для микроорганизмов. Бактерии прикрепляются к поверхности устройства и выделяют клейкую матрицу из сахаров, белков и липидов, формируя фортификацию, которая защищает их от антибиотиков и иммунной системы. В результате инфекции, связанные с устройствами, составляют более четверти всех внутрибольничных инфекций и обходятся в сотни миллионов долларов ежегодно. Существующие защитные покрытия на основе антибиотиков или простого серебра испытывают трудности с предотвращением биопленок в долгосрочной перспективе и могут способствовать росту устойчивости к антибиотикам.
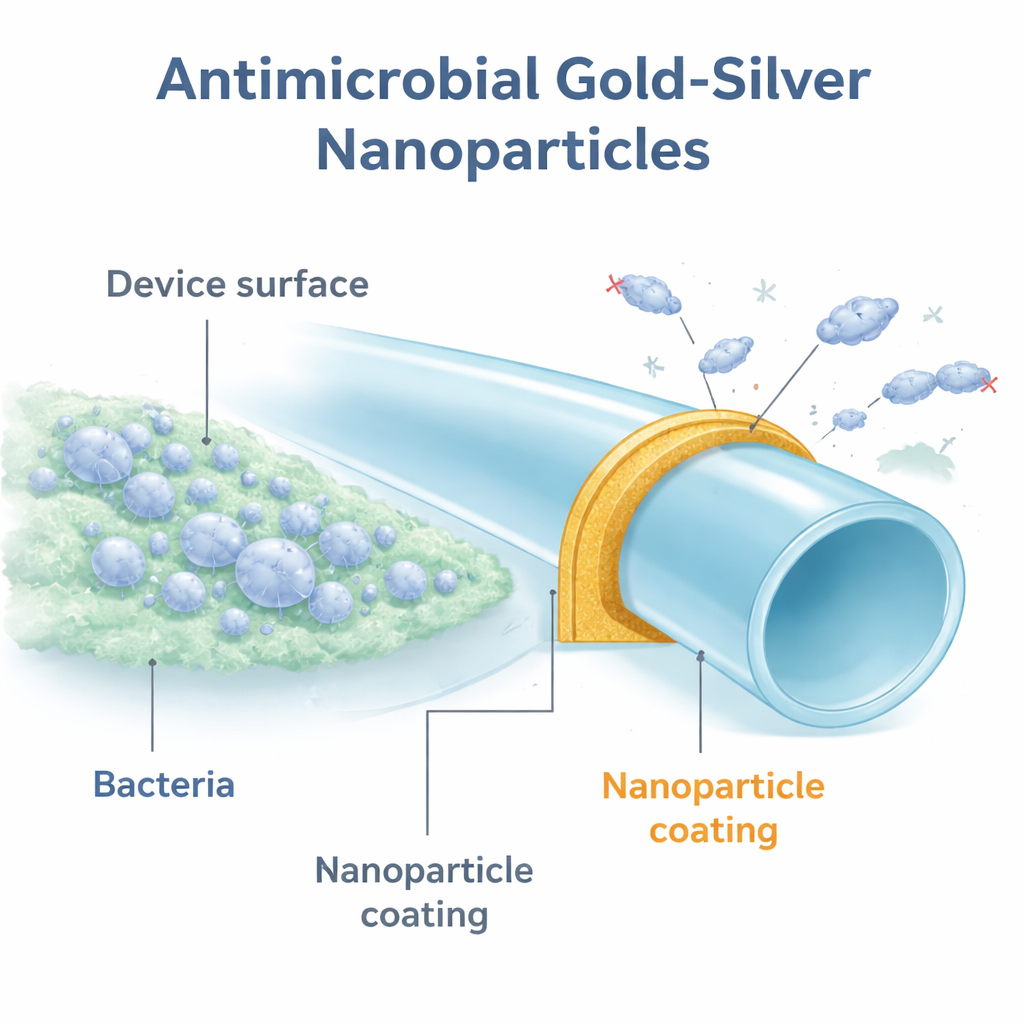
Новый вид защитной брони
Исследователи сосредоточились на крошечных металлических частицах размером в несколько миллиардных долей метра. Эти наночастицы строились вокруг углеродной клеточной структуры, называемой полигидроксифуллереном, известной своей низкой токсичностью и способностью усиливать свойства некоторых металлов. Они создали несколько вариантов с разными металлами и покрыли ими небольшие диски из полиуретана — пластика, широко применяемого в урологических устройствах. При испытаниях таких покрытых дисков на стандартном штамме Escherichia coli только частицы, содержащие серебро, показали выраженный антибактериальный эффект. Явным лидером оказалась комбинация золота и серебра, обозначенная как GSNPs, которая сокращала число бактерий до 100 000 раз по сравнению с непокрытым пластиком.
Остановить реальные урологические возбудители
Чтобы проверить, сохраняется ли эффект на клинических штаммах, команда испытала лучшее покрытие против шести видов бактерий, взятых непосредственно с инфицированных уретеральных стентов и пенильных протезов. Среди них были как грамположительные, так и грамотрицательные виды, известные вызывающими упорные инфекции. При уровнях бактерий, сопоставимых с теми, что обнаруживают у пациентов, поверхности, покрытые GSNPs, обеспечили 100% уничтожение как плавающих, так и прикреплённых к поверхности бактерий для всех протестированных штаммов. В отдельных экспериментах исследователи подвергали бактерии воздействию разных концентраций наночастиц в жидкости и оценивали, какое количество GSNP необходимо для подавления роста. Все штаммы полностью ингибировались при концентрации GSNP в жидкости на уровне или ниже 3 микрограмм на миллилитр, хотя некоторым грамположительным организмам требовалось немного большее количество.
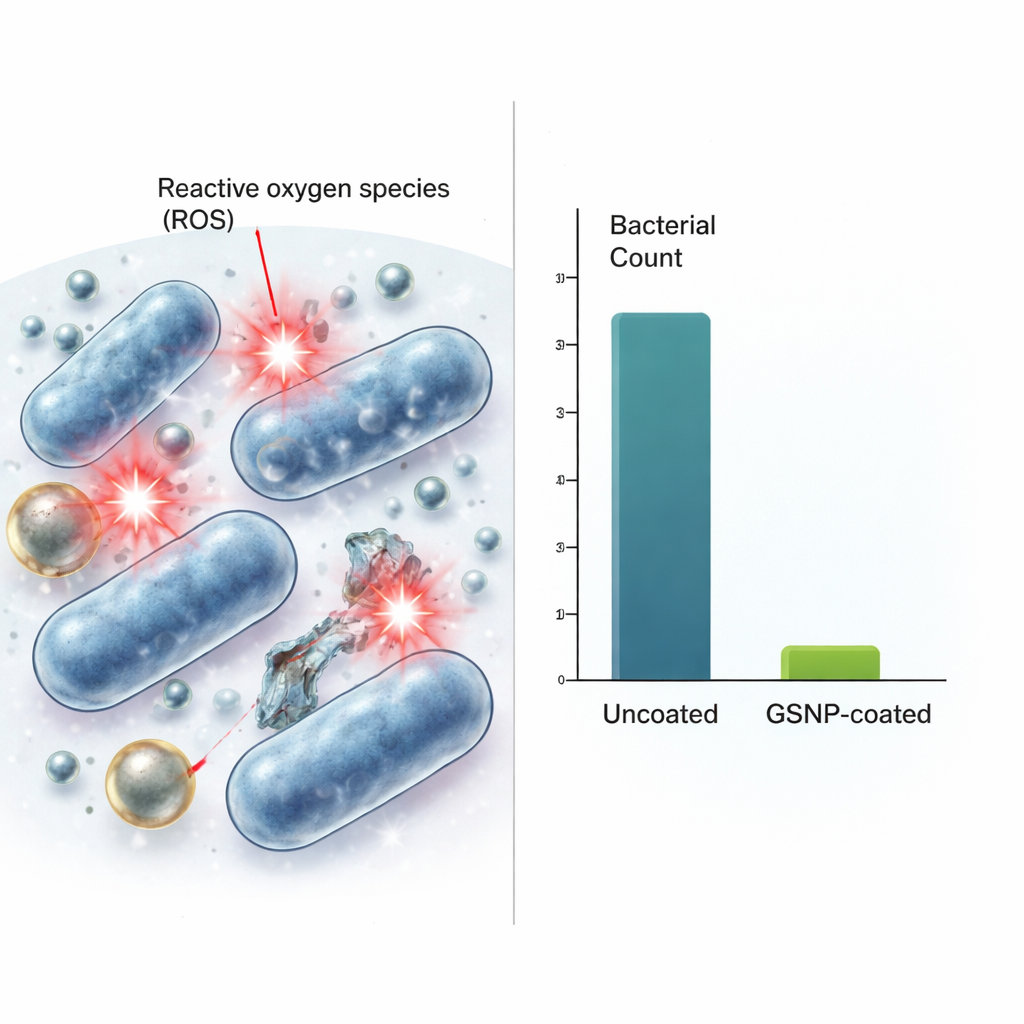
Как они действуют и насколько безопасны
Далее команда выясняла, как эти покрытия убивают бактерии и могут ли они повредить клетки человека. Данные указывают на реакктивные формы кислорода — химически активные формы кислорода — как на ключевой компонент механизма гибели. Сами по себе наночастицы не генерировали эти реактивные молекулы, однако бактерии, подвергнутые воздействию GSNPs, производили значительно больше таких веществ, чем необработанные бактерии, что говорит о том, что частицы запускают разрушающую химию внутри или вблизи микроорганизмов. Когда фибробласты мыши подвергали воздействию схожих или более высоких концентраций GSNPs, более 80% клеток оставались жизнеспособными при наихудшей антибактериальной дозе. Другими словами, уровни, уничтожающие бактерии, оказывали лишь умеренное влияние на клетки млекопитающих. GSNPs также показали значительно большую эффективность по сравнению с коммерческим продуктом на основе золота и серебра, протестированным параллельно, достигая примерно миллионного преимущества по сокращению числа бактерий при равных дозах.
Что это может значить для пациентов
Хотя эти исследования проводились в лабораторных условиях и ещё не в испытаниях на животных или людях, результаты указывают на перспективную стратегию для более безопасных медицинских имплантов. Тонкий слой GSNPs на катетере или протезе мог бы обеспечить широкую защиту против различных бактерий, снизить необходимость удаления устройства и при этом не полагаться на традиционные антибиотики. Покрытие использует небольшие количества металла, демонстрирует относительно низкую токсичность в начальных тестах и просто в производстве. При дальнейшей доработке для улучшения долговременной стабильности и тщательном тестировании в реалистичных моделях эти покрытия из золото‑серебряных наночастиц могут помочь сохранить важные урологические устройства в рабочем состоянии для пациентов, а не превращать их в очаги инфекции.
Цитирование: Rodriguez-Alvarez, J.S., Xu, Y., Gutierrez-Aceves, J. et al. Broad spectrum antimicrobial nanoparticles with low toxicity to prevent biofilm formation on urologic devices. Sci Rep 16, 7333 (2026). https://doi.org/10.1038/s41598-026-36969-2
Ключевые слова: биопленка, урологические устройства, антимикробное покрытие, наночастицы, золото‑серебро