Clear Sky Science · ru
Про‑воспалительная субпопуляция нейтрофилов вызывает ишемико‑реперфузионное повреждение кишечника через путь стресса эндоплазматического ретикулума, опосредованный ATF4
Когда кровоток вредит кишечнику
Хирурги и врачи интенсивной терапии давно озадачены опасным парадоксом: когда кровоснабжение кишечника прекращается, а затем восстанавливается, само восстановление потока иногда наносит серьезный урон слизистой. Этот процесс, называемый ишемико‑реперфузионным повреждением кишечника, может привести к угрожающим жизни осложнениям, таким как сепсис и полиорганная недостаточность. В приведённом исследовании показано, что не все иммунные клетки, стремящиеся на место происшествия, одинаковы — одна особенно агрессивная подгруппа лейкоцитов играет ключевую роль в превращении спасительной реакции в вредную.
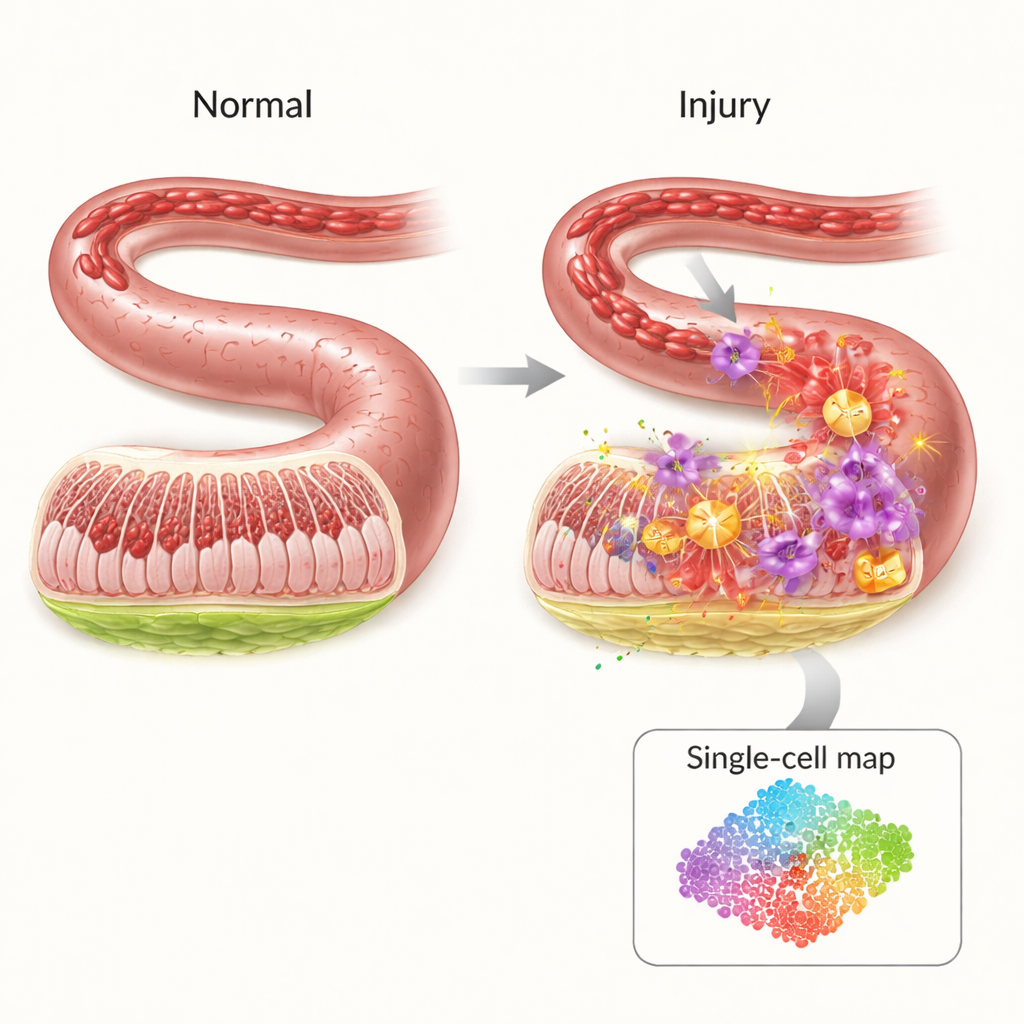
Хрупкая защитная стена кишечника
Внутренняя поверхность кишечника покрыта тонким, но высокоорганизованным барьером, который удерживает бактерии и токсины в просвете, одновременно пропуская питательные вещества. Когда кровоток прерывается — например при шоке, крупной операции или тяжелой травме — этот барьер лишается кислорода. Удивительно, но большая часть повреждений возникает не в период отсутствия кровоснабжения, а при его восстановлении. Внезапный приток кислорода и иммунных клеток запускает лавину воспалительных сигналов и реактивных молекул, которые могут проделывать отверстия в стенке кишечника, позволяя микробам проникать в кровь. Несмотря на клиническую важность явления, сегодня у врачей мало целенаправленных средств для предотвращения этой каскадной реакции.
Взгляд на отдельные клетки
Чтобы выяснить, кто что делает во время этого кризиса, исследователи применили секвенирование РНК на уровне отдельных клеток — метод, который считывает, какие гены активны в тысячах отдельных клеток одновременно. В моделях ишемии‑реперфузии кишечника у мышей они сравнили поврежденные и здоровые ткани и сопоставили 19 основных типов клеток. Выяснилось, что определённые иммунные клетки — особенно нейтрофилы и воспалительные моноциты — существенно расширялись после повреждения, тогда как защитные клетки, такие как Т‑ и В‑лимфоциты и натуральные киллеры, снижались. Сети коммуникации между типами клеток также изменились: нейтрофилы выступили в роли центральных узлов, посылающих и получающих множество воспалительных сигналов, что указывает на их ключевую роль в повреждении.
Вредная подгруппа первичных реагентов
Нейтрофилы — одни из самых быстрых первичных реагентов организма, они по кровотоку спешат бороться с инфекциями и убирать разрушенные участки. Но исследование показывает, что внутри популяции нейтрофилов есть особенно агрессивная подгруппа, ответственная за значительную часть «побочного урона» в кишечнике. Когда учёные истощали нейтрофилы у мышей перед индуцированием ишемии‑реперфузии, у животных уменьшалось укорочение кишечника, снижались уровни маркеров повреждения в крови, улучшалась гистологическая картина тканей и укреплялись белки‑«молнии», скрепляющие эпителиальный барьер. В ко‑культурных экспериментах нейтрофилы, взятые из повреждённых мышей, прямо повреждали кишечные клетки: снижали их выживаемость, увеличивали гибель и нарушали ключевые «замочные» белки, поддерживающие непроницаемость барьера.
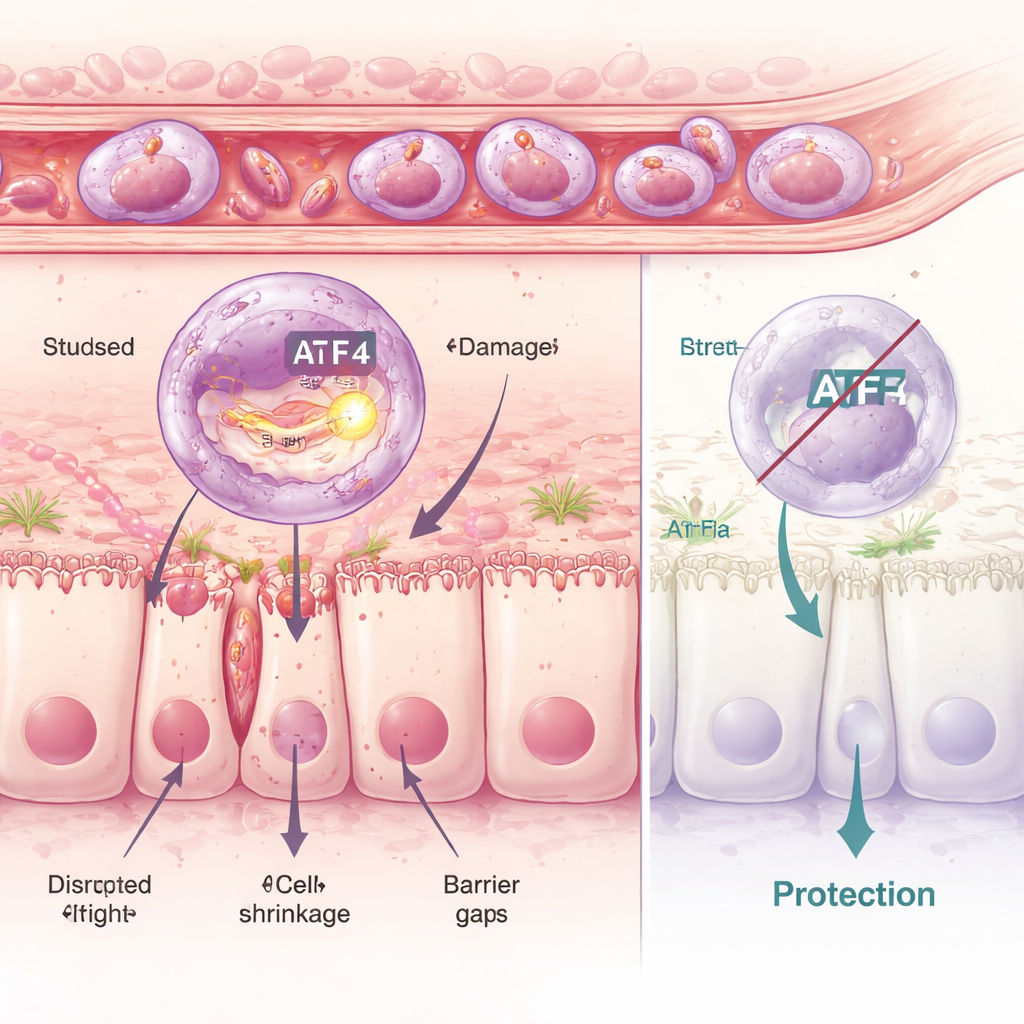
Стресс внутри клеток: когда контроль качества даёт сбой
Углубившись, исследователи проанализировали нейтрофилы поодиночке и выделили шесть разных подгрупп. Одна из них, названная кластером C5, выделялась выраженным воспалительным профилем и включением молекулярной стресс‑программы в структуре, называемой эндоплазматическим ретикулумом — мастерской сворачивания белков. Ключевым регулятором этой программы является белок ATF4. В вредной популяции C5 ATF4 и его генетические мишени были сильно активны. Применяя препараты, которые либо усиливают, либо подавляют этот внутриклеточный стресс‑ответ, исследователи показали: усиление стресса приводит к большему повреждению кишечника, тогда как его блокирование сохраняет барьер. Мыши с генетической инактивацией ATF4 были в значительной мере защищены: даже при введении стресс‑индуцирующих веществ их нейтрофилы не могли полностью реализовать свой повреждающий потенциал, и слизистая оставалась гораздо более целой.
Что это значит для будущих методов лечения
В совокупности эти результаты дают понятную картину для неспециалистов: среди роя иммунных клеток, наводняющих кишечник при восстановлении кровотока, определённая стресс‑предрасположенная подгруппа нейтрофилов действует как чрезмерно рьяная бригада уборщиков, разрушающая здание вместе с мусором. Их деструктивная сила зависит от встроенного стресс‑пути, контролируемого ATF4 внутри клеток. Подавление этого пути — не уничтожая все нейтрофилы — может стать способом защитить кишечник во время событий с высоким риском, таких как крупные операции, тяжёлые инфекции или травмы. Хотя требуются дополнительные исследования для подтверждения результатов у людей и поиска безопасных, точных препаратов, работа открывает перспективный путь к терапии, сохраняющей целостность кишечного барьера в критические моменты.
Цитирование: Yang, Y., Zhou, Q., Liu, S. et al. A pro-inflammatory neutrophil subpopulation drives intestinal ischemia–reperfusion injury via the ATF4-mediated endoplasmic reticulum stress pathway. Sci Rep 16, 6117 (2026). https://doi.org/10.1038/s41598-026-36938-9
Ключевые слова: кишечный барьер, ишемия реперфузия, нейтрофилы, стресс эндоплазматического ретикулума, ATF4