Clear Sky Science · ru
Пептид CKAAKN, конъюгированный с долгоциркулирующими нанолипосомами, для таргетной доставки оридонина при раке поджелудочной железы
Почему это исследование важно
Рак поджелудочной железы — один из самых смертоносных видов рака, отчасти потому, что его обычно обнаруживают на поздних стадиях и он часто устойчив к стандартной химиотерапии. В этом исследовании изучается более изящный способ доставки растительного противоракового соединения оридонина непосредственно в опухоли поджелудочной железы с помощью крошечных жировых пузырьков — нанолипосом. Помогая доставлять больше препарата в опухоль и щадить здоровые ткани, эта работа указывает путь к более мягким и эффективным методам лечения для болезни, которая отчаянно в них нуждается.
Смертельный рак, который трудно лечить
Рак поджелудочной железы заслужил мрачное прозвище «король раков», поскольку для большинства пациентов показатели выживаемости остаются в однозначных процентах. Только небольшая часть людей подходит для операции, и даже после операции многие опухоли рецидивируют. Химиопрепараты, такие как паклитаксел и цисплатин, могут замедлить развитие заболевания, но они вызывают серьезные побочные эффекты, и опухоли часто становятся резистентными. Поэтому исследователи ищут препараты, которые были бы более точными и менее токсичными, а также системы доставки, способные концентрировать лекарство в самой опухоли, а не заливать весь организм.
Преобразование растительной молекулы в современный препарат
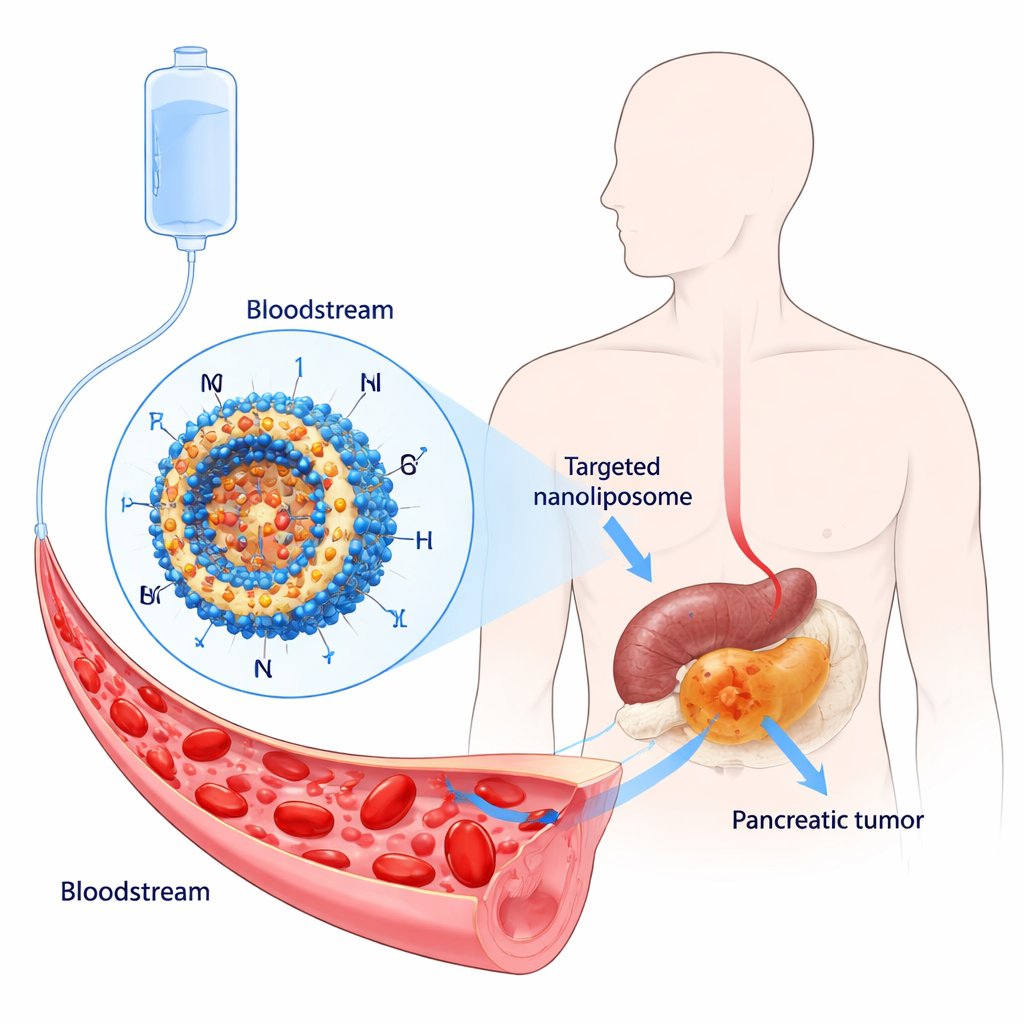
Оридонин — природное соединение, выделяемое из традиционного китайского лекарственного растения Rabdosia rubescens. Лабораторные исследования показали, что он может убивать или замедлять рост многих типов раковых клеток, включая клетки поджелудочной железы, вмешиваясь в деление клеток и вызывая апоптоз. Однако сам по себе оридонин трудно использовать как лекарство: он плохо растворим в воде, слабо всасывается и может быть токсичен при более высоких дозах. Чтобы реализовать его потенциал, авторы поместили оридонин внутрь нанолипосом — крошечных сфер, сделанных из липидов, схожих с липидами клеточных мембран, — сконструированных так, чтобы безопасно нести препарат через кровоток и медленно высвобождать его в месте опухоли.
Создание «маскирующей» и нацеливающей оболочки для препарата
Команда разработала двухслойную систему доставки. Сначала они создали долгоциркулирующие липосомы, покрыв их поверхность полиэтиленгликолем (ПЭГ) — гибким, гидрофильным полимером, который помогает частицам уклоняться от иммунных клеток и дольше находиться в крови. Затем добавили короткий пептид CKAAKN, который действует как метка‑направитель для рака поджелудочной железы. Этот пептид имитирует часть сигнального пути Wnt, который аномально активен во многих панкреатических опухолях, позволяя модифицированным липосомам (называемым ORI@CPD‑Lipo) прикрепляться к раковым клеткам, экспрессирующим соответствующие рецепторы. Конечные частицы имели диаметр около 100 нанометров, содержали большое количество оридонина и медленно высвобождали препарат в течение многих часов, а не сразу.
Поведение таргетных частиц в клетках и животных
В тестах на клеточных культурах липосомы с меткой CKAAKN захватывались человеческими раковыми клетками поджелудочной железы значительно эффективнее, чем нормальными панкреатическими клетками, особенно в первые часы контакта. Когда в качестве отвлекающего фактора добавляли избыток свободного пептида CKAAKN, раковые клетки поглощали меньше частиц, что подтверждает участие специфического связывания. Пустые липосомы проявили низкую токсичность и не повреждали эритроциты, что указывает на хорошую безопасность. Загруженные оридонином таргетные липосомы убивали раковые клетки эффективнее, чем свободный оридонин или нетаргетные липосомы, и сильнее замедляли миграцию раковых клеток по «царапающей» культуре. У мышей с опухолями поджелудочной железы флуоресцентно меченые таргетные липосомы накапливались в опухоли до 48 часов и скапливались там более выраженно, чем нетаргетные липосомы, при этом в основном очищаясь через печень и селезенку, как и ожидалось.
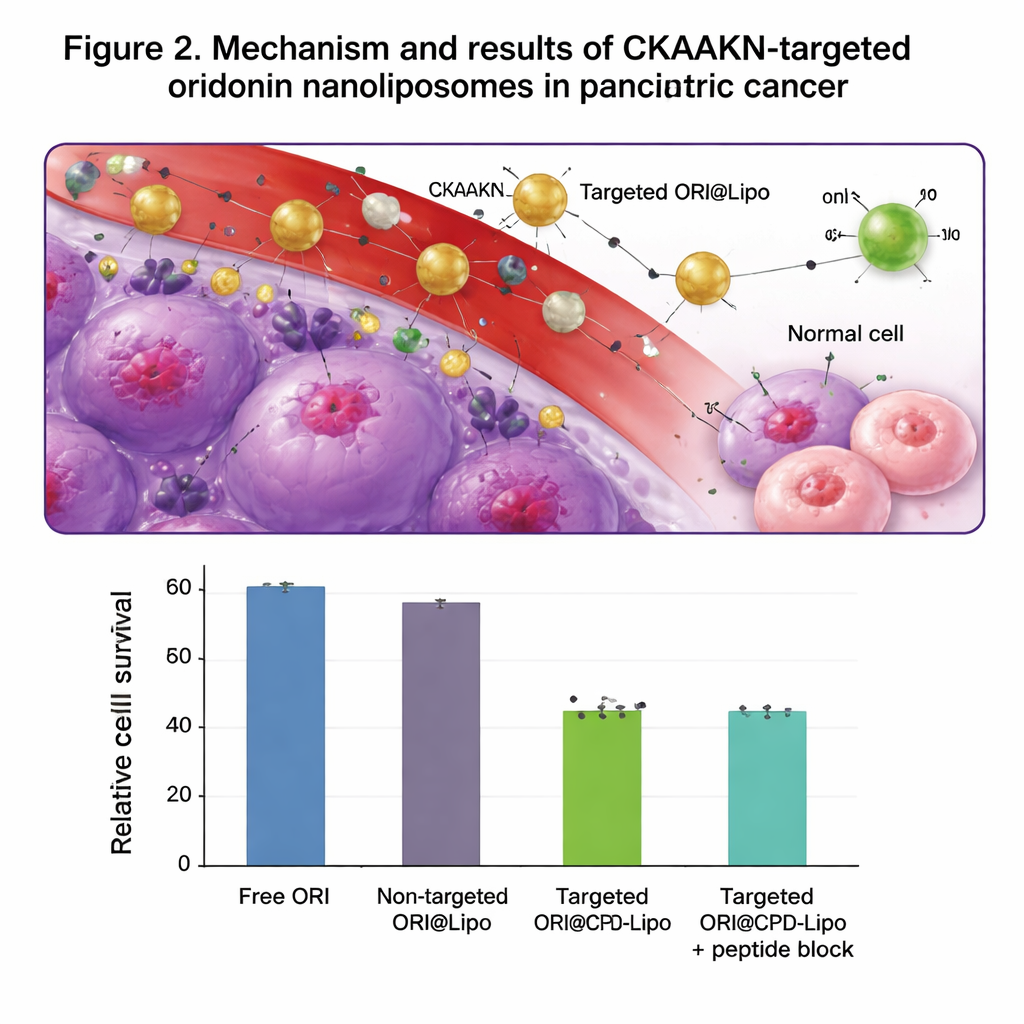
Что это может означать для будущего лечения
В совокупности результаты показывают, что сочетание традиционного растительного соединения с современной точной системой доставки может существенно усилить его антиопухолевую активность в лабораторных моделях. Нанолипосомы с декором CKAAKN и длительным циркулированием направляют больше оридонина в раковые клетки поджелудочной железы при ограничении воздействия на нормальные ткани, усиливая гибель опухолевых клеток и уменьшая подвижность, которая могла бы привести к метастазированию. Хотя эти данные пока доклинические и авторы отмечают необходимость полноценных исследований на животных и клинических испытаний, работа закладывает прочную основу для таргетированных наномедицинских подходов к раку поджелудочной железы и предлагает общую стратегию превращения других перспективных природных молекул в практичные, опухоле‑ориентированные препараты.
Цитирование: Zhang, F., Luo, K., Xuan, S. et al. CKAAKN peptide-conjugated long-circulating nanoliposomes for the targeted delivery of oridonin to pancreatic cancers. Sci Rep 16, 6065 (2026). https://doi.org/10.1038/s41598-026-36920-5
Ключевые слова: рак поджелудочной железы, нанолипосомы, таргетная доставка лекарств, оридонин, пептид, нацеливающий на опухоль