Clear Sky Science · ru
Синтез и оценка антираковой активности новых производных тиоимидазола с триметоксифенильной группой
Новые химические инструменты в борьбе с раком
Химиотерапевтические препараты часто повреждают здоровые клетки наряду с опухолевыми, вызывая тяжелые побочные эффекты. В этом исследовании рассматривается новая группа синтетических молекул, которые нацелены на то, чтобы поражать раковые клетки заметно сильнее, чем нормальные ткани. Объединив два химических фрагмента, уже известных своей эффективностью в лекарственных средствах, исследователи получили соединения, демонстрирующие сильное и направленное уничтожение раковых клеток в тестах в пробирке и в 3D-моделях опухолей, при этом здоровые клетки остаются в основном невредимыми.
Создание более «умных» молекул для уничтожения рака
Команда сосредоточилась на двух «привилегированных» химических мотивах, которые часто встречаются в успешных лекарствах. Один — имидазол, маленькое кольцо, которое хорошо взаимодействует с множеством биологических мишеней. Другой — триметоксифенильная (TMP) группа, набор из трех кислородсодержащих побочных цепей на ароматическом кольце, центральный элемент нескольких противораковых препаратов, нарушающих деление клеток. Введение атома серы в ядро имидазола (получая тиоимидазол) и его связь с TMP-группой позволили химикам тонко настроить фармакокинетику молекул и их сродство к белкам, связанным с раком. С помощью пошагового синтетического пути была собрана библиотека родственных соединений, каждое слегка модифицированное для выявления ключевых для антираковой активности характеристик. 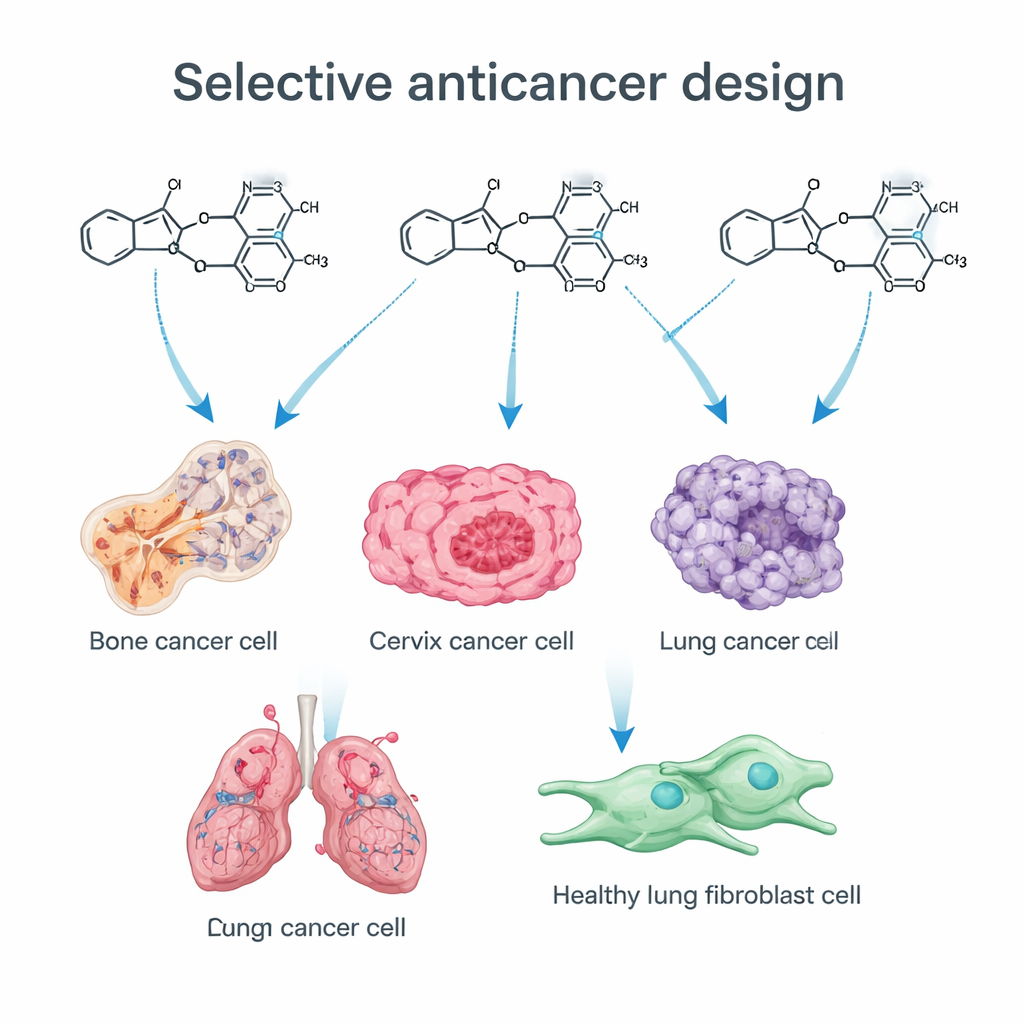
Тестирование на раковых клетках с щадящим отношением к здоровой ткани
Новые молекулы испытывали на четырех линиях человеческих раковых клеток — остеосаркомы (костная), шейки матки, толстой кишки и легких — а также на непораженных фибробластах легкого. Многие соединения замедляли или останавливали рост опухолевых клеток, но одно, обозначенное как 13b, выделилось особенно. Оно убивало клетки костной и шейной опухоли при очень низких концентрациях и при этом не проявляло обнаруживаемой токсичности в отношении нормальных фибробластов даже при дозах более чем в 60 раз выше. Несколько других соединений были умеренно активны, но менее селективны, что подчеркивает, как небольшие структурные изменения — например, добавление атома хлора или нитрогруппы в определенных положениях — могут смещать баланс между широкотоксичным эффектом и направленным действием против рака.
Как ведущий препарат заставляет раковые клетки самоуничтожаться
Чтобы понять, что именно делает 13b внутри клеток, исследователи искали признаки программируемой гибели клетки, или апоптоза. Раковые клетки, обработанные 13b, стали положительными по Annexin V и активировали ферменты каспазы-3 и -7 — классические маркеры того, что клетка запущена в упорядоченную программу самоубийства, а не просто лизируется. Микроскопия показала яркие участки γH2AX, сигнал о разрывах ДНК, в ядрах обработанных клеток. Со временем внутриклеточный каркас стал реорганизовываться и разрушаться, особенно в клетках шейной опухоли, которые округлялись и отставали — визуальные признаки развивающегося апоптоза. В совокупности эти данные указывают, что 13b повреждает ДНК раковых клеток и затем направляет их по контролируемому пути гибели.
От плоских слоев клеток к 3D-миниопухолям
Большинство лабораторных тестов растят раковые клетки в тонких слоях, которые не полностью воспроизводят плотную, многослойную структуру реальных опухолей. Чтобы учесть это, команда выращивала клетки в трехмерные сфероиды — крошечные шаровидные кластеры, которые лучше имитируют архитектуру опухоли и проблемы проникновения препарата. При обработке этих сфероидов 13b они уменьшались в размерах в зависимости от дозы. Сфероиды костной опухоли были особенно чувствительны, становясь мелкими, рыхлыми и фрагментированными при более высоких концентрациях препарата. Флуоресцентное окрашивание показало волны апоптоза, распространяющиеся от поверхности сфероида внутрь по мере увеличения концентрации, что доказывает способность 13b проникать и убивать клетки внутри этих плотных структур. 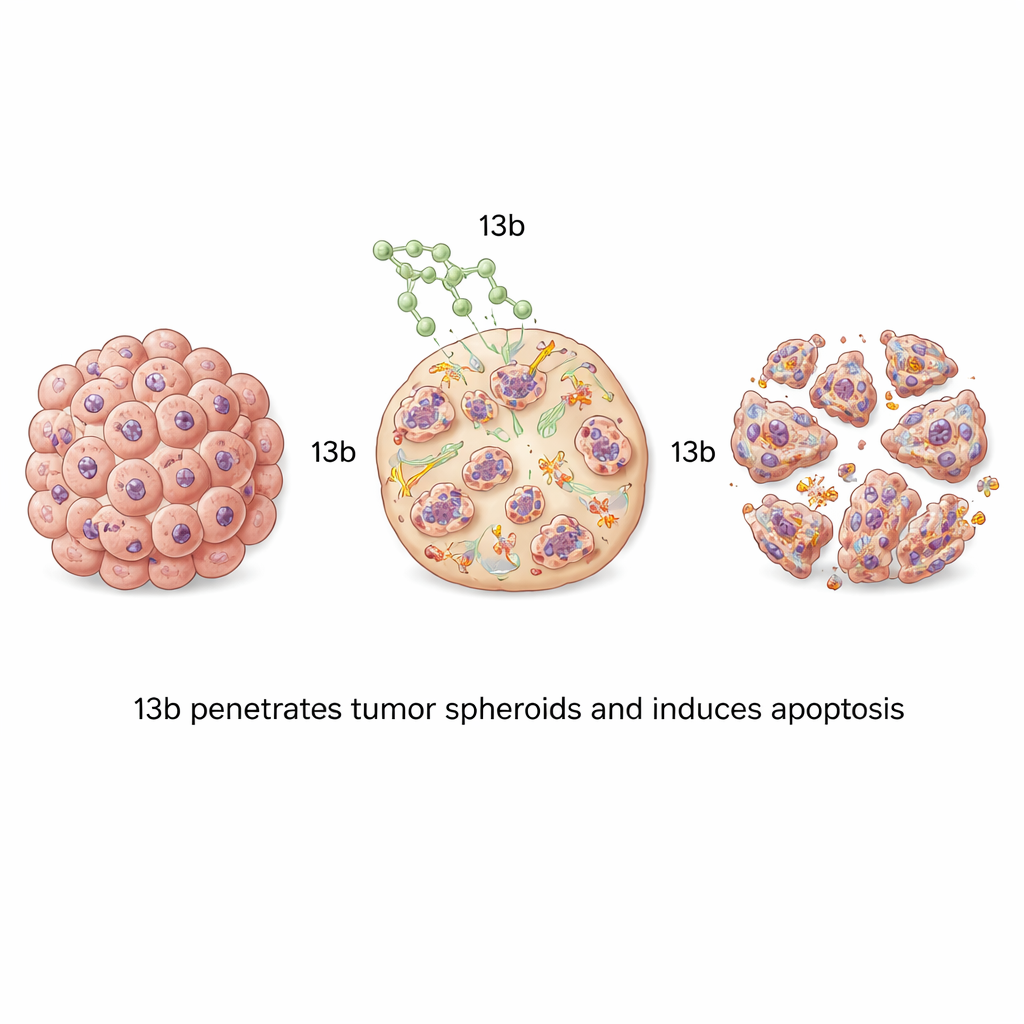
Почему эта работа важна для будущих методов лечения рака
Для неспециалиста ключевая мысль такова: исследователи создали новый класс малых молекул, объединяющий лучшие свойства двух проверенных компонентов в гибридный дизайн. Их ведущий кандидат, 13b, способен эффективно распознавать и уничтожать раковые клетки при значительном щадящем эффекте для здоровых клеток в лабораторных тестах и сохраняет активность даже в более реалистичных 3D-моделях опухолей. Хотя предстоит еще много работы — включая определение точных молекулярных мишеней, улучшение растворимости и испытания на животных — это исследование показывает, что сочетание каркасов тиоимидазола и TMP — перспективная стратегия для создания более селективных и мощных противораковых средств.
Цитирование: Maciejewska, N., Grybaitė, B., Anusevičius, K. et al. Synthesis and anticancer evaluation of novel thioimidazole derivatives bearing a trimethoxyphenyl moiety. Sci Rep 16, 6271 (2026). https://doi.org/10.1038/s41598-026-36890-8
Ключевые слова: антираковые препараты, производные имидазола, триметоксифенил, апоптоз, 3D-сфероиды опухоли