Clear Sky Science · ru
Фармакокинетика, патология и эффективность ингибитора главного протеази SARS-CoV-2 VPC285785 в мышиной модели коронавирусной инфекции
Почему нам всё ещё нужны лучшие противовирусные таблетки от COVID
Первые противовирусные таблетки для лечения COVID‑19, такие как Паксловид, стали переломным моментом в пандемии. Но они не идеальны: их нужно принимать очень рано, требуется несколько таблеток в день, и они могут опасно взаимодействовать с другими препаратами. В этом исследовании изучаются новые кандидатные препараты, разработанные так, чтобы блокировать коронавирус по двум направлениям, хорошо работать как единичные пероральные таблетки и вызывать меньше лекарственно‑лекарственных взаимодействий, с использованием мышиной модели коронавирусной инфекции.
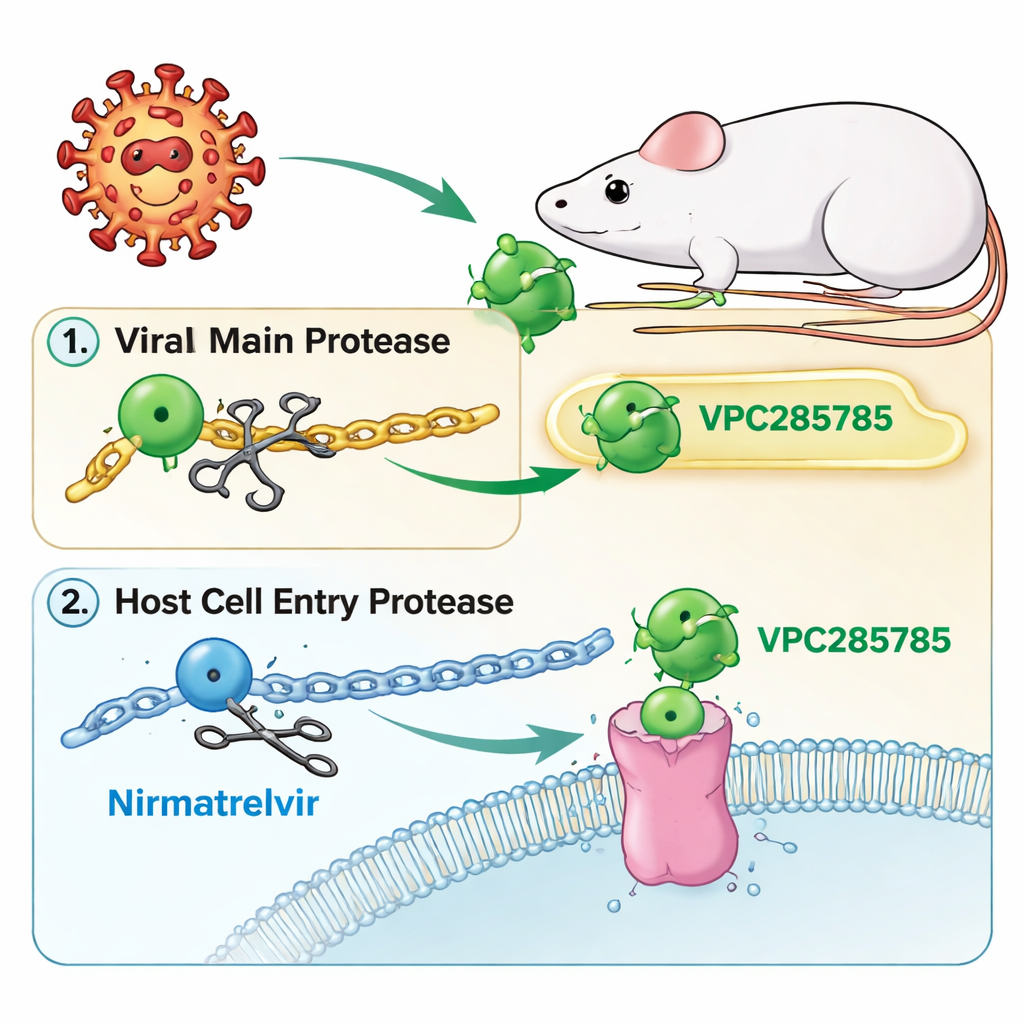
Новый поворот у мишени — протеаза SARS‑CoV‑2
Как и Паксловид, новые соединения — VPC285785 и VPC285786 — нацелены на «главную протеазу» вируса, молекулярные ножницы, которые разрезают длинные вирусные белки на функциональные части. Если эти ножницы заклинить, вирус не сможет завершить сборку и остановится. Исследователи также спроектировали молекулы так, чтобы они поражали второй белок в клетках хозяина — катепсин L, который помогает некоторым коронавирусам проникать внутрь. Нацеленность одновременно на вирусную протеазу и помощьника входа в клетку позволяла надеяться на препарат с двойным действием, от которого вирусу будет сложнее уклоняться, и который не потребует усилителя‑дополнителя.
Спроектированы на стойкость, а не на усилитель
Паксловид сочетает нимратрелвир с другим препаратом — ритонавиром, задача которого не борьба с вирусом, а замедление разрушения нимратрелвира в печени. Однако ритонавир вмешивается во многие ферменты, обрабатывающие распространённые лекарства, что приводит к сложным и иногда опасным взаимодействиям. VPC285785 и VPC285786 химически настроили так, чтобы они сами были более устойчивы к распаду, используя такие приёмы, как атомы фтора и «упрочнение» колец, делающие их менее привлекательными для печёночных ферментов. В лабораторных тестах на препаратах человеческой и мышиной печени оба новых соединения оказались по крайней мере столь же стабильными, как нимратрелвир, а VPC285786 в некоторых отношениях оказался ещё более стойким, и всё это — без присутствия ритонавира.
Как препараты ведут себя и перемещаются в организме мышей
Команда затем изучила, как соединения распределяются по организму мышей, измеряя, как быстро они исчезают из крови и насколько хорошо всасываются при приёме внутрь. После инъекции VPC285785 и VPC285786 задерживались в кровотоке примерно так же долго, как нимратрелвир, и обеспечивали более высокую суммарную экспозицию. Однако при пероральном приёме их пути разошлись: VPC285785 достигал умеренного, но работоспособного всасывания (примерно 15% от проглоченной дозы попадало в циркуляцию), тогда как VPC285786 практически не попадал в кровь (около 3%). Поскольку таблетки должны пересекать стенку кишечника, чтобы быть практичным лечением, только VPC285785 был выбран для дальнейших экспериментов с инфекцией.
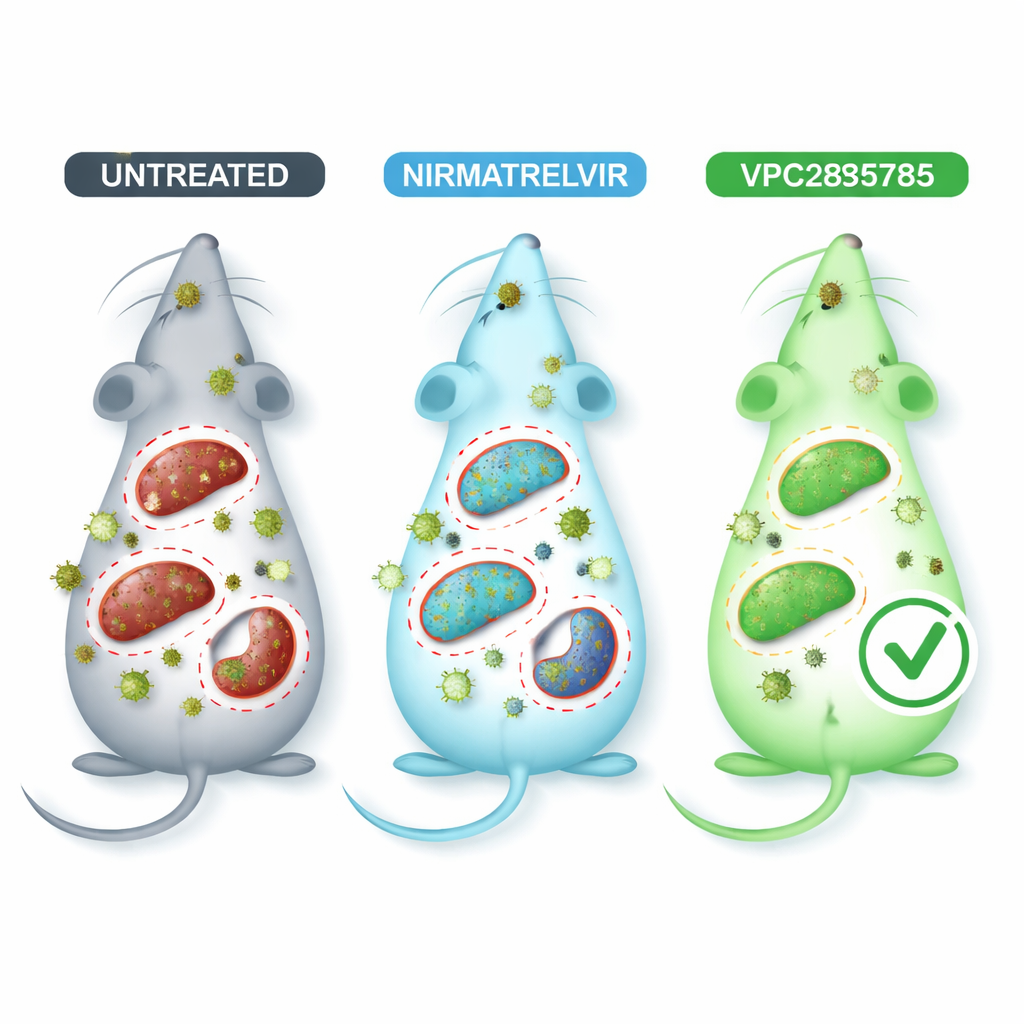
Испытание новой таблетки на инфицированных мышах
Чтобы моделировать коронавирусное заболевание в более безопасных условиях, исследователи использовали мышиный коронавирус MHV‑A59, который поражает несколько органов и вызывает поражения легких и печени, во многих отношениях схожие с человеческой инфекцией. Заражённым мышам давали перорально VPC285785, нимратрелвир в качестве сравнения или неактивный растворитель. Анализы крови показали, что инфекция нагружает печень и почки, но животные, получавшие VPC285785 или нимратрелвир, как правило, имели более благоприятные показатели ферментов печени и маркеров функции почек по сравнению с не лечеными мышами. Наиболее заметно VPC285785 резко снизил количество вирусного генетического материала в печени, мозге и селезёнке, тогда как нимратрелвир дал явное снижение только в мозге. В лёгких, сердце и почках при испытанных условиях ни одно из лечений существенно не повлияло на уровни вируса.
Что это может значить для будущих препаратов против COVID
Хотя VPC285785 в пробирке менее мощен против вирусной протеазы, чем нимратрелвир, он хорошо проявляет себя в живых животных, значительно снижая уровни вируса в ряде ключевых органов и сохраняя функцию органов, и всё это без усилителя‑ритоновира. Его «сестринское» соединение VPC285786 показывает, что ещё более сильное двойное нацеливание на вирусную протеазу и катепсин L возможно, но его плохое всасывание нужно исправить. В целом эти результаты свидетельствуют, что препараты следующего поколения от COVID могут быть разработаны как единичные пероральные лекарства, действующие на вирусные и клеточные мишени одновременно, с меньшим риском опасных взаимодействий с другими медикаментами и с сохранением сильной защиты в жизненно важных тканях.
Цитирование: Smith, J.R., Toro, A., Sabater, A. et al. Pharmacokinetics, pathology and efficacy of SARS-CoV-2 main protease inhibitor VPC285785 in a murine model of coronavirus infection. Sci Rep 16, 6905 (2026). https://doi.org/10.1038/s41598-026-36842-2
Ключевые слова: антивирусы против SARS-CoV-2, ингибиторы главной протеазы, альтернативы Паксловиду, мышиная модель коронавируса, пероральное лечение COVID