Clear Sky Science · ru
YTHDC1 модулирует злокачественный фенотип ретинобластомы через SQSTM1-опосредованный аутофагический путь
Почему это важно при детской опухоли глаза
Ретинобластома — наиболее частая опухоль глаза у маленьких детей. Если её обнаружить на ранней стадии, врачи часто могут вылечить ребёнка, однако когда опухоль прорастает в окружающие ткани или распространяется в направлении мозга, сохранить и жизнь ребёнка, и зрение становится гораздо труднее. В этом исследовании изучается молекулярный «тормоз» внутри раковых клеток — две молекулы, YTHDC1 и SQSTM1, — которые, по-видимому, помогают удерживать ретинобластому в менее агрессивном состоянии. Понимание того, как работает этот тормоз, может открыть новые пути для более бережных и целевых методов лечения.
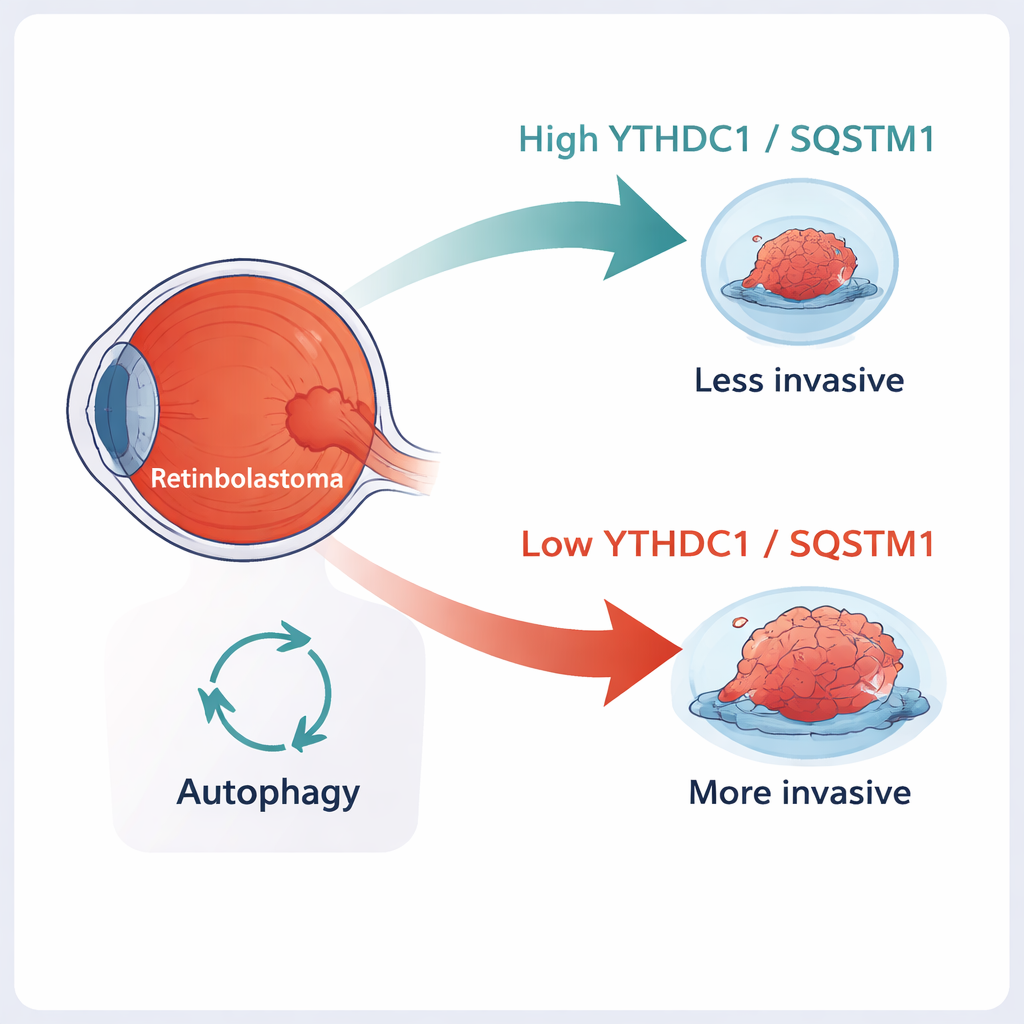
Ближе к детским опухолям глаза
Ретинобластома возникает из светочувствительного слоя глаза — сетчатки, обычно у детей младше пяти лет. Классически заболевание начинается с утраты обеих копий защитного гена RB1. Но потеря RB1 сама по себе не полностью объясняет, почему одни опухоли остаются в пределах глаза, а другие проникают в соседние ткани или распространяются по зрительному нерву. Исследователи всё больше осознают, что химические метки на РНК — временных сообщениях, указывающих клетке, какие белки синтезировать — могут существенно влиять на поведение рака. Одна из самых распространённых таких меток, m6A, способна менять стабильность этих сообщений и продолжительность их жизни в клетке.
Обнаружение утраченного молекулярного тормоза
Авторы начали с сравнения генетической активности в опухолях, оставшихся внутри глаза, и в тех, что стали инвазивными. Используя публичный набор данных секвенирования РНК образцов ретинобластомы, они выявили тысячи генов с различной активностью между двумя группами и затем сосредоточились на ключевых регуляторах m6A. Сюда входят ферменты, добавляющие или удаляющие m6A, и «ридеры» — белки, которые интерпретируют эту метку. Среди десяти основных регуляторов они обнаружили, что один ридер, YTHDC1, стабильно снижен в инвазивных опухолях. При обследовании образцов от 50 детей и проведении лабораторных тестов на опухолевой ткани подтвердилось, что уровни YTHDC1 — как на уровне РНК, так и белка — уменьшены в более агрессивных случаях.
Проверка роли YTHDC1
Чтобы выяснить, что именно делает YTHDC1, команда изменила его уровни в двух линиях человеческих клеток ретинобластомы. При снижении YTHDC1 с помощью генетических инструментов клетки делились быстрее и лучше преодолевали искусственные мембраны, имитирующие тканевые барьеры — признаки повышенной инвазивности. У мышей клетки с дефицитом YTHDC1 образовывали более крупные и тяжёлые опухоли. Обратный эффект также наблюдали: вынужденная сверхэкспрессия YTHDC1 замедляла рост и снижала способность клеток мигрировать и инвазировать. Эти эксперименты указывают на то, что YTHDC1 действует как супрессор опухоли, помогая сдерживать наиболее опасные свойства ретинобластомы.
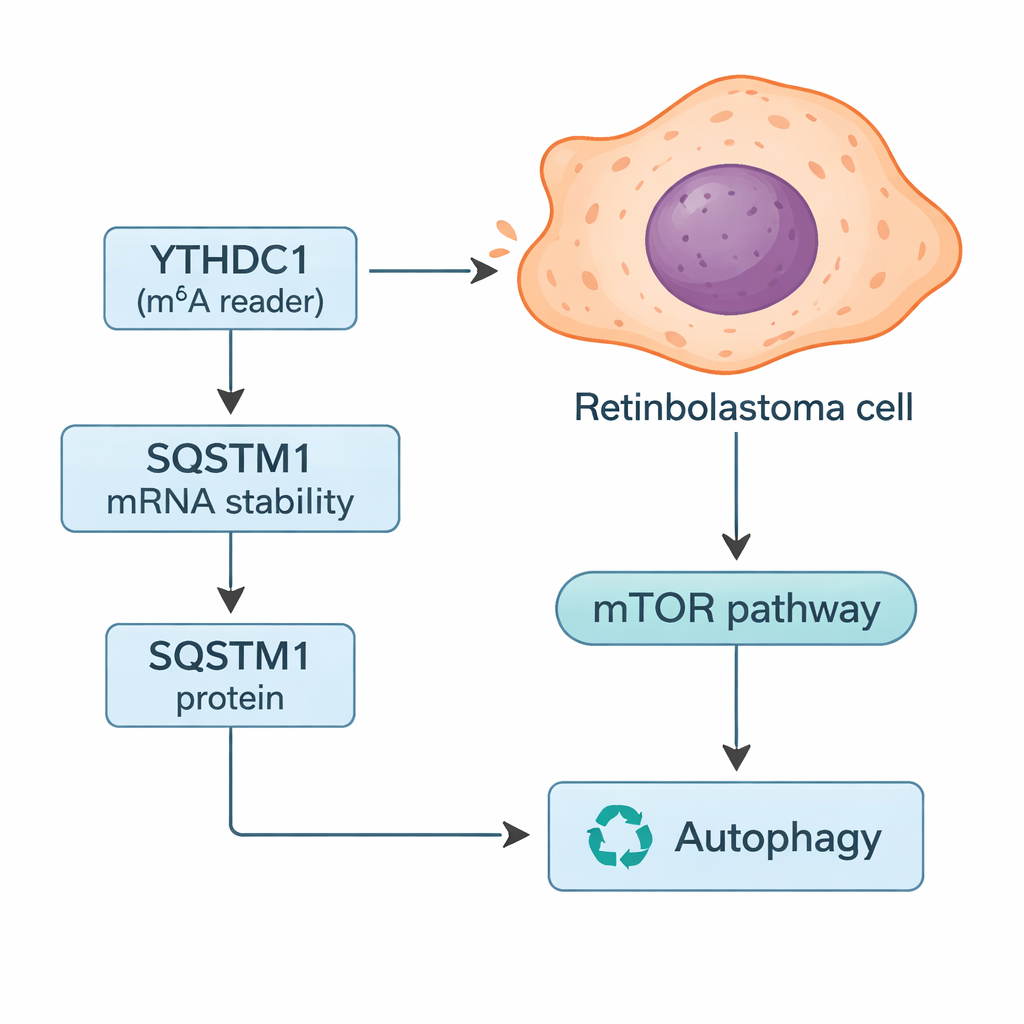
Как YTHDC1 контролирует систему утилизации клетки
Углубляясь, исследователи искали конкретные гены, чьи сообщения могли бы контролироваться YTHDC1. Объединив результаты поиска по базам данных с собственными данными по опухолям, они сфокусировались на SQSTM1, белке, более известном как p62. SQSTM1 участвует в регуляции аутофагии — системы утилизации клетки, разрушающей повреждённые компоненты и обеспечивающей энергией в условиях дефицита ресурсов. В исследовании показали, что YTHDC1 физически связывается с РНК SQSTM1 и стабилизирует её, что позволяет синтезировать больше белка SQSTM1. При снижении YTHDC1 уровни SQSTM1 падали, а её РНК распадалась быстрее. Подавление SQSTM1 само по себе усиливало рост и инвазирование клеток ретинобластомы и частично устраняло защитный эффект, наблюдавшийся при сверхэкспрессии YTHDC1, что делает SQSTM1 ключевым промежуточным звеном в этом пути.
Аутофагия, энергия и агрессивность опухоли
Поскольку SQSTM1 центральен для аутофагии, команда проверила, как изменение YTHDC1 и SQSTM1 влияет на этот процесс утилизации. С помощью комбинации флуоресцентных маркеров и измерения белков они обнаружили, что снижение либо YTHDC1, либо SQSTM1 усиливает аутофагический «трафик» — больше клеточного материала направляется в систему утилизации и через неё. Также были отмечены изменения в пути mTOR, ключевом сенсоре питательных веществ, который обычно сдерживает аутофагию. При меньшем уровне SQSTM1 активность mTOR падала, что согласуется с активацией аутофагии. Авторы предполагают, что в инвазивной ретинобластоме снижение YTHDC1 приводит к ослаблению сигналов SQSTM1, снижению активности mTOR и повышению аутофагии, что помогает опухолевым клеткам выживать в стрессовых условиях и распространяться.
Что это значит для будущего лечения
Для неспециалиста ключевая мысль такова: исследование выявляет цепочку событий в клетках ретинобластомы — YTHDC1 контролирует SQSTM1, который в свою очередь формирует систему утилизации клетки — и эта цепочка влияет на агрессивность опухоли. При ослаблении этой цепи опухоли растут быстрее и становятся более инвазивными. Хотя до клинического применения ещё далеко, этот путь даёт новые идеи для терапии: восстановление функции YTHDC1, стабилизация SQSTM1 или точная модуляция аутофагии и активности mTOR в будущем могут дополнить существующие химиотерапии. Для детей с этой опухолью такие целевые стратегии могли бы помочь ограничить распространение опухоли, сохранить больше зрения и снизить побочные эффекты лечения.
Цитирование: Ding, J., Sun, J., Wang, J. et al. YTHDC1 modulates the malignant phenotype of retinoblastoma via SQSTM1-mediated autophagy. Sci Rep 16, 6292 (2026). https://doi.org/10.1038/s41598-026-36833-3
Ключевые слова: ретинобластома, YTHDC1, SQSTM1, аутофагия, ммунулопатия mTOR