Clear Sky Science · ru
Ирисин регулирует липидный метаболизм и ферроптоз в клетках рака яичников путем модуляции оси ALOX5–5‑HETE–PD‑L1
Почему это растительное соединение важно для рака яичников
Рак яичников — один из наиболее смертельных видов рака у женщин, поскольку обычно обнаруживается на поздних стадиях и часто рецидивирует после лечения. В этом исследовании изучают, может ли природное соединение текторигенин, обнаруженное в растении Belamcanda chinensis, замедлить развитие рака яичников, лишая опухолевые клетки определённых жиров и заставляя их подвергаться особому типу клеточной смерти, зависящему от железа. Также исследуют, может ли это соединение ослабить «плащ‑невидимку», который опухоль использует, чтобы скрыться от иммунной системы.
Скрытый источник топлива внутри опухолевых клеток
Как и многие виды рака, опухоли яичников перенастраивают обращение с липидами. Вместо того чтобы просто использовать жиры как источник энергии, раковые клетки запасают их как строительные блоки для новых мембран и как буфер от повреждений. В клеточных культурах рака яичников добавление дополнительных мононенасыщенных жирных кислот приводило к накоплению свободных жирных кислот, триглицеридов и холестерина — ключевых форм депонированного жира. Этот избыток жира способствовал росту и инвазии клеток и помогал им сопротивляться разрушительному процессу, называемому ферроптозом, при котором железо и окисленные липиды разрушают клеточные мембраны. Иными словами, аномальный липидный метаболизм давал раку преимущества в росте и защиту для выживания.
Заставляя раковые клетки участвовать в самоуничтожении
Затем исследователи протестировали текторигенин на нормальных клетках яичников и нескольких линиях клеток рака яичников. При дозах до 200 микрограммов на литр соединение не вредило нормальным клеткам, но явно замедляло рост раковых клеток, снижало их способность проникать через мембрану и увеличивало долю программируемой гибели. Когда раковые клетки предварительно обрабатывали блокатором ферроптоза, они становились более агрессивными. Добавление текторигенина обращало эти эффекты: запасы жира уменьшались, повышались маркеры, связанные с железом и окислением, и больше клеток погибало. В мышиных моделях с человеческими опухолями яичников инъекции текторигенина уменьшали размер опухолей, снижали содержание жира в опухолевой ткани и усиливали химические признаки ферроптоза, что вновь указывает на то, что соединение направляет раковые клетки на путь этой железозависимой смерти.
Ключевой молекулярный переключатель, связывающий липиды и уход от иммунного надзора
Чтобы понять молекулярный механизм действия текторигенина, команда сочетала масштабную обработку данных с компьютерным моделированием взаимодействий препарата с белками. Они сфокусировались на ферменте ALOX5, который превращает распространённую жирную кислоту в сигнальная молекулу 5‑HETE. В клетках рака яичников и образцах опухолей уровни ALOX5 были значительно выше, чем в нормальной ткани. Моделирование докинга и молекулярно‑динамические симуляции показали, что текторигенин может надежно связываться с ALOX5, действуя как внутренний тормоз. Когда исследователи искусственно повышали уровень ALOX5 в раковых клетках, запасы жира увеличивались, маркеры ферроптоза снижались, и клетки становились более инвазивными. Лечение текторигенином отменяло эти изменения. Подавление ALOX5 вызывало обратный эффект — меньше жира, больше ферроптоза и снижение пролиферации — что убедительно ставит этот фермент в центр действия соединения.
Как опухоли теряют щит против иммунной системы
Исследование также связало этот липидный путь с важной молекулой иммунного контрольного пункта PD‑L1, которой опухоли пользуются, чтобы выключать атакующие иммунные клетки. Продукт ALOX5, 5‑HETE, повышал уровни PD‑L1, усиливая этот щит. При выключении ALOX5 и 5‑HETE, и PD‑L1 снижались; при повторном введении 5‑HETE PD‑L1 снова повышался, и раковые клетки возвращали часть своей защиты от ферроптоза. Текторигенин снижал ALOX5, уменьшал 5‑HETE и, в свою очередь, уменьшал PD‑L1 в клеточных культурах и в опухолях у мышей. Это свидетельствует о том, что, нацеливаясь на один метаболический фермент, соединение одновременно разрушает липидную защиту рака и ослабляет его способность скрываться от иммунного ответа.
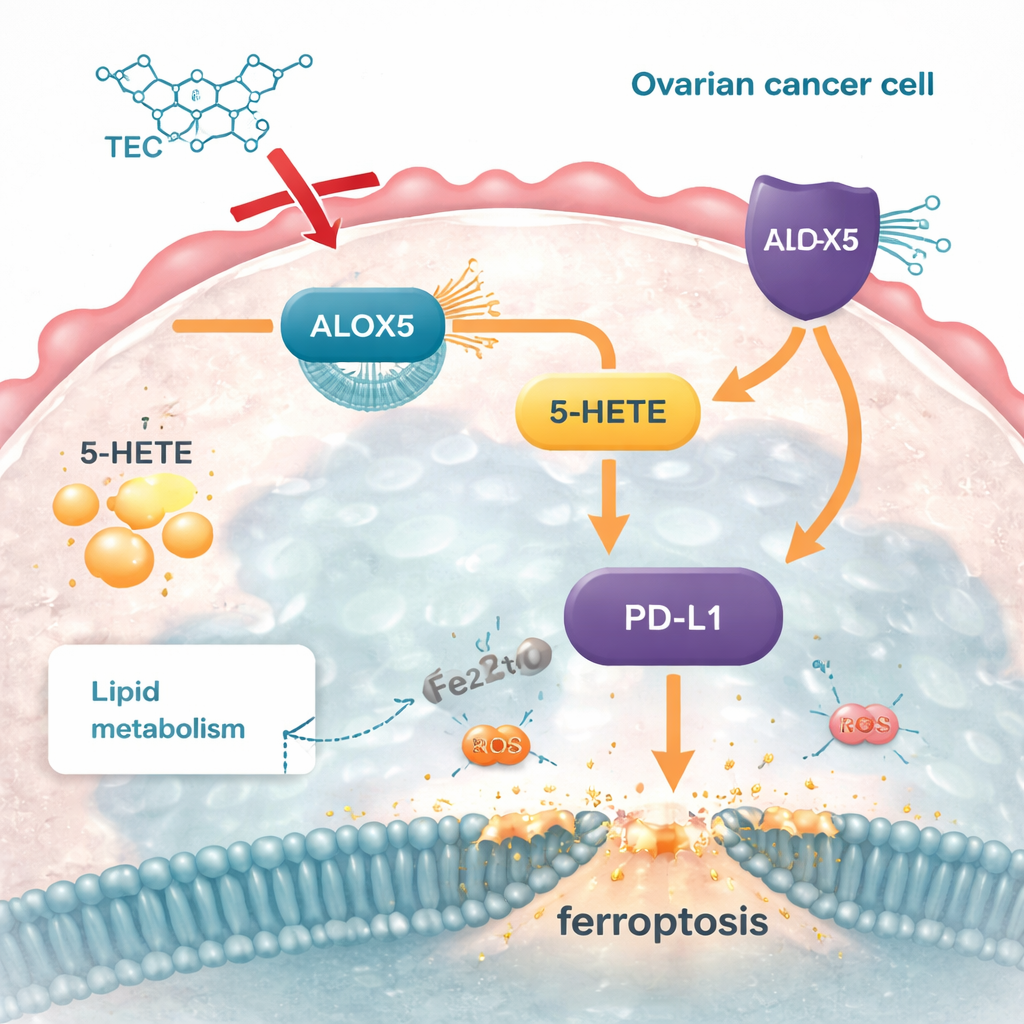
Что это может значить для будущих методов лечения
Проще говоря, эта работа показывает, что текторигенин действует как точный гаечный ключ, брошенный в механизм обращения с липидами внутри раковой клетки. Блокируя ALOX5, он прекращает выработку 5‑HETE, сокращает избыточные жировые запасы, делает клетки уязвимыми к железозависимым повреждениям и снимает часть их иммунного камуфляжа. Хотя эти данные получены в исследованиях на клетках и мышах — и многое ещё предстоит проверить на людях — они указывают на перспективную стратегию: нацеливание на ось ALOX5–5‑HETE–PD‑L1, чтобы одновременно истощать опухоли яичников и облегчать их устранение собственными защитными силами организма или будущими иммунотерапиями.
Цитирование: Cai, H., Huang, C. & Zhang, Z. Irisin regulates lipid metabolism and ferroptosis in ovarian cancer cells by modulating the ALOX5-5-HETE-PD-L1 axis. Sci Rep 16, 7223 (2026). https://doi.org/10.1038/s41598-026-36816-4
Ключевые слова: рак яичников, липидный метаболизм, ферроптоз, ALOX5, терапия натуральными соединениями