Clear Sky Science · ru
Сравнительная оценка методов таргетного профильного анализа транскриптома HTG и TempO-Seq
Почему это важно для лечения рака
Когда врачи и учёные изучают рак, они часто обращаются к «молекулам‑сообщениям» клетки — РНК — чтобы понять, какие гены активны, а какие молчат. Эти шаблоны могут раскрыть поведение опухоли и подсказать, какие методы лечения будут наиболее эффективны. Но большинство образцов в больницах хранятся в парафине после фиксации формалином, что повреждает хрупкую РНК. В этом исследовании поставлен практический вопрос с большими последствиями для онкологии: теперь, когда широко используемый тест РНК исчез с рынка, может ли новая методика заменить его и дать столь же полезные результаты на этих рутинно сохранённых образцах?
Два инструмента для чтения активности генов
Многие лаборатории годами опирались на метод HTG EdgeSeq Human Transcriptome Panel (HTP) для считывания активности генов непосредственно с небольших соскобов формалин‑фиксированной, парафинированной (FFPE) ткани. Этот подход позволял охватить почти все человеческие гены без предварительной экстракции РНК, экономя время и сохраняя ценный материал. Однако компания, стоящая за HTG EdgeSeq, обанкротилась, и исследователи остались в поиске альтернативы. Новая технология TempO‑Seq (TOS) от другого производителя обещает похожие возможности: она тоже таргетирует большое число генов одновременно, работает с повреждённой РНК из FFPE образцов и разработана как чувствительная, воспроизводимая и относительно доступная по цене.
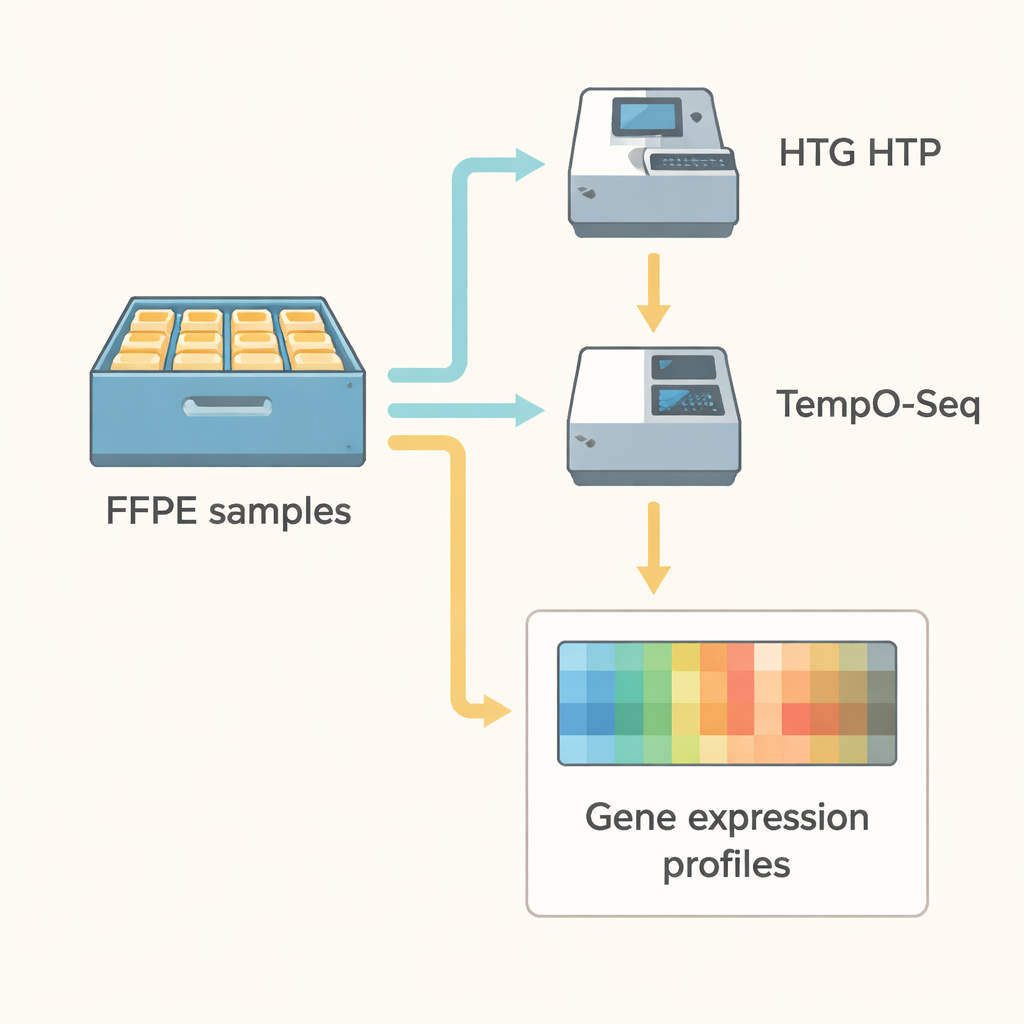
Проверка методов в деле
Команда сравнила эти две технологии лицом к лицу в очень практических условиях. Они проанализировали 21 сохранённый образец рака эндометрия, а также три эталонных материала РНК, сначала с помощью HTG HTP, а затем с TempO‑Seq. Оба метода использовали таргетные панели, которые в совокупности охватывали более 18 000 одинаковых генов. Учёные применили строгие проверки качества, убедившись, что каждое образец дал достаточное число прочтений секвенирования и что измерения стабильны. Также были использованы статистические методы для удаления «пакетных эффектов» — искусственных различий, которые могут появляться просто из‑за того, что тесты выполнялись в разные дни, на разных машинах или платформах.
Что совпадает, а что нет
При анализе уровня экспрессии отдельных генов по одному методы не всегда соглашались. Различия в проектировании зондов, подготовке образцов и подсчёте прочтений у каждой технологии могут сделать сравнение по одному гену шумным. Однако картина меняется, если рассматривать более широкие паттерны, объединяющие информацию многих генов одновременно. Многоgenные сигнатуры — например те, что используются для группировки опухолей по молекулярным подтипам, оценки доли иммунных клеток в образце или оценки чистоты опухолевой ткани — показали заметно лучшее согласование между TempO‑Seq и HTG. В большинстве случаев баллы или классификации были схожи, даже после того как исследователи смоделировали использование меньшего числа прочтений, имитируя разные мощности секвенирования.
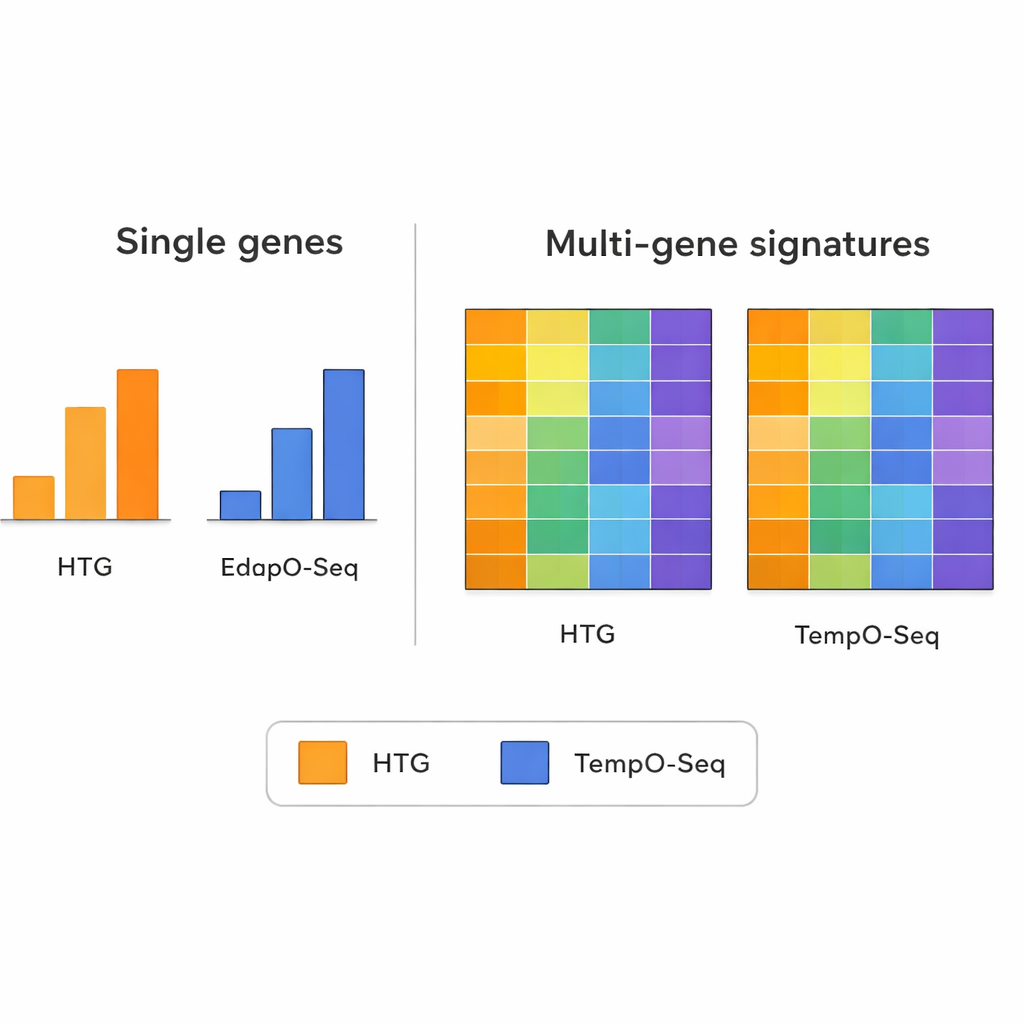
Много‑генные паттерны как надёжные сигналы
Исследование подчёркивает важный принцип современной геномики: хотя измерение любого отдельного гена может быть искажено техническими артефактами, объединение сигналов десятков или сотен генов, как правило, усредняет этот шум. Авторы использовали несколько широко известных много‑генных инструментов в качестве технических стресс‑тестов. Среди них — панель для рака молочной железы, назначающая опухоли к внутренним подтипам, алгоритм, оценивающий долю иммунной и стромальной ткани в образце, и метод, оценивающий пропорции различных типов иммунных клеток. По этим сложным показателям TempO‑Seq обычно тесно коррелировал с HTG, что даёт основание полагать: хотя некоторые тонкие детали могут различаться, обе платформы считывают одинаковые биологические сигналы.
Что это значит в дальнейшем
Для исследователей, опирающихся на архивы FFPE при изучении рака, потеря надёжной платформы могла быть серьёзной проблемой. Эта бенчмаркинговая работа приносит уверенность: TempO‑Seq выглядит достойной заменой HTG HTP, когда цель — использовать много‑генные биомаркеры и широкие паттерны экспрессии, которые лежат в основе многих современных диагностических и прогностических инструментов. Авторы предупреждают, что прямое сравнение результатов по отдельным генам между платформами нежелательно, поскольку каждая методика таргетирует гены немного по‑своему. Вместо этого они рекомендуют ориентироваться на сложные, много‑генные сигнатуры при работе между платформами. Простыми словами, новая методика, по всей видимости, способна продолжить работу своего предшественника для большинства прикладных задач онкологической науки, особенно когда важен общий рисунок многих генов, а не точное значение одного.»
Цитирование: Fernández-Serra, A., López-Reig, R., Romero, I. et al. Comparative evaluation of HTG and TempO Seq targeted transcriptome profiling methods. Sci Rep 16, 6108 (2026). https://doi.org/10.1038/s41598-026-36810-w
Ключевые слова: транскриптомный профиль, рак эндометрия, FFPE ткань, таргетное секвенирование РНК, биомаркеры экспрессии генов