Clear Sky Science · ru
Разработка и валидация мышиной модели тройного негативного рака молочной железы с положительной экспрессией PSMA для доклинических таргетных радионуклидных терапий
Почему это исследование важно
Тройной негативный рак молочной железы — одна из самых труднолечимых форм рака молочной железы. Он склонен быстро распространяться, для пациентов доступно меньше таргетных опций лечения, и он часто рецидивирует после стандартной терапии. В то же время новый класс «умных» радиационных препаратов, нацеленных на молекулу PSMA, преобразил подход к лечению распространённого рака простаты. В этом исследовании поставлен простой, но важный вопрос: можно ли создать реалистичную лабораторную модель тройного негативного рака молочной железы, содержащую тот же PSMA-мишень, чтобы честно оценить, смогут ли эти «умные» радиопрепараты помочь и при этой агрессивной форме рака груди?
От мишени простаты к вызову в раке молочной железы
PSMA (простатспецифический мембранный антиген) — небольшая структура на поверхности некоторых клеток. Он широко представлен при многих раках простаты и распознаётся радиоактивными препаратами, которые как выявляют опухоли на сканах, так и доставляют им излучение. Исследователи недавно обнаружили, что PSMA также встречается, в различной степени, в сосудах и клетках нескольких других опухолей, включая тройной негативный рак молочной железы. Однако в этих непроостатических опухолях PSMA обычно фокальный и слабее экспрессируется, что затрудняет прогнозирование эффективности PSMA-направленных терапий. Перед тем как пробовать новые лечения на пациентах, учёным нужны животные модели, которые достоверно воспроизводят этот рисунок экспрессии PSMA в опухолях молочной железы — а это оказалось неожиданно трудно реализовать.
Испытание множества моделей опухолей, которые отказывались сотрудничать
Команда сначала изучила широкий спектр существующих мышиных моделей тройного негативного рака молочной железы, используя как мышиные, так и человеческие раковые клеточные линии, имплантированные в разные места и при разных условиях. Они варьировали число вводимых клеток, добавляли поддерживающие гели для стимуляции ангиогенеза и даже смешивали клетки человеческих сосудов в надежде повысить уровень PSMA. Для каждой модели оценивали надёжность приживаемости и роста опухолей, исследовали срезы опухолей под микроскопом и использовали ПЭТ-трейсер, нацеленный на PSMA, чтобы увидеть, светились ли опухоли на сканах всего тела. Несмотря на выраженный рост опухолей и плотную сеть сосудов, ни одна из 23 моделей не показала существенной экспрессии PSMA ни в тканевой окраске, ни на ПЭТ. Опухоли выглядели активными и хорошо васкуляризованными, но конкретная «стоянка» PSMA, необходимая исследователям, фактически отсутствовала.
Создание опухоли, демонстрирующей нужную мишень
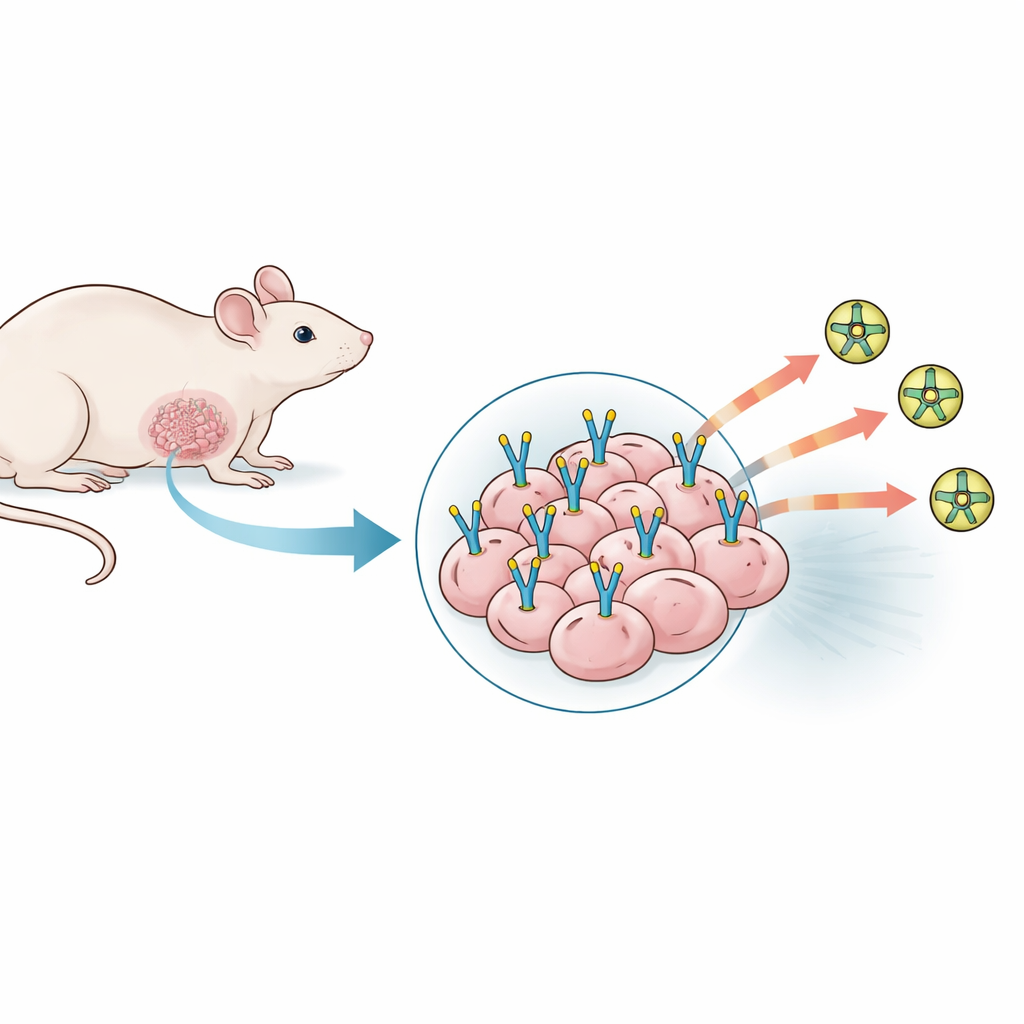
Столкнувшись с этим препятствием, исследователи пошли более прямым путём. Они генетически модифицировали широко используемую человеческую клеточную линию тройного негативного рака молочной железы MDA-MB-231, заставив её экспрессировать PSMA на поверхности. Эти изменённые клетки имплантировали в жировую подушку молочной железы иммунодефицитных мышей — место, лучше моделирующее естественную среду молочной железы. Учёные создали две версии модели: одну, в которой все опухолевые клетки экспрессировали PSMA, и «смешанную» опухоль, содержащую равные пропорции PSMA-положительных и обычных раковых клеток, чтобы имитировать пятнистый рисунок, наблюдаемый у пациентов. Обе модели образовывали опухоли с той же надёжностью и росли с похожей скоростью, как и опухоли из немодифицированных клеток, показав, что добавление PSMA не меняет поведение самой опухоли необычным образом.
Видимость новой мишени на сканах и под микроскопом
После введения ПЭТ-трейсера, нацеленного на PSMA, созданные опухоли ярко светились на сканах: захват в опухоли был примерно в десять раз выше, чем в печени или мышце. Этот сильный и селективный сигнал подтвердил, что PSMA теперь обильно представлен на раковых клетках и доступен циркулирующему препарату. Микроскопический анализ ткани опухоли подтвердил данные: окраска на PSMA была высокой, но неоднородной, с участками более сильной и более слабой экспрессии, напоминая гетерогенный рисунок, наблюдаемый при человеческом тройном негативном раке молочной железы. Важно, что добавленный PSMA был ограничен опухолевыми клетками, а не сосудами в окружении, что делает модель пригодной для оценки клеточно-направленных терапий. Участки некроза внутри больших опухолей не накапливали трейсер, что совпадает с клиническими наблюдениями.
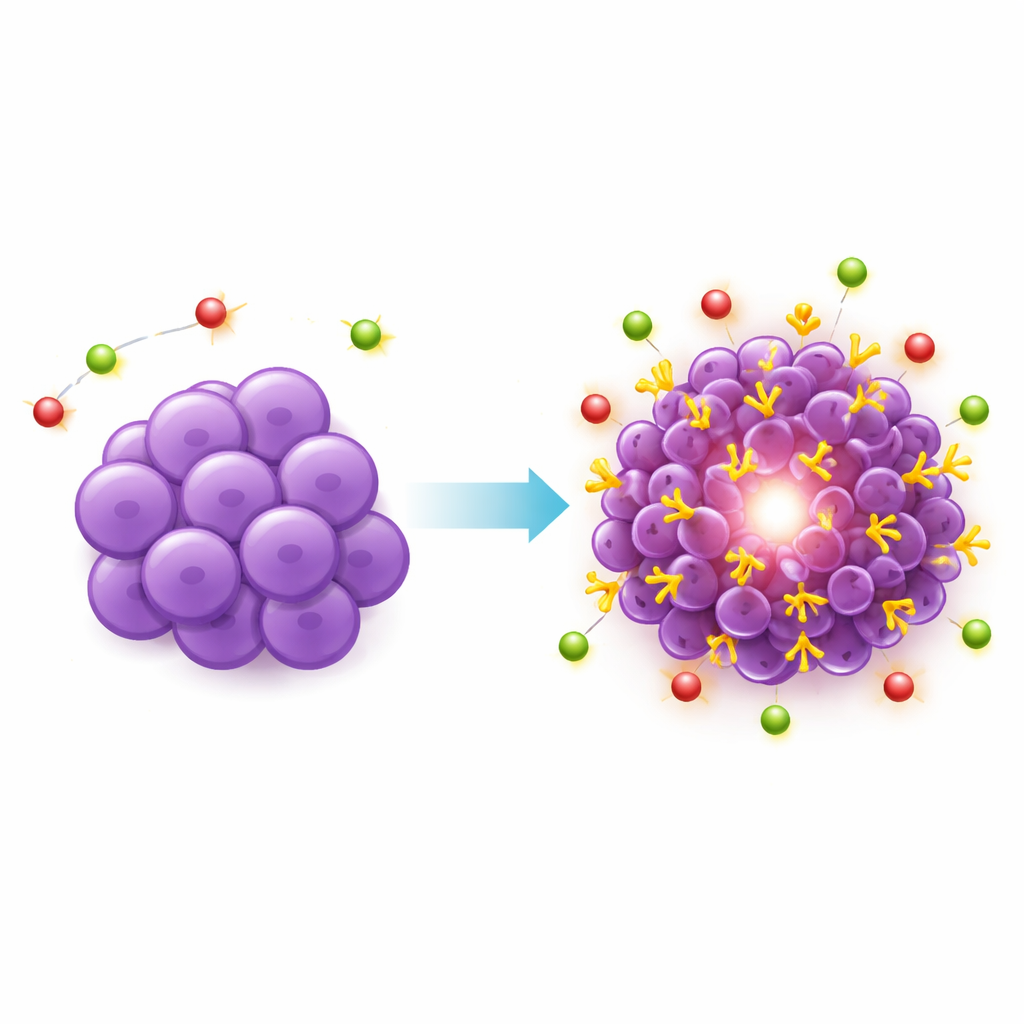
Что это значит для будущих методов лечения
Показав системно, что стандартные мышиные модели рака молочной железы ненадёжно экспрессируют PSMA, а затем создав новую модель, которая это делает, эта работа предоставляет важную тестовую платформу для следующего поколения таргетных радиационных терапий. PSMA-положительная модель тройного негативного рака молочной железы стабильна, растёт предсказуемо и демонстрирует реалистичное сочетание областей с высокой и низкой экспрессией PSMA, что делает её пригодной для оценки поведения PSMA-ориентированных препаратов перед их применением у пациентов. Хотя модель не может отразить все аспекты человеческого заболевания — например влияние полноценно функционирующей иммунной системы — она даёт мощный инструмент для изучения, сможет ли успех PSMA-основанных терапий при раке простаты однажды распространиться и на людей с этой особенно агрессивной формой рака молочной железы.
Цитирование: Chaussin, B., Sanchez, L., Levesque, S. et al. Development and validation of a PSMA-positive triple-negative breast cancer mouse model for preclinical targeted radionuclide therapies. Sci Rep 16, 9348 (2026). https://doi.org/10.1038/s41598-026-36724-7
Ключевые слова: тройной негативный рак молочной железы, PSMA, таргетная радионуклидная терапия, доклиническая мышиная модель, ПЭТ-визуализация