Clear Sky Science · ru
Идентификация и верификация SPP1 в аноикисе как прогностического биомаркера для кишечной метаплазии и рака желудка
Почему это важно для здоровья желудка
Рак желудка — один из самых смертельных видов рака в мире, в основном потому, что его часто обнаруживают на поздних стадиях. Перед появлением развившейся опухоли слизистая желудка часто проходит предвестниковую стадию, называемую кишечной метаплазией, при которой нормальные клетки желудка начинают напоминать клетки кишечника. В этом исследовании прослеживается весь этот путь — от здоровой ткани через кишечную метаплазию до рака желудка — с целью найти единый измеримый сигнал в ткани, который мог бы ранне выявлять высокий риск и помогать врачам прогнозировать, у каких пациентов прогноз хуже и кто может потребовать более тщательного наблюдения или новых методов лечения.
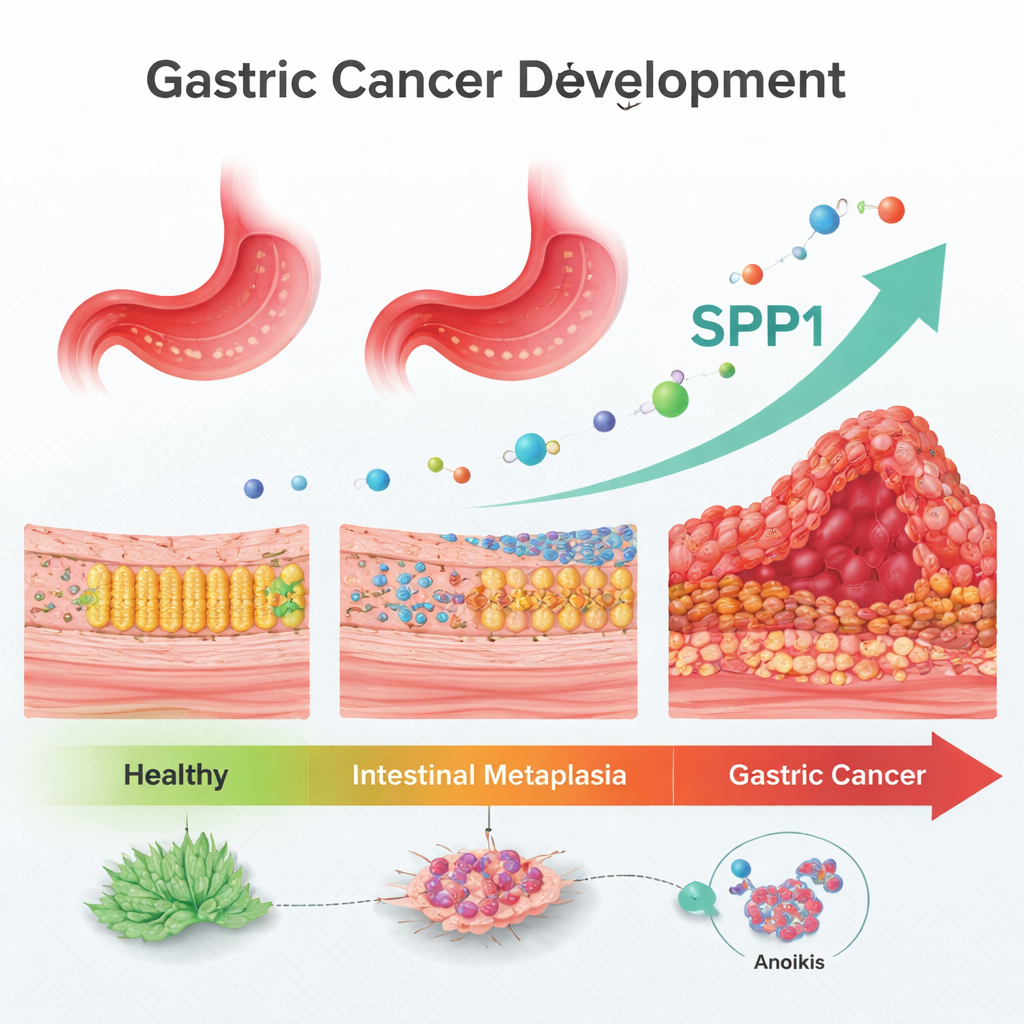
Перекресток на пути к раку
Врачи давно знают, что кишечная метаплазия является предраковым состоянием, но им не хватает надежных маркеров, которые бы предсказывали, у кого действительно разовьется рак. Исследователи сосредоточились на типе клеточной гибели, называемом аноикис, который обычно уничтожает клетки, отделяющиеся от своего нормального места в ткани. Клетки рака должны научиться сопротивляться аноикису, чтобы перемещаться, выживать в крови и давать метастазы. Разрабатывая анализ больших публичных генетических баз данных сотен пациентов, команда искала гены, связанные с аноикисом, которые последовательно меняются по мере прохождения «каскада Корреа»: от здоровой слизистой желудка через кишечную метаплазию до рака желудка.
Фокус на ключевой предупредительной молекуле
С помощью продвинутых статистических методов и сетевого анализа ученые многократно выделяли один заметный ген: SPP1, кодирующий белок, также известный как остеопонтин. В трёх независимых наборах данных уровни SPP1 были последовательно низкими в здоровой ткани желудка, выше при кишечной метаплазии и наивысшими при раке желудка. Этот ступенчатый паттерн сохранялся даже после корректировки технических различий между исследованиями. Дальнейшие компьютерные анализы тысяч генов показали, что высокий уровень SPP1 часто сопровождался изменениями в иммунных путях и реакциях на экологический и химический стресс, что предполагает, что молекула может связывать вместе выживание клеток, хроническое раздражение и иммунную систему в процессе развития рака.
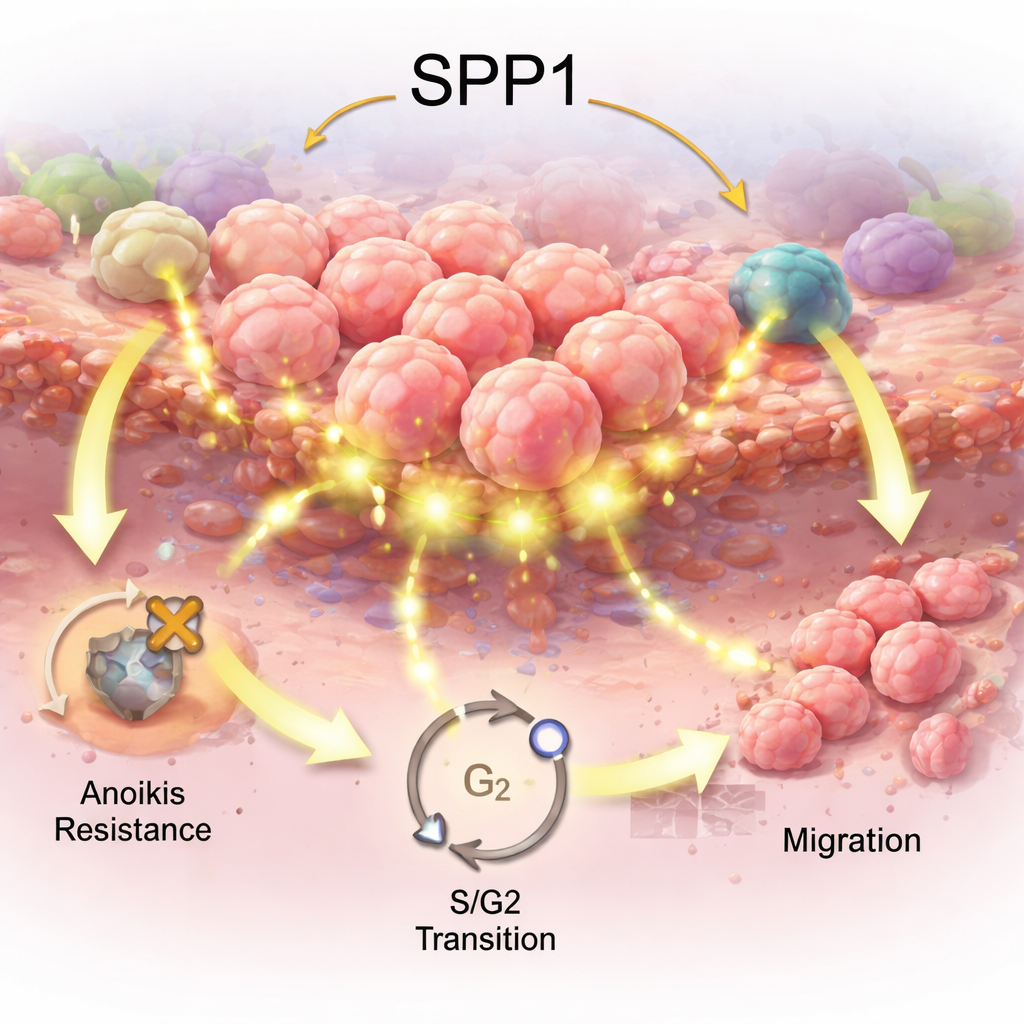
Подсказки от клеток защитной системы организма
Далее команда изучила, как SPP1 соотносится с иммунными клетками, инфильтрирующими опухоли. В массовых образцах опухолей повышенный уровень SPP1 связывался со сдвигами в соотношении иммунных клеток, включая увеличение определённых макрофагов и Т-клеток, которые могут либо атаковать опухоль, либо быть подавлены ею. Одноклеточное секвенирование РНК — чтение активности генов по одной клетке — показало, что SPP1 сильно включён в опухоле-ассоциированных макрофагах и других клетках микроокружения опухоли. Сигналы с участием SPP1 и его партнёрного рецептора CD44, по-видимому, связывали эти макрофаги с хелперными Т-клетками, что указывает на то, что этот путь может формировать иммунный «квартал», благоприятный для выживания опухоли, а не для её уничтожения. Хотя эти связи коррелятивны, они выдвигают SPP1 как потенциального участника механизмов уклонения желудочных опухолей от иммунной атаки.
От больших данных к реальным тканям и клеткам
Чтобы проверить соответствие вычислительных выводов реальности, исследователи измерили SPP1 в 32 образцах желудочной ткани человека. И генетические, и белковые тесты показали ту же тенденцию: минимальные уровни в нормальной ткани, выше — при кишечной метаплазии и наивысшие — при раке желудка. У пациентов с опухолями, экспрессирующими больше SPP1, было значительно хуже общая выживаемость, а статистические модели показывали, что SPP1 помогал прогнозировать исходы на один, три и пять лет. В культурах клеток подавление SPP1 в линии клеток рака желудка замедляло рост клеток, снижало их миграционную способность, увеличивало программируемую гибель и вызывало задержку клеток в критической фазе клеточного цикла. Эти эксперименты подтверждают идею о том, что SPP1 активно помогает раковым клеткам противостоять гибели и продолжать делиться.
Что это может значить для пациентов
Для неспециалистов основной вывод таков: SPP1 ведёт себя как нарастающий сигнал тревоги на пути от «рискованной, но ещё не раковой» слизистой желудка к полноценному раку. Высокие уровни этой молекулы отмечают ткани, которые с большей вероятностью прогрессируют, и пациентов с худшими прогнозами. Хотя необходимы дополнительные исследования — в частности, более крупные клинические исследования и опыты на животных — мониторинг SPP1 в биоптатах кишечной метаплазии мог бы в будущем помочь врачам решать, кому требуется более тщательное наблюдение или более раннее лечение. При уже развившемся раке желудка препараты, блокирующие SPP1 или его ключевых партнёров, могли бы ослабить защиту опухоли — как делая раковые клетки более уязвимыми к гибели, так и перестраивая окружающие иммунные клетки для более эффективной борьбы с заболеванием.
Цитирование: Wu, K., Ye, Y., Pei, B. et al. Identification and verification of SPP1 in anoikis as a prognostic biomarker for intestinal metaplasia and gastric cancer. Sci Rep 16, 5842 (2026). https://doi.org/10.1038/s41598-026-36714-9
Ключевые слова: рак желудка, кишечная метаплазия, биомаркеры, остеопонтин SPP1, опухолевый микроокружение